8.化学小组同学发现在面包制作过程中加入了一些白色粉末,使面包变得松软.同学们对白色粉末的成分进行探究.
【查阅资料】①经调查,市场上有以下3种主要产品.
②氨气(NH3)是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
③2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑; NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑; 2NH3+H2SO4═(NH4)2SO4
【实验准备】同学们选用下列实验装置,经组合进行实验:
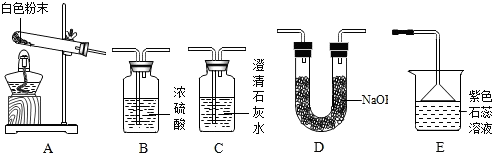
【实验记录】
【实验分析】
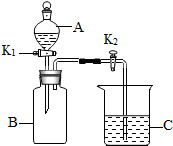
根据上述实验,甲同学认为该粉末的主要成分为食臭粉,乙同学认为上述实验不能确定该粉末为食臭粉.为进一步确认其组成及含量,同学们设计了如下定量实验:
(1)实验3中装置B的作用是除尽水蒸气和氨气.
(2)实验3中测得装置D增重a g,a的范围是>4.4.
(3)若测得a为92.4,该碱性膨松剂中NaHCO3与NH4HCO3的质量比为3360:79(结果用最简整数比表示).
0 166126 166134 166140 166144 166150 166152 166156 166162 166164 166170 166176 166180 166182 166186 166192 166194 166200 166204 166206 166210 166212 166216 166218 166220 166221 166222 166224 166225 166226 166228 166230 166234 166236 166240 166242 166246 166252 166254 166260 166264 166266 166270 166276 166282 166284 166290 166294 166296 166302 166306 166312 166320 211419
【查阅资料】①经调查,市场上有以下3种主要产品.
| 商品名称 | 小苏打 | 食臭粉 | 混合碱性膨松剂 |
| 主要成分 | 碳酸氢钠 | 碳酸氢铵 | 碳酸氢钠和碳酸氢铵 |
③2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑; NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑; 2NH3+H2SO4═(NH4)2SO4
【实验准备】同学们选用下列实验装置,经组合进行实验:

【实验记录】
| 实验序号 | 实验装置 | 实验现象 | 实验结论及分析 |
| 实验1 | 选用A、B、C | C中澄清石灰水变浑浊 | 有CO2生成,C中反应的化学方程式是 CO2+Ca(OH)2═CaCO3↓+H2O |
| 实验2 | 选用A、 D和E | E中紫色石蕊溶液变成 蓝色 | 有NH3生成 |
根据上述实验,甲同学认为该粉末的主要成分为食臭粉,乙同学认为上述实验不能确定该粉末为食臭粉.为进一步确认其组成及含量,同学们设计了如下定量实验:
| 实验序号 | 实验目的 | 实验装置 | 数据记录 | 实验结论 |
| 实验3 | 测定生成CO2的质量 | 选用A、B、D | 装置D增重a g | 该粉末为“混合碱性膨松剂” |
| 实验4 | 测定生成NH3的质量 | 选用A、B、D | 装置B增重1.7g |
(2)实验3中测得装置D增重a g,a的范围是>4.4.
(3)若测得a为92.4,该碱性膨松剂中NaHCO3与NH4HCO3的质量比为3360:79(结果用最简整数比表示).
 以下为初中化学常见物质,由H、C、O、S、Na、Ca、Fe等元素组成.
以下为初中化学常见物质,由H、C、O、S、Na、Ca、Fe等元素组成.
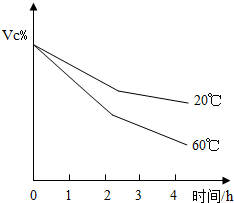 兴趣小组的同学对食品中含有的维生素C(化学式为C6H8O6,可表示为Vc)进行探究.
兴趣小组的同学对食品中含有的维生素C(化学式为C6H8O6,可表示为Vc)进行探究.