3.原子中( )
| A. | 质子数和中子数相等 | B. | 中子数和电子数相等 | ||
| C. | 质子数和电子数相等 | D. | 质子数大于电子数 |
2.水受热变成水蒸气是因为( )
| A. | 水分子被破坏 | B. | 水分子的间隔增大了 | ||
| C. | 水分子的间隔变小了 | D. | 水发生了分解反应 |
1.下列各物质的化学名称和俗称与化学式不相符的是( )
| A. | 碳酸钠 纯碱 NaHCO3 | B. | 氯化钠 食盐 NaCl | ||
| C. | 汞 水银 Hg | D. | 氢氧化钙 消石灰 Ca(OH)2 |
19.根据下列装置图,按要求回答问题.
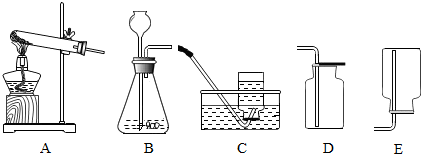
(1)中考化学实验考查要求组装氯酸钾和二氧化锰制取较纯净的氧气,应选择图中的AC装置.若改用高锰酸钾,装置须改动的地方是在试管口塞一团棉花.实验结束后,应先移出导管,后停止加热.
(2)若重组一套装置制取二氧化碳气体,你会选择BD.选择这套装置的原因是二氧化碳密度大于空气,能溶于水和二氧化碳密度大于空气,能溶于水.一丰在进行该实验前对装置B进行了气密性检查,具体方法是将注射器连接在装置B 的右端导管处.在拉动注射器的同时,若气密性良好,我们将会看到长颈漏斗末端冒出气泡.
实验结束后,小豪、佳琪和宇飞就试管中“废液”的成分产生争议.几位同学对此进行了如下实验:
①小豪用pH试纸测得试剂瓶中液体的pH值=1,由此推断液体中一定含有溶于水的氯化钙、
稀盐酸和水三种物质.
②佳琪将一颗生锈的铁钉放入少量废液中,开始看到铁锈消失,溶液变黄.一段时间后还可能看到有气泡冒出,该反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.
③宇飞想对废液先中和,然后回收氯化钙.他忽然想到,如果把检验CO2后集气瓶内变浑浊的“石灰水”与废液按一定比例混合就能达到预期效果.于是,他和其他同学一起设计了如下实验:
【步骤一】:用实验确认集气瓶内变浑浊的“石灰水”的成分:
【步骤二】:确认集气瓶内变浑浊的“石灰水”与废液恰好完全反应:
他取少量集气瓶内变浑浊的“石灰水”于试管中,滴加几滴无色酚酞后变红,逐滴加入废液,看到现象时说明恰好反应.发生反应的方程式①无气泡生成,溶液变为无色,②Ca(OH)2+2HCl=CaCl2+2H2O.
【步骤三】从反应后的溶液中获取氯化钙晶体可采用蒸发结晶方法.

(1)中考化学实验考查要求组装氯酸钾和二氧化锰制取较纯净的氧气,应选择图中的AC装置.若改用高锰酸钾,装置须改动的地方是在试管口塞一团棉花.实验结束后,应先移出导管,后停止加热.
(2)若重组一套装置制取二氧化碳气体,你会选择BD.选择这套装置的原因是二氧化碳密度大于空气,能溶于水和二氧化碳密度大于空气,能溶于水.一丰在进行该实验前对装置B进行了气密性检查,具体方法是将注射器连接在装置B 的右端导管处.在拉动注射器的同时,若气密性良好,我们将会看到长颈漏斗末端冒出气泡.
实验结束后,小豪、佳琪和宇飞就试管中“废液”的成分产生争议.几位同学对此进行了如下实验:
①小豪用pH试纸测得试剂瓶中液体的pH值=1,由此推断液体中一定含有溶于水的氯化钙、
稀盐酸和水三种物质.
②佳琪将一颗生锈的铁钉放入少量废液中,开始看到铁锈消失,溶液变黄.一段时间后还可能看到有气泡冒出,该反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.
③宇飞想对废液先中和,然后回收氯化钙.他忽然想到,如果把检验CO2后集气瓶内变浑浊的“石灰水”与废液按一定比例混合就能达到预期效果.于是,他和其他同学一起设计了如下实验:
【步骤一】:用实验确认集气瓶内变浑浊的“石灰水”的成分:
| 操作 | 现象 | 结论 |
| (1) | (1)仍有没反应的氢氧化钙 | |
| (2) | (2)还含有生成的碳酸钙 |
他取少量集气瓶内变浑浊的“石灰水”于试管中,滴加几滴无色酚酞后变红,逐滴加入废液,看到现象时说明恰好反应.发生反应的方程式①无气泡生成,溶液变为无色,②Ca(OH)2+2HCl=CaCl2+2H2O.
【步骤三】从反应后的溶液中获取氯化钙晶体可采用蒸发结晶方法.
18.已知某铝合金的成分除铝外,还含有铁、铜中的一种或两种.某化学兴趣小组对合金中铁、铜的存在情况进行如下探究:
查阅资料】铝与氢氧化钠溶液反应,生成偏铝酸钠[NaAlO2,溶于水],反应的化学方程式为
2Al+2NaOH+2H2O=2NaAlO2+3H2↑,铁、铜不与氢氧化钠溶液反应.
【做出猜想】
猜想一:该合金中除铝外,还含有铁.
猜想二:该合金中除铝外,还含有铜.
猜想三:该合金中除铝外,还含有铜和铁.
【实验探究】该小组同学进行了如下实验.请你完成下表,写出他们所用的试剂和实验现象.
【知识拓展】以上实验能否说明铁和铜的金属性强弱?若能,请简述理由.铁能与盐酸反应,而铜不能与盐酸反应.
查阅资料】铝与氢氧化钠溶液反应,生成偏铝酸钠[NaAlO2,溶于水],反应的化学方程式为
2Al+2NaOH+2H2O=2NaAlO2+3H2↑,铁、铜不与氢氧化钠溶液反应.
【做出猜想】
猜想一:该合金中除铝外,还含有铁.
猜想二:该合金中除铝外,还含有铜.
猜想三:该合金中除铝外,还含有铜和铁.
【实验探究】该小组同学进行了如下实验.请你完成下表,写出他们所用的试剂和实验现象.
| 实验步骤 | 实验现象 | 结论或解释 |
| ①取适量的合金粉末于烧杯中,加入过量的氢氧化钠,充分反应 | 除去合金粉末中铝 | |
| ②将步骤①所得物质过滤,再向滤渣中加入过量的稀盐酸,充分反应. | 猜想三成立 |
15.森林初发火灾时,可以使用爆炸灭火的方法,将灭火弹抛到火场将火扑灭.关于爆炸灭火的原因分析的不合理的是( )
0 165992 166000 166006 166010 166016 166018 166022 166028 166030 166036 166042 166046 166048 166052 166058 166060 166066 166070 166072 166076 166078 166082 166084 166086 166087 166088 166090 166091 166092 166094 166096 166100 166102 166106 166108 166112 166118 166120 166126 166130 166132 166136 166142 166148 166150 166156 166160 166162 166168 166172 166178 166186 211419
| A. | 爆炸气浪降低了可燃物的着火点 | |
| B. | 爆炸时燃烧处于暂时缺氧状态 | |
| C. | 爆炸气浪降低了可燃物的温度 | |
| D. | 炸起的沙土覆盖了可燃物,隔绝空气 |
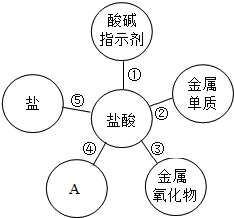 归纳是重要的学习方法,小红在复习盐酸的性质是,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).
归纳是重要的学习方法,小红在复习盐酸的性质是,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).