11.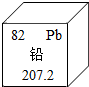 近年来,部分儿童血铅超标事件,倍受社会各界关注.铅元素相关信息如图所示.下列说法中,不正确的是( )
近年来,部分儿童血铅超标事件,倍受社会各界关注.铅元素相关信息如图所示.下列说法中,不正确的是( )
 近年来,部分儿童血铅超标事件,倍受社会各界关注.铅元素相关信息如图所示.下列说法中,不正确的是( )
近年来,部分儿童血铅超标事件,倍受社会各界关注.铅元素相关信息如图所示.下列说法中,不正确的是( )| A. | 铅原子核内有82个质子 | B. | 铅有毒,儿童不能使用铅笔 | ||
| C. | 相对原子质量为207.2 | D. | 该元素属于金属元素 |
10.镁能够在二氧化碳气体中燃烧,方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO,下列关于该反应判断正确的( )
| A. | C有还原性,是该反应的还原剂 | |
| B. | 二氧化碳发生还原反应,具有还原性 | |
| C. | 镁带失火,不可以用二氧化碳灭火 | |
| D. | 该反应中所有元素均存在化合价的变化 |
9.科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为 4NH3+3O2$\frac{\underline{\;\;△\;\;}}{\;}$2X+6H2O,则X的化学式为( )
| A. | N2 | B. | O3 | C. | H2 | D. | NO2 |
8.根据实践经验,你认为下列家庭小实验不能成功的是( )
| A. | 鸡蛋放入醋中变成“软壳蛋” | B. | 用肥皂水区别硬水和软水 | ||
| C. | 用回火后的钢针作鱼钩 | D. | 用自来水清除盛石灰水瓶壁的白膜 |
3.某兴趣小组的同学对实验室里久置于空气中变质的过氧化钠(Na2O2)固体的成分进行探究.
【查阅资料】
(1)过氧化钠化学性质很活泼,能与水、二氧化碳反应.其中相关反应:2Na2O2+2H2O=4NaOH+O2↑ 2Na2O2+2CO2=2Na2CO3+O2
(2)Ba(NO3)2溶液、NaNO3溶液均为中性溶液
【猜想与假设】猜想Ⅰ:固体为Na2O2、NaOH、Na2CO3的混合物
猜想Ⅱ:固体为NaOH、Na2CO3的混合物
猜想Ⅲ:固体为NaOH
猜想Ⅳ:固体为Na2CO3
【实验推断】
【反思评价】过氧化钠在变质成碳酸钠过程中除了资料中显示的两个反应外,还可能发生了其他反应,请把该反应的化学方程式写在下列横线上:CO2+2NaOH═Na2CO3+H2O.
【拓展迁移】小组同学认识到过氧化钠(Na2O2)应该密封保存.
0 165711 165719 165725 165729 165735 165737 165741 165747 165749 165755 165761 165765 165767 165771 165777 165779 165785 165789 165791 165795 165797 165801 165803 165805 165806 165807 165809 165810 165811 165813 165815 165819 165821 165825 165827 165831 165837 165839 165845 165849 165851 165855 165861 165867 165869 165875 165879 165881 165887 165891 165897 165905 211419
【查阅资料】
(1)过氧化钠化学性质很活泼,能与水、二氧化碳反应.其中相关反应:2Na2O2+2H2O=4NaOH+O2↑ 2Na2O2+2CO2=2Na2CO3+O2
(2)Ba(NO3)2溶液、NaNO3溶液均为中性溶液
【猜想与假设】猜想Ⅰ:固体为Na2O2、NaOH、Na2CO3的混合物
猜想Ⅱ:固体为NaOH、Na2CO3的混合物
猜想Ⅲ:固体为NaOH
猜想Ⅳ:固体为Na2CO3
【实验推断】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体的于试管中,加水振荡制直至完全溶解. | 不产生气泡 | 猜想Ⅰ不成立. |
| ②取少量①的溶液于试管中,滴加过量的Ba(NO3)2溶液. | 产生白色沉淀 | 证明有Na2CO3存在.化学反应方程为:Na2CO3+Ba(NO3)2═BaCO3↓+2NaNO3 |
| ③取少量②的溶液于试管中,滴加无色酚酞试液. | 酚酞试液变红 | 证明NaOH存在. |
| 结合以上实验现象,说明猜想Ⅱ是成立的. | ||
【拓展迁移】小组同学认识到过氧化钠(Na2O2)应该密封保存.
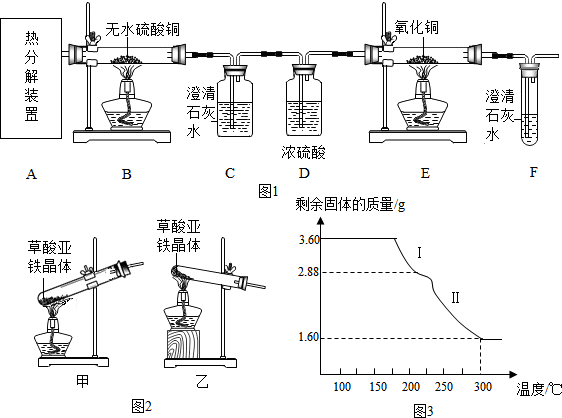
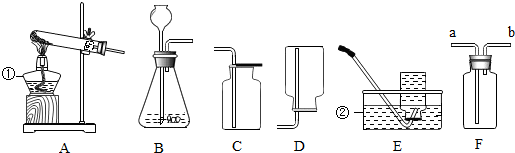
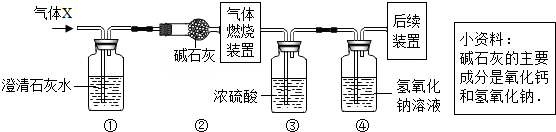
 生活中处处有化学.
生活中处处有化学.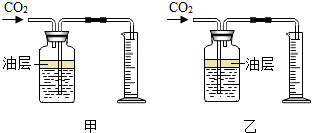 化学兴趣小组测定某石灰石样品中碳酸钙的质量分数
化学兴趣小组测定某石灰石样品中碳酸钙的质量分数