2.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 分子是构成物质的微粒,物质都是由分子构成的 | |
| B. | 氧化物一定含氧元素,含氧元素的物质一定是氧化物 | |
| C. | 中和反应生成盐和水,生成盐和水的反应一定是中和反应 | |
| D. | 酸性较强的溶液能使石蕊溶液变红,能使石蕊溶液变红的溶液一定呈酸性 |
1.河南是产粮大省,小麦年产量占全国总量的四分之一,其主要成分淀粉的化学式是(C6H10O5)n.下列有关淀粉的说法错误的是( )
| A. | 淀粉属于有机化合物 | |
| B. | 淀粉在人体内经过一系列反应能为人体活动提供能量 | |
| C. | 每个分子中含有6n个碳原子 | |
| D. | 淀粉中碳、氢、氧元素的质量比为6:10:5 |
20. 把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )
把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )
 把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )
把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )| A. | 分子总是不断运动的 | |
| B. | 分子间都是有间隔的 | |
| C. | 相同条件下,NO2气体的密度大于H2的密度 | |
| D. | 分子间有吸引力 |
19.10克不纯的MgCO3(含杂质M)和10克不纯的Na2CO3(含杂质N)分别与足量的稀盐酸反应后,都得到4.4克二氧化碳,则M、N可能是( )
| A. | M为CaCO3,N为MgCO3 | B. | M为BaCO3,N为KHCO3 | ||
| C. | M为K2CO3,N为NaHCO3 | D. | M为Na2CO3,N为ZnCO3 |
18.下列对部分化学知识的归纳完全正确的一组是( )
| A、化学与生活 | B、化学与环境 |
| ①生活中常用加热煮沸的方法软化硬水 ②干冰用于人工降雨 ③农业上熟石灰不能和氯化铵同时施用 | ①焚烧植物秸杆会造成空气污染 ②PM2.5是造成雾霾天气的元凶之一 ③保护金属资源只能通过防止金属腐蚀实现 |
| C、化学与安全 | D、化学与健康 |
| ①在室内放一盆水,可防止煤气中毒 ②夜间发现液化气泄漏开灯寻找泄漏源 ③煤矿井下严禁烟火 | ①人体缺铁会引起贫血 ②用甲醛的水溶液浸泡海产品保鲜 ③过量食用加碘食盐会引起甲状腺肿大 |
| A. | A | B. | B | C. | C | D. | D |
17.下列应用的原理(用化学方程式表示)及反应的基本类型中有错误的是( )
| 选项 | 应用 | 化学方程式 | 反应类型 |
| A | 用赤铁矿炼铁 | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | 置换反应 |
| B | 用熟石灰中和硫酸厂污水中的残余硫酸 | Ca(OH)2+H2SO4=CaSO4+2H2O | 复分解反应 |
| C | 加热混有二氧化锰的氯酸钾制取氧气 | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ | 分解反应 |
| D | 用红磷测定空气中氧气的含量 | 4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5 | 化合反应 |
| A. | A | B. | B | C. | C | D. | D |
15. 实验室里有一瓶保管不当、标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图1所示),某兴趣小组对其组成进行如下探究.
实验室里有一瓶保管不当、标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图1所示),某兴趣小组对其组成进行如下探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,该瓶试剂不可能是A.
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ.CaCl2溶液和BaCl2溶液都呈中性.
Ⅱ.初中化学中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3,其中一种物质的类别有别于其它三种物质,该物质是氢氧化钠或NaOH.
Ⅲ.室温(20℃)时,四种物质的溶解度数据如下:
【资料分析】依据上述资料分析该瓶试剂也不可能是碳酸氢钠或NaHCO3.
【实验探究】
实验1:实验测得该溶液的pH>7,则这瓶试剂也不可能是氯化钠或NaCl.
实验2:为了检验该溶液是NaOH溶液还是Na2CO3溶液,又进行了如下实验:
取少量溶液于试管中,滴加足量的盐酸,有气泡产生,得出结论,该溶液是Na2CO3溶液.写出上述反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
实验3:有同学对实验2结论提出质疑,认为该溶液可能是部分变质的氢氧化钠溶液,请你设计实验来验证.写出实验步骤、现象和结论.
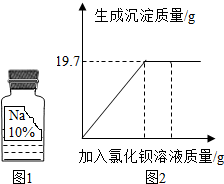
【计算】取试剂瓶中的溶液50g,逐滴加入一定溶质质量分数的BaCl2溶液.实验过程中,生成沉淀质量与加入BaCl2溶液的质量关系如图2所示,试计算溶液中碳酸钠的质量分数.
0 164917 164925 164931 164935 164941 164943 164947 164953 164955 164961 164967 164971 164973 164977 164983 164985 164991 164995 164997 165001 165003 165007 165009 165011 165012 165013 165015 165016 165017 165019 165021 165025 165027 165031 165033 165037 165043 165045 165051 165055 165057 165061 165067 165073 165075 165081 165085 165087 165093 165097 165103 165111 211419
 实验室里有一瓶保管不当、标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图1所示),某兴趣小组对其组成进行如下探究.
实验室里有一瓶保管不当、标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图1所示),某兴趣小组对其组成进行如下探究.【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,该瓶试剂不可能是A.
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ.CaCl2溶液和BaCl2溶液都呈中性.
Ⅱ.初中化学中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3,其中一种物质的类别有别于其它三种物质,该物质是氢氧化钠或NaOH.
Ⅲ.室温(20℃)时,四种物质的溶解度数据如下:
| 物质 | NaHCO3 | NaCl | NaOH | Na2CO3 |
| 溶解度g/100g水 | 9.6 | 36 | 109 | 215 |
【实验探究】
实验1:实验测得该溶液的pH>7,则这瓶试剂也不可能是氯化钠或NaCl.
实验2:为了检验该溶液是NaOH溶液还是Na2CO3溶液,又进行了如下实验:
取少量溶液于试管中,滴加足量的盐酸,有气泡产生,得出结论,该溶液是Na2CO3溶液.写出上述反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
实验3:有同学对实验2结论提出质疑,认为该溶液可能是部分变质的氢氧化钠溶液,请你设计实验来验证.写出实验步骤、现象和结论.
【计算】取试剂瓶中的溶液50g,逐滴加入一定溶质质量分数的BaCl2溶液.实验过程中,生成沉淀质量与加入BaCl2溶液的质量关系如图2所示,试计算溶液中碳酸钠的质量分数.