18.2011年为国际化学年,主题是“化学--人类的生活,人类的未来”.如表列出了几种与人类的生活和未来密切相关的物质:
(1)请按要求填写表格:
(2)从表中选择两种物质,说明其与人类生活的密切关系甲烷,熟石灰.
(3)由于物质的多样性,化学上通常用分类的方法认识物质.
①从应用物质的角度,人们常常根据物质的性质对物质进行分类,其原因在于物质的性质决定物质的用途.
(2)中两种物质分别利用了物质的哪些性质?甲烷的可燃性,熟石灰显碱性.
②研究物质的性质时,又常常根据物质的组成和结构对物质进行分类,其原因在于物质的结构决定物质的性质.请用上述6种物质中属于同一类的两种物质说明你的观点烧碱和熟石灰均显碱性.
(4)根据物质的组成,把题中6种物质分类,并将各物质的名称写在相应类别的后面.要求:用框图的形式表示,层次分明.
(1)请按要求填写表格:
| 物质编号 | A | B | C | D | E |
| 物质名称 | 烧碱 | 甲烷 | 铜 | 熟石灰 | 干冰 |
| 物质组成 (用化学式表示) | |||||
| 构成微粒 (用符号表示) |
(3)由于物质的多样性,化学上通常用分类的方法认识物质.
①从应用物质的角度,人们常常根据物质的性质对物质进行分类,其原因在于物质的性质决定物质的用途.
(2)中两种物质分别利用了物质的哪些性质?甲烷的可燃性,熟石灰显碱性.
②研究物质的性质时,又常常根据物质的组成和结构对物质进行分类,其原因在于物质的结构决定物质的性质.请用上述6种物质中属于同一类的两种物质说明你的观点烧碱和熟石灰均显碱性.
(4)根据物质的组成,把题中6种物质分类,并将各物质的名称写在相应类别的后面.要求:用框图的形式表示,层次分明.
17.下列关于溶液的说法中,正确的是( )
| A. | 食盐溶液各部分性质相同,是因为氯化钠分子均匀分散在水分子中 | |
| B. | 氯化氢的水溶液可以导电,是因为氯化氢溶液中有大量的自由移动的离子 | |
| C. | 80℃硝酸钾饱和溶液降温至20℃,溶液中的硝酸钾会全部析出 | |
| D. | 20℃,氯化钠的溶解度为36g,则20℃时氯化钠的饱和溶液中一定含有36g氯化钠 |
16.材料是时代进步的重要标志.下列有关材料的说法中,正确的是( )
| A. | 合金比纯金属性能优越,但是它们的组成和结构相同 | |
| B. | 只有通过化学变化,才能获取新材料 | |
| C. | 复合材料的性能优于组成它的成分材料,是因为混合后组成和结构发生了变化 | |
| D. | 用于远距离、大容量信息传输的光导纤维属于有机高分子材料 |
15.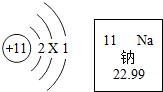 根据如图的有关信息判断,下列说法错误的是( )
根据如图的有关信息判断,下列说法错误的是( )
 根据如图的有关信息判断,下列说法错误的是( )
根据如图的有关信息判断,下列说法错误的是( )| A. | 钠原子的核电荷数为11 | |
| B. | 钠的原子结构示意图中X=8 | |
| C. | 钠原子的相对原子质量为22.99 | |
| D. | 在化学反应中,钠原子容易得到1个电子 |
14.下列关于化学史方面的叙述中,正确的是( )
| A. | 汤姆森通过α粒子轰击金箔实验,认识到原子是可分的 | |
| B. | 侯德榜是唯一研发出利用食盐制取纯碱的科学家 | |
| C. | 拉瓦锡最早通过实验得出空气中含有稀有气体 | |
| D. | 门捷列夫发现元素之间存在联系,排列出元素周期表,为化学研究做出了重大贡献 |
13.探究水壶内部水垢的主要成分
小花和小红同学非常善于进行实验探究,他们发现长期使用的热水壶底部有一层水垢,小花想这层水垢的主要成分是什么?围绕这个问题,他们展开了探究,请你也参入到他们的学习过程,并协助完成相关任务.
【提出问题】热水壶底部水垢的主要成分是什么?
【查阅资料】通过查阅资料知道,天然水和水垢所含的物质及其溶解性如表:
【提出猜想】通过分析,他们认为水垢的主要成分中一定含有Mg(0H)2和CaCO3(写化学式,下同),可能含有Ca(OH)2和MgCO3.
【设计方案,进行实验】
(1)小花在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,静置.取上层清液滴入Na2CO3溶液,如果没有白色沉淀生成,说明水垢中不含有Ca(0H)2(填化学式).
(2)欲证明水垢中含有碳酸盐的实验方法是取少量水垢于试管中,向试管中加入稀盐酸,有气泡产生,把生成的气体通入澄清石灰水中,石灰水变浑浊.
(3)为了进一步确定水垢中含有碳酸盐的成分,他们设计了下列实验装置.

Ⅰ.小花和小红的主要实验步骤如下:
①按如图1所示组装仪器,将50g水垢试样放入锥形瓶中,逐滴加入足量稀盐酸.
②待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气.
③称量D瓶内物质增加的质量.
④重复②和③的操作,直至D瓶内物质的质量不变.
经过上述实验,他们测量滴加稀盐酸的体积与D瓶内物质增加质量的关系如图2曲线所示.
Ⅱ.小花和小红另取50g碳酸钙放入锥形瓶中,利用上述装置,重复 I中①~④的操作,称量D瓶内物质增加的质量是22g.
【实验评价】
(1)A瓶中的NaOH溶液起到吸收空气中二氧化碳的作用.若A瓶中无NaOH溶液,D瓶中的质量将增大(填“增大”、“不变”或“减小”),D瓶中发生反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.C瓶中浓硫酸的作用是除去二氧化碳气体中的水蒸气.
(2)在实验I与II中,小花、小红运用了化学实验中的对比试验方法.
(3)一般情况下,两种不同金属形成的碳酸盐与足量盐酸反应时,若两种金属的化合价相同、两种盐的质量相同,则相对分子质量小者放出的气体多.分析实验I与II可知,水垢中一定含有MgCO3(填化学式),理由是50g碳酸钙与盐酸反应放出二氧化碳22g,而50g水垢与盐酸反应实际生成二氧化碳的质量是24g,大于22g,所以水垢中一定含有碳酸镁.
(4)以上实验不能(填“能够”或“不能”) 检测出水垢中是否含有Mg(OH)2.
小花和小红同学非常善于进行实验探究,他们发现长期使用的热水壶底部有一层水垢,小花想这层水垢的主要成分是什么?围绕这个问题,他们展开了探究,请你也参入到他们的学习过程,并协助完成相关任务.
【提出问题】热水壶底部水垢的主要成分是什么?
【查阅资料】通过查阅资料知道,天然水和水垢所含的物质及其溶解性如表:
| 物质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(0H)2 | Mg(0H)2 | CaCO3 | MgCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |
【设计方案,进行实验】
(1)小花在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,静置.取上层清液滴入Na2CO3溶液,如果没有白色沉淀生成,说明水垢中不含有Ca(0H)2(填化学式).
(2)欲证明水垢中含有碳酸盐的实验方法是取少量水垢于试管中,向试管中加入稀盐酸,有气泡产生,把生成的气体通入澄清石灰水中,石灰水变浑浊.
(3)为了进一步确定水垢中含有碳酸盐的成分,他们设计了下列实验装置.

Ⅰ.小花和小红的主要实验步骤如下:
①按如图1所示组装仪器,将50g水垢试样放入锥形瓶中,逐滴加入足量稀盐酸.
②待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气.
③称量D瓶内物质增加的质量.
④重复②和③的操作,直至D瓶内物质的质量不变.
经过上述实验,他们测量滴加稀盐酸的体积与D瓶内物质增加质量的关系如图2曲线所示.
Ⅱ.小花和小红另取50g碳酸钙放入锥形瓶中,利用上述装置,重复 I中①~④的操作,称量D瓶内物质增加的质量是22g.
【实验评价】
(1)A瓶中的NaOH溶液起到吸收空气中二氧化碳的作用.若A瓶中无NaOH溶液,D瓶中的质量将增大(填“增大”、“不变”或“减小”),D瓶中发生反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.C瓶中浓硫酸的作用是除去二氧化碳气体中的水蒸气.
(2)在实验I与II中,小花、小红运用了化学实验中的对比试验方法.
(3)一般情况下,两种不同金属形成的碳酸盐与足量盐酸反应时,若两种金属的化合价相同、两种盐的质量相同,则相对分子质量小者放出的气体多.分析实验I与II可知,水垢中一定含有MgCO3(填化学式),理由是50g碳酸钙与盐酸反应放出二氧化碳22g,而50g水垢与盐酸反应实际生成二氧化碳的质量是24g,大于22g,所以水垢中一定含有碳酸镁.
(4)以上实验不能(填“能够”或“不能”) 检测出水垢中是否含有Mg(OH)2.
12.物质的构成与分类
(1)世界上的物质都是由元素组成的,而物质又是由原子、分子和离子等基本粒子构成的.在宏观物质--微观构成--符号之间建立联系,是化学学科特有的思维方式.现有氢、碳、氧、钠、铜、氯六种元素,请按要求填写表中的空白:
(2)分类法是科学研究的一种重要方法,分类标准有多种,化学上可从不同的角度对物质进行分类.请按要求完成下列问题:
Ⅰ.下列两组物质中均有一种物质所属类别与其它两种不同,请指出你的分类标准,并选出该物质,用化学式表示,说明选择的理由.
①烧碱、硫酸铜、熟石灰:
你的分类标准是根据物质的性质不同;选出的物质是CuSO4,理由是硫酸铜属于盐,其它两种是碱.
②硫酸、氯酸钾、二氧化碳:
你的分类标准是根据物质的组成元素不同;选出的物质是CO2,理由是二氧化碳由2种元素组成,其它两种由3种元素组成.
Ⅱ.以构成物质粒子的种类不同为分类标准,将水、铁、金刚石三种物质进行分类,其中不同类的物质是(用化学式表示)H2O,理由是水是由分子构成的,铁和金刚石是由原子构成的.
(1)世界上的物质都是由元素组成的,而物质又是由原子、分子和离子等基本粒子构成的.在宏观物质--微观构成--符号之间建立联系,是化学学科特有的思维方式.现有氢、碳、氧、钠、铜、氯六种元素,请按要求填写表中的空白:
| 编号 | 组成物质的要求 | 物质的名称 | 物质的化学式 | 构成物质的粒子 (用化学符号表示) |
| 示例 | 一种气体单质 | 氧气 | O2 | O2 |
| ① | 常做导线的一种金属单质 | |||
| ② | 由三种元素组成的 一种可溶性盐 | |||
| ③ | 由三种元素组成的有机物,可作燃料 |
Ⅰ.下列两组物质中均有一种物质所属类别与其它两种不同,请指出你的分类标准,并选出该物质,用化学式表示,说明选择的理由.
①烧碱、硫酸铜、熟石灰:
你的分类标准是根据物质的性质不同;选出的物质是CuSO4,理由是硫酸铜属于盐,其它两种是碱.
②硫酸、氯酸钾、二氧化碳:
你的分类标准是根据物质的组成元素不同;选出的物质是CO2,理由是二氧化碳由2种元素组成,其它两种由3种元素组成.
Ⅱ.以构成物质粒子的种类不同为分类标准,将水、铁、金刚石三种物质进行分类,其中不同类的物质是(用化学式表示)H2O,理由是水是由分子构成的,铁和金刚石是由原子构成的.
11.化学与食品、药品安全
近年来,食品安全已受到了国人的普遍关注.但是一些不法商贩仍然不顾国家法律,置若罔闻,从瘦肉精到染色馒头、毒豆芽、地沟油、药品胶囊,危害食品安全的事件时有发生.请阅读下列信息,回答有关问题:
事件一:2011年4月11日晚,央视曝光“上海华联超市等销售染色馒头”,商家为了降低成本将柠檬黄用在玉米馒头中着色,山梨酸钾用在馒头中防止馒头发霉,甜蜜素用在馒头中代替蔗糖.面对记者的采访,而染色馒头的生产者对自己生产的馒头却说“我不会吃的,打死我都不会吃,饿死我都不会吃”.
事件二:2011年4月17日,沈阳警方端掉一黑豆芽加工点,老板称这种豆芽“旺季每天可售出2000斤”. 经检验这些“毒豆芽”中含有过量的亚硝酸钠、尿素等有害物质,其中尿素超标27倍,长期食用这种豆芽可致癌.
事件三:2012年4月16日国家食品药品监督管理局发出紧急通知,要求对修正药业等9个厂家,13个药用空心胶囊产品暂停销售和使用.经检验这些用工业明胶制成的胶囊中重金属铬含量超过国家标准规定2mg/kg的限量值,其中超标最多的达90多倍.
(1)馒头是我们的主食之一.食用馒头摄入体内的主要营养物质属于糖类,馒头中的主要成分是淀粉,它在人体内不能直接被吸收,而是在淀粉酶和水的作用下,转变成葡萄糖并溶解在血液中,生成的葡萄糖在体内经缓慢氧化放出热量供肌体活动,这一过程的化学反应方程式为C6H12O6+6O2═6CO2+6H2O.
(2)防腐剂山梨酸钾的化学式为C6H7KO2,试回答:
①山梨酸钾中C、H、K、O各元素的质量比为72:7:39:32;
②山梨酸钾中钾元素的质量分数为26.0%(结果保留1位小数).
(3)亚硝酸钠(NaNO2)是一种白色固体,有咸味,外观与氯化钠相似,有毒,过量或长期食用会对人体产生危害.有关氯化钠和亚硝酸钠的部分资料如表:
①根据上表提供的信息,写出亚硝酸钠的两条化学性质:溶液呈弱碱性、不稳定受热易分解.
②测定亚硝酸钠水溶液的pH约为C(填序号).
A.4 B.6.4 C.7.5 D.13
③工业用盐中常混有亚硝酸钠.为检验某食盐中是否含有亚硝酸钠,你的操作方法是取少量食盐于试管中,然后加热,若有刺激性气味的气体产生,就证明食盐中含有亚硝酸钠..
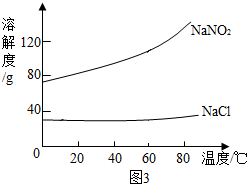
(4)如图3为氯化钠和亚硝酸钠的溶解度曲线,试回答:
①在20℃时,氯化钠饱和溶液中溶质的质量分数小于(填“大于”、“等于”、“小于”)亚硝酸钠的饱和溶液中溶质的质量分数.
②在20℃时,各取氯化钠和亚硝酸钠50g,分别加入到100g水中充分搅拌后,得到的亚硝酸钠溶液属于不饱和(填“饱和”或“不饱和”)溶液.
(5)食用铬含量超标的药品胶囊,会使人中毒的原因是铬是重金属,人体中具有生命活性的物质是蛋白质,当人体摄入重金属铬盐后,蛋白质的结构就会被破坏,生理活性随之消失.
0 164747 164755 164761 164765 164771 164773 164777 164783 164785 164791 164797 164801 164803 164807 164813 164815 164821 164825 164827 164831 164833 164837 164839 164841 164842 164843 164845 164846 164847 164849 164851 164855 164857 164861 164863 164867 164873 164875 164881 164885 164887 164891 164897 164903 164905 164911 164915 164917 164923 164927 164933 164941 211419
近年来,食品安全已受到了国人的普遍关注.但是一些不法商贩仍然不顾国家法律,置若罔闻,从瘦肉精到染色馒头、毒豆芽、地沟油、药品胶囊,危害食品安全的事件时有发生.请阅读下列信息,回答有关问题:

事件一:2011年4月11日晚,央视曝光“上海华联超市等销售染色馒头”,商家为了降低成本将柠檬黄用在玉米馒头中着色,山梨酸钾用在馒头中防止馒头发霉,甜蜜素用在馒头中代替蔗糖.面对记者的采访,而染色馒头的生产者对自己生产的馒头却说“我不会吃的,打死我都不会吃,饿死我都不会吃”.
事件二:2011年4月17日,沈阳警方端掉一黑豆芽加工点,老板称这种豆芽“旺季每天可售出2000斤”. 经检验这些“毒豆芽”中含有过量的亚硝酸钠、尿素等有害物质,其中尿素超标27倍,长期食用这种豆芽可致癌.
事件三:2012年4月16日国家食品药品监督管理局发出紧急通知,要求对修正药业等9个厂家,13个药用空心胶囊产品暂停销售和使用.经检验这些用工业明胶制成的胶囊中重金属铬含量超过国家标准规定2mg/kg的限量值,其中超标最多的达90多倍.
(1)馒头是我们的主食之一.食用馒头摄入体内的主要营养物质属于糖类,馒头中的主要成分是淀粉,它在人体内不能直接被吸收,而是在淀粉酶和水的作用下,转变成葡萄糖并溶解在血液中,生成的葡萄糖在体内经缓慢氧化放出热量供肌体活动,这一过程的化学反应方程式为C6H12O6+6O2═6CO2+6H2O.
(2)防腐剂山梨酸钾的化学式为C6H7KO2,试回答:
①山梨酸钾中C、H、K、O各元素的质量比为72:7:39:32;
②山梨酸钾中钾元素的质量分数为26.0%(结果保留1位小数).
(3)亚硝酸钠(NaNO2)是一种白色固体,有咸味,外观与氯化钠相似,有毒,过量或长期食用会对人体产生危害.有关氯化钠和亚硝酸钠的部分资料如表:
| 物质名称 | 水溶性 | 熔点 | 溶液的酸碱性 | 热稳定性 | 与稀盐酸作用 |
| 亚硝酸钠 | 易溶,在15℃时 溶解度为81.5g | 271℃ | 弱碱性 | 320℃以上会分解 放出刺激性气体 | 放出红棕色气体 |
| 氯化钠 | 易溶,在15℃时 溶解度为35.8g | 801℃ | 中性 | 受热不分解 | 不反应 |
②测定亚硝酸钠水溶液的pH约为C(填序号).
A.4 B.6.4 C.7.5 D.13
③工业用盐中常混有亚硝酸钠.为检验某食盐中是否含有亚硝酸钠,你的操作方法是取少量食盐于试管中,然后加热,若有刺激性气味的气体产生,就证明食盐中含有亚硝酸钠..
(4)如图3为氯化钠和亚硝酸钠的溶解度曲线,试回答:
①在20℃时,氯化钠饱和溶液中溶质的质量分数小于(填“大于”、“等于”、“小于”)亚硝酸钠的饱和溶液中溶质的质量分数.
②在20℃时,各取氯化钠和亚硝酸钠50g,分别加入到100g水中充分搅拌后,得到的亚硝酸钠溶液属于不饱和(填“饱和”或“不饱和”)溶液.
(5)食用铬含量超标的药品胶囊,会使人中毒的原因是铬是重金属,人体中具有生命活性的物质是蛋白质,当人体摄入重金属铬盐后,蛋白质的结构就会被破坏,生理活性随之消失.
