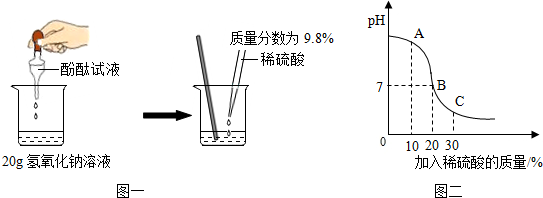
16.下列图示所提供的能量不是由化学变化提供的是( )
| A. |  火力发电 | B. |  冶炼钢铁 | C. |  炸药爆破 | D. |  风力发电 |
10.除去下列物质中的少量杂质(括号内为杂质),所选用的试剂及操作正确的是( )
| 选项 | 物质(杂质) | 选用试剂及操作 |
| A | CaCO3(CaCl2) | 加盐酸,将固体溶解后蒸发结晶 |
| B | KCl溶液(MgCl2) | 加适量NaOH溶液,过滤 |
| C | CO2气体(水蒸气) | 将气体通过装有足量CaO的玻璃管 |
| D | Cu粉(Fe粉) | 加过量稀盐酸,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
9.利用化学实验可以鉴别一些物质.下表中各组物质的鉴别方法能将本组待鉴别物质都区分出来的是( )
0 164385 164393 164399 164403 164409 164411 164415 164421 164423 164429 164435 164439 164441 164445 164451 164453 164459 164463 164465 164469 164471 164475 164477 164479 164480 164481 164483 164484 164485 164487 164489 164493 164495 164499 164501 164505 164511 164513 164519 164523 164525 164529 164535 164541 164543 164549 164553 164555 164561 164565 164571 164579 211419
| 选项 | 待鉴别的物质 | 鉴别方法 |
| A | 氢气、甲烷 | 点燃,用干冷烧杯罩住火焰,观察内壁有无水雾 |
| B | N2、O2、CO2、空气 | 用燃着的木条检验,观察木条燃烧情况 |
| C | 棉纤维、羊毛纤维、涤纶 | 灼烧,闻燃烧产生的气味,观察燃烧情况 |
| D | 氯化钾、硫酸钾、磷矿粉 | 看外观,再加水,观察是否溶于水 |
| A. | A | B. | B | C. | C | D. | D |
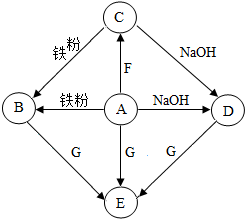 A-G是初中化学常见物质.其中A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.
A-G是初中化学常见物质.其中A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.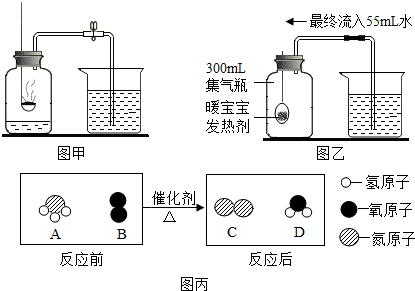
 请回答以下问题.
请回答以下问题.