16. 糕点包装袋中常见的保鲜剂组成为还原性铁粉、氯化钠、炭粉等.某化学兴趣小组为了探究铁粉的作用,设计了如下实验:
糕点包装袋中常见的保鲜剂组成为还原性铁粉、氯化钠、炭粉等.某化学兴趣小组为了探究铁粉的作用,设计了如下实验:
【实验装置】
【步骤及现象】
①连接好实验装置,并检查装置气密性.
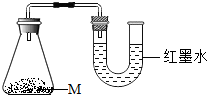
②按图装好药品M,经过一段时间(各组实验时间相等)后观察现象.
实验现象如下:
(1)实验Ⅰ中U型管左、右两端液面相平,水明锥形瓶内气压等于(填“大于”、“小于”或“等于”)外界大气压.
(2)实验Ⅱ说明锥形瓶内的气体分子数减少了(填“增多了”、“减少了”或“未改变”),可能的原因是铁粉消耗了锥形瓶中的氧气.其他条件不变,放置一段时间后,实验Ⅱ中U型管两端的液面能否恢复至原来的相平状态?否(填“能”或“否”)
(3)一段时间后,取出锥形瓶中物质,发现实验Ⅱ中铁粉表面有红褐色物质,其他实验中M固体变化不明显,经进一步分析,该红色物质是Fe2O3•nH2O.生成该物质的化学方程式为4Fe+3O2+2nH2O=2Fe2O3•nH2O.
(4)由实验可得出还原性铁粉在食品袋中的作用是除去氧气和水.
【交流与反思】
(5)①有同学根据上述实验探究受到启发:他认为可以用生石灰替代上述保鲜剂,你是否同意他的观点并简述理由:不同意,生石灰只能吸收水蒸气,不能除去食品袋中的氧气,食品会被氧化变质.
②你认为本实验成功的关键是装置气密性良好.
 糕点包装袋中常见的保鲜剂组成为还原性铁粉、氯化钠、炭粉等.某化学兴趣小组为了探究铁粉的作用,设计了如下实验:
糕点包装袋中常见的保鲜剂组成为还原性铁粉、氯化钠、炭粉等.某化学兴趣小组为了探究铁粉的作用,设计了如下实验:【实验装置】
【步骤及现象】
①连接好实验装置,并检查装置气密性.
②按图装好药品M,经过一段时间(各组实验时间相等)后观察现象.
实验现象如下:
| 实验 | M成分 | 实验现象 |
| Ⅰ | 干燥的铁粉、炭粉和氯化钠的混合物 | U型管左、右两端液面相平 |
| Ⅱ | 用氯化钠的溶液浸泡的铁粉、炭粉 | U型管左端液面明显高于右端 |
| Ⅲ | 用水浸泡的铁粉和炭粉 | U型管左、右两端液面基本相平 |
| Ⅳ | 用氯化钠溶液浸泡的铁粉 | U型管左端液面略高于右端 |
(2)实验Ⅱ说明锥形瓶内的气体分子数减少了(填“增多了”、“减少了”或“未改变”),可能的原因是铁粉消耗了锥形瓶中的氧气.其他条件不变,放置一段时间后,实验Ⅱ中U型管两端的液面能否恢复至原来的相平状态?否(填“能”或“否”)
(3)一段时间后,取出锥形瓶中物质,发现实验Ⅱ中铁粉表面有红褐色物质,其他实验中M固体变化不明显,经进一步分析,该红色物质是Fe2O3•nH2O.生成该物质的化学方程式为4Fe+3O2+2nH2O=2Fe2O3•nH2O.
(4)由实验可得出还原性铁粉在食品袋中的作用是除去氧气和水.
【交流与反思】
(5)①有同学根据上述实验探究受到启发:他认为可以用生石灰替代上述保鲜剂,你是否同意他的观点并简述理由:不同意,生石灰只能吸收水蒸气,不能除去食品袋中的氧气,食品会被氧化变质.
②你认为本实验成功的关键是装置气密性良好.
15.某研究性学习小组在验证“碱使酚酞试液变红”的实验时,发现一个意外现象:将酚酞试液滴入某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失.
【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;
乙同学:可能是NaOH溶液与空气中的CO2发生了反应;
丙同学:可能与氢氧化钠溶液的浓度大小有关;
【设计实验】三位同学分别设计实验验证自己的猜想:
(1)甲同学设计了如下实验,请你填写下表.
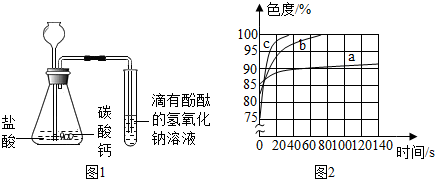
(2)乙同学设计如图一装置进行实验,一段时间后,试管中溶液的红色褪去,于是认定自己的猜想正确.写出CO2与NaOH溶液反应的化学方程式:2NaOH+CO2=Na2CO3+H2O.甲同学认为乙同学的实验不够严谨,理由是:若制取的二氧化碳气体中混有氯化氢气体,试管中溶液的红色也能褪去.
(3)丙同学使用了色度传感器测溶液的颜色.他在a、b、c三个比色皿中分别加入等量5%、10%、20%
的NaOH溶液,然后各滴加2滴酚酞试液.溶液颜色的变化曲线如图[说明:溶液无色 时色度值(透过率)为100%].请你观察图二写出规律性结论:氢氧化钠溶液的浓度越大,酚酞试液变红后褪色越快;氢氧化钠溶液的浓度越小,色度值越大..

【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;
乙同学:可能是NaOH溶液与空气中的CO2发生了反应;
丙同学:可能与氢氧化钠溶液的浓度大小有关;
【设计实验】三位同学分别设计实验验证自己的猜想:
(1)甲同学设计了如下实验,请你填写下表.
| 实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
| ①将NaOH溶液加热煮沸 | ①除去溶液中的氧气 | 溶液变红,过一会儿红色消失 | 甲同学猜想不正确(填“正确”或不正确”) |
| ②向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | ②隔绝氧气 |
(3)丙同学使用了色度传感器测溶液的颜色.他在a、b、c三个比色皿中分别加入等量5%、10%、20%
的NaOH溶液,然后各滴加2滴酚酞试液.溶液颜色的变化曲线如图[说明:溶液无色 时色度值(透过率)为100%].请你观察图二写出规律性结论:氢氧化钠溶液的浓度越大,酚酞试液变红后褪色越快;氢氧化钠溶液的浓度越小,色度值越大..
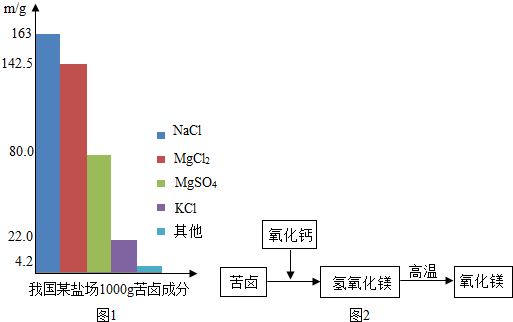
9.沿海某化工厂利用海水中含有的氯化镁、海边的贝壳(主要成分是碳酸钙)制取纯净的氯化镁,生产的大致过程为:原料(海水、贝壳)→氢氧化镁$\stackrel{盐酸}{→}$氯化镁溶液$\stackrel{蒸发}{→}$无水氯化镁,该生产过程中的有关化学反应中,没有涉及的反应类型是( )
0 164383 164391 164397 164401 164407 164409 164413 164419 164421 164427 164433 164437 164439 164443 164449 164451 164457 164461 164463 164467 164469 164473 164475 164477 164478 164479 164481 164482 164483 164485 164487 164491 164493 164497 164499 164503 164509 164511 164517 164521 164523 164527 164533 164539 164541 164547 164551 164553 164559 164563 164569 164577 211419
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |