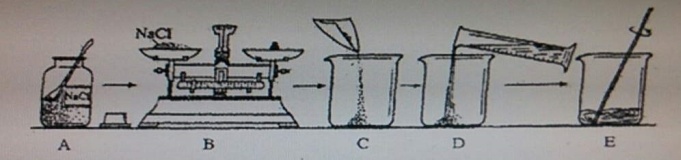
2.某混合气体可能含有CO,H2,CO2,HCl,N2中的以一种或几种,依次进行以下实验(假设每步反应都完全进行).
①通过一定量澄清石灰水不变浑浊;
②通过CaCl2溶液不变浑浊;
③通过浓硫酸,再通过灼热的CuO时,固体变成红色;
④通过澄清石灰水变浑浊;
⑤通过无水硫酸铜变蓝.
下列对原混合气体的判断正确的是( )
①通过一定量澄清石灰水不变浑浊;
②通过CaCl2溶液不变浑浊;
③通过浓硫酸,再通过灼热的CuO时,固体变成红色;
④通过澄清石灰水变浑浊;
⑤通过无水硫酸铜变蓝.
下列对原混合气体的判断正确的是( )
| A. | 可能同时含有CO2和HCl,一定含有一氧化碳,可能含有氢气 | |
| B. | 一定无CO2,一定有CO,可能有H2 | |
| C. | 同时含有CO2和CO,不一定有H2 | |
| D. | 一定无CO2,一定有CO和H2 |
19.比较推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 烧碱属于碱,故纯碱也属于碱 | |
| B. | 氢氧化铝可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多 | |
| C. | 由金属离子和酸根离子组成的化合物是盐,故盐中一定含有金属离子 | |
| D. | 酸雨的pH小于7,但pH小于7的雨水不一定是酸雨 |
18.乙烷是重要的燃料和化工原料.下列有关乙烷叙述错误的是( )
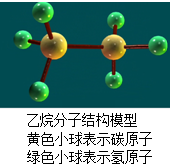

| A. | 乙烷由碳、氢元素组成 | B. | 每个乙烷分子中有8个原子 | ||
| C. | 乙烷中碳、氢元素的质量比为1:3 | D. | 乙烷的相对分子质量为30 |
17.某同学对CaH2的制备和性质进行探究.
【阅读资料】①用H2与钙加热制得CaH2
②钙遇水立即发生剧烈反应生成一种碱和一种气体
③CaH2要密封保存,遇水反应也生成一种碱和一种气体
【CaH2的制备】设计的制取装置如图所示.
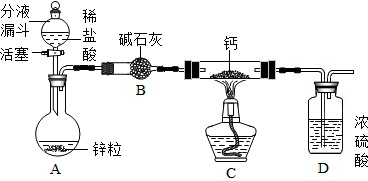
(1)装置B的作用是吸收水蒸气;装置D的作用是防止空气中的水蒸气与钙反应;
(2)制备CaH2实验结束后,取少量产物,小心加入水中,观察有气泡产生,在溶液中滴入石蕊试液后显蓝色.该同学据此判断:实验中确有氢化钙生成,其他同学提出结论不一定正确,原因是也可能是钙和水反应.
【CaH2的性质探究】
取少量上述制得的CaH2 样品加入到足量的碳酸钠溶液中,产生大量气泡,过滤,得到滤渣和滤液.经检验滤渣的成分是碳酸钙.该同学进行了如下的探究.
(3)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象.则该气体为H2 (写化学式).
(4)对滤液中溶质的成分做出如下猜测并进行实验:
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2=CaCO3+2NaOH
【实验验证】
【定量分析】
取制得的CaH2样品1g(假设不含其他杂质)加入到足量的Na2CO3溶液中,充分反应后,过滤、洗涤、干燥称得CaCO3质量为2g,则该样品中CaH2的质量分数为84%.
0 164133 164141 164147 164151 164157 164159 164163 164169 164171 164177 164183 164187 164189 164193 164199 164201 164207 164211 164213 164217 164219 164223 164225 164227 164228 164229 164231 164232 164233 164235 164237 164241 164243 164247 164249 164253 164259 164261 164267 164271 164273 164277 164283 164289 164291 164297 164301 164303 164309 164313 164319 164327 211419
【阅读资料】①用H2与钙加热制得CaH2
②钙遇水立即发生剧烈反应生成一种碱和一种气体
③CaH2要密封保存,遇水反应也生成一种碱和一种气体
【CaH2的制备】设计的制取装置如图所示.

(1)装置B的作用是吸收水蒸气;装置D的作用是防止空气中的水蒸气与钙反应;
(2)制备CaH2实验结束后,取少量产物,小心加入水中,观察有气泡产生,在溶液中滴入石蕊试液后显蓝色.该同学据此判断:实验中确有氢化钙生成,其他同学提出结论不一定正确,原因是也可能是钙和水反应.
【CaH2的性质探究】
取少量上述制得的CaH2 样品加入到足量的碳酸钠溶液中,产生大量气泡,过滤,得到滤渣和滤液.经检验滤渣的成分是碳酸钙.该同学进行了如下的探究.
(3)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象.则该气体为H2 (写化学式).
(4)对滤液中溶质的成分做出如下猜测并进行实验:
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2=CaCO3+2NaOH
【实验验证】
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量 Na2CO3溶液 | 无明显现象 | 猜想二不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | 过一会儿有气泡产生 | 猜想三成立 |
取制得的CaH2样品1g(假设不含其他杂质)加入到足量的Na2CO3溶液中,充分反应后,过滤、洗涤、干燥称得CaCO3质量为2g,则该样品中CaH2的质量分数为84%.