6.关于溶液的下列说法正确的是( )
| A. | 任何溶液都只能含有一种溶质 | |
| B. | 将硝酸钾固体溶于水时加热,既可以使硝酸钾溶得更快,又能使其溶得更多 | |
| C. | 向水中加入少量蔗糖固体可增强水的导电性 | |
| D. | 一定温度下,任何物质都可以无限制溶解在一定量的水中 |
5.下列实验现象描述中不正确的是( )
| A. | 在无色的碘化钾溶液中滴加淀粉溶液,溶液变蓝 | |
| B. | 加热铜绿,固体由绿色变成黑色,生成一种能使澄清石灰水变浑浊的气体 | |
| C. | 硫磺在氧气中燃烧,发出明亮的蓝紫色火焰,生成一种刺激性气味的气体 | |
| D. | 铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成一种黑色固体 |
4.下列实验操作正确的是( )
| A. | 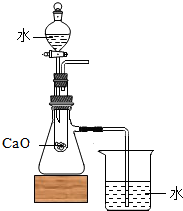 验证反应放热 | B. | 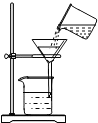 过滤 | ||
| C. | 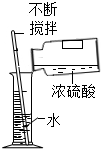 稀释浓硫酸 | D. | 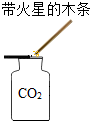 验满 |
3.下列标志属于中国节能标志的是( )
| A. |  | B. |  | C. |  | D. |  |
2.下列化学用语中的数字“2”表示分子个数的是( )
| A. | 2H2 | B. | H2O | C. | 2H | D. | 2H+ |
1.地壳中含量最多的金属元素所对应的氧化物是( )
| A. | SiO2 | B. | CaO | C. | Al2O3 | D. | Fe2O3 |
20.下列物质属于纯净物的是( )
| A. | 医用酒精 | B. | 铁水 | C. | 洁净的空气 | D. | 稀有气体 |
17.如图是某品牌牙膏的部分成分表,学习小组对其中的碳酸氢钠和碳酸钠过氧化物产生了兴趣,对该牙膏展开探究.(已知牙膏中不含其它碳酸盐,不考虑牙膏中其它物质对本实验的影响且每次反应均认为是完全反应.
【实验目的】
(1)验证该牙膏中含有碳酸氢钠和碳酸钠过氧化物.
(2)测定牙膏中的碳酸氢钠的质量分数.
【资料卡片】
(1)碳酸钠过氧化物学名过氧碳酸钠,化学式:Na2CO4,白色晶体.在水中能生成碳酸钠和过氧化氢.能与盐酸反应,方程式为:2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O.
(2)常温下,氧气和二氧化碳密度可分别用ρO2、ρCO2表示.
【实验原理】
(1)通过是否有氧气生成来检测过氧碳酸钠.
(2)取样品加入足量稀盐酸后分别测出二氧化碳质量M1和氧气的质量M2,M1和M2关系满足$\frac{{M}_{1}}{{M}_{2}}>\frac{11}{4}$即证明含有碳酸氢钠.
(3)通过碳酸氢钠生成的二氧化碳的质量计算碳酸氢钠的质量.
【实验探究】
(1)先取部分样品于试管中,再依次加入二氧化锰和水,将带火星的木条伸入试管,木条复燃.
(2)如图所示连接好装置ABCD,检查装置气密性(打开K2,向D装置中加水,调节两边液面相平,关闭K2,改变水准管高度,如D两边有稳定液面高度差,则气密性良好).
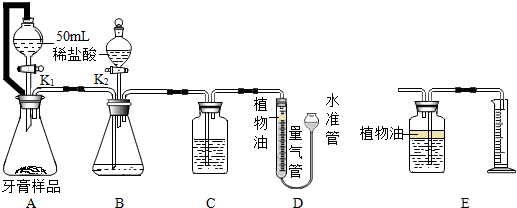
(3)在分液漏斗中均装入50mL足量的稀盐酸,称取质量为M牙膏样品放入A锥形瓶,B、C容器中分别放入氢氧化钠溶液和浓硫酸试剂.D量气管液面调节至“0”刻读处.(以下实验中始终保持D装置两边液面相平)
(4)打开活塞K1,待盐酸全部滴入锥形瓶后关闭K1.等装置A中不再产生气泡时,读数为V1.
(5)打开活塞K2,待盐酸全部滴入锥形瓶后关闭K2.等装置B中不再产生气泡时,读数为V2.
【数据处理】
(1)产生二氧化碳与氧气的质量比为(可用字母表示):(V2-V1-50mL)•ρCO2/V1•ρO2.
(2)如用装置E代替装置D,收集气体的量将偏小.(填“偏大”或“偏小”或“不变”).
【实验结论】
(1)该牙膏中含有碳酸氢钠和碳酸钠过氧化物.
(2)由具体数据计算所得牙膏样品中碳酸氢钠的质量分数约为65%.
0 163813 163821 163827 163831 163837 163839 163843 163849 163851 163857 163863 163867 163869 163873 163879 163881 163887 163891 163893 163897 163899 163903 163905 163907 163908 163909 163911 163912 163913 163915 163917 163921 163923 163927 163929 163933 163939 163941 163947 163951 163953 163957 163963 163969 163971 163977 163981 163983 163989 163993 163999 164007 211419
| 品名 | XXX亮白洁净牙膏 |
| 成分 | 碳酸氢钠、PEG-8\PEG-116共聚物、碳酸钠过氧化物 |
(1)验证该牙膏中含有碳酸氢钠和碳酸钠过氧化物.
(2)测定牙膏中的碳酸氢钠的质量分数.
【资料卡片】
(1)碳酸钠过氧化物学名过氧碳酸钠,化学式:Na2CO4,白色晶体.在水中能生成碳酸钠和过氧化氢.能与盐酸反应,方程式为:2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O.
(2)常温下,氧气和二氧化碳密度可分别用ρO2、ρCO2表示.
【实验原理】
(1)通过是否有氧气生成来检测过氧碳酸钠.
(2)取样品加入足量稀盐酸后分别测出二氧化碳质量M1和氧气的质量M2,M1和M2关系满足$\frac{{M}_{1}}{{M}_{2}}>\frac{11}{4}$即证明含有碳酸氢钠.
(3)通过碳酸氢钠生成的二氧化碳的质量计算碳酸氢钠的质量.
【实验探究】
(1)先取部分样品于试管中,再依次加入二氧化锰和水,将带火星的木条伸入试管,木条复燃.
(2)如图所示连接好装置ABCD,检查装置气密性(打开K2,向D装置中加水,调节两边液面相平,关闭K2,改变水准管高度,如D两边有稳定液面高度差,则气密性良好).

(3)在分液漏斗中均装入50mL足量的稀盐酸,称取质量为M牙膏样品放入A锥形瓶,B、C容器中分别放入氢氧化钠溶液和浓硫酸试剂.D量气管液面调节至“0”刻读处.(以下实验中始终保持D装置两边液面相平)
(4)打开活塞K1,待盐酸全部滴入锥形瓶后关闭K1.等装置A中不再产生气泡时,读数为V1.
(5)打开活塞K2,待盐酸全部滴入锥形瓶后关闭K2.等装置B中不再产生气泡时,读数为V2.
【数据处理】
(1)产生二氧化碳与氧气的质量比为(可用字母表示):(V2-V1-50mL)•ρCO2/V1•ρO2.
(2)如用装置E代替装置D,收集气体的量将偏小.(填“偏大”或“偏小”或“不变”).
【实验结论】
(1)该牙膏中含有碳酸氢钠和碳酸钠过氧化物.
(2)由具体数据计算所得牙膏样品中碳酸氢钠的质量分数约为65%.
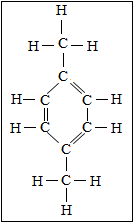 2015年4月6日位于福建漳州的PX项目突然起火爆炸引起世人关注.PX学名对二甲苯,其组成和结构如图所示.PX来自石油制品,主要用于制取生产涤纶纤维的原料聚酯树脂.
2015年4月6日位于福建漳州的PX项目突然起火爆炸引起世人关注.PX学名对二甲苯,其组成和结构如图所示.PX来自石油制品,主要用于制取生产涤纶纤维的原料聚酯树脂.