18.下列四个图象分别表示对应的四种操作过程,其中表示正确的图象是( )
| A. | 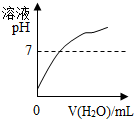 向pH=2的酸溶液中不断加水 | |
| B. | 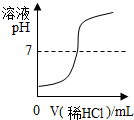 向NaOH溶液中逐滴加入稀盐酸 | |
| C. | 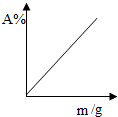 向一定量的水中持续加入食盐(m表示食盐的质量,A%表示溶质分数) | |
| D. | 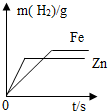 等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量随反应时间t的变化 |
17.向氧化铜和铁粉的混合物中加入一定量的稀硫酸,微热,充分反应后过滤.以下判断错误的是( )
| A. | 滤液中一定含有硫酸亚铁 | B. | 滤液中一定含有硫酸铜 | ||
| C. | 滤纸上可能含有铜 | D. | 滤纸上可能含有氧化铜 |
16.梳理化学知识是学习化学的一个主要方法,下列正确的一组是( )
| A.性质与用途 | B.保护环境 |
| 利用熟石灰的碱性改良酸性土壤 利用一氧化碳的还原性冶炼金属 利用氧化铝薄膜的致密性防止铝被腐蚀 | 使用无磷洗衣粉可减少水污染 不使用一次性塑料袋可减少白色污染 化石燃料不充分燃烧不会污染空气 |
| C.安全常识 | D.营养物质 |
| 进入地窖要先做灯火实验 面粉加工厂要严禁明火 炒菜时,食用油着火要立即用水浇灭 | 缺钙易患坏血病 蛋白质由多种氨基酸构成 糖类和油脂可以提供能量 |
| A. | A | B. | B | C. | C | D. | D |
15.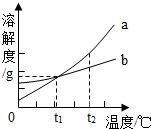 如图是a、b两种固体物质的溶解度曲线图,下列说法中错误的是( )
如图是a、b两种固体物质的溶解度曲线图,下列说法中错误的是( )
 如图是a、b两种固体物质的溶解度曲线图,下列说法中错误的是( )
如图是a、b两种固体物质的溶解度曲线图,下列说法中错误的是( )| A. | a的溶解度受温度变化的影响比b的大 | |
| B. | t2℃时,a物质的饱和溶液浓度大于b | |
| C. | t1℃时,a、b物质饱和溶液中含溶质的质量相等 | |
| D. | t1℃至t2℃之间b的曲线以下区域为a、b两物质的不饱和溶液 |
14.下列生产、生活现象的解释正确的是( )
| A. | 铝锭难被压缩,因为铝原子间没有间隙 | |
| B. | 若家中燃气泄漏,应立即打开排气扇或抽油烟机 | |
| C. | pH大于5.6的雨水为酸雨,能使紫色石蕊溶液变红 | |
| D. | 生活中为了降低水的硬度往往采用加热煮沸 |
13.硝酸铵(NH4NO3)是一种常见的氮肥,下列关于硝酸铵说法正确的是( )
| A. | 共含4种元素 | B. | 氮元素化合价是+1价 | ||
| C. | 氮、氢、氧原子个数比是2:4:3 | D. | 氮肥硝酸铵能与碱性物质滥用 |
12.下列叙述中一定化学变化的是( )
| A. | 干冰升华 | B. | 粮食酿酒 | C. | 活性炭净水 | D. | 氮气作保护气 |
11.一种名为“污渍爆炸盐”的洗涤产品能高效去除衣物上的顽固污渍,是当前使用最为广泛的洗涤助剂之一.某校化学兴趣小组的同学在老师的指导下对该产品开展了以下探究活动.
【查阅资料】
“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4,相对分子质量为122),它是一种白色粉末,易溶于水,且能与水反应,生成一种碳酸盐和一种强氧化性的物质.
【实验探究一】过碳酸钠的性质
为探究过碳酸钠的性质,同学们设计了以下实验,请按要求完成表格内容:
【实验探究二】过碳酸钠的含量测定
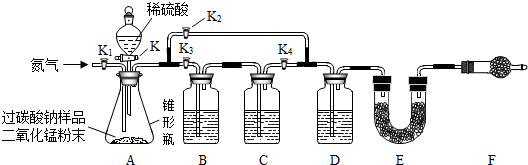
同学们经讨论设计了如图所示的实验装置.图中装置B盛装氢氧化钠溶液,C盛装澄清石灰水,D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气).
【实验讨论】
(1)①称量装置E的质量;②组装好装置,检查气密性,装入药品;③关闭活塞K,打开活塞K1,通入氮气;④关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气;⑤依次关闭活塞K1、K3、K4,打开活塞K K2、,直到反应不再进行;⑥再次称量装置E的质量.
以上实验步骤的正确顺序是D;
A.①②③④⑤⑥B.②①④⑤③⑥C.①②④⑤③⑥D.②④①⑤③⑥
(2)关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气排出装置中原有的空气,此时装置B的作用是除去原有空气中的二氧化碳,防止空气中的二氧化碳进入E装置;
(3)反应完全后关闭活塞K,打开活塞K1,通入氮气的目的是将装置中残留的二氧化碳排出,被E装置充分吸收;
(4)同学们称取6.63g含碳酸钠杂质的过碳酸钠样品(不含其他杂质)进行实验,根据实验后E装置增重2.42g,求该样品中过碳酸钠的含量(写出计算过程,结果保留小数点后一位).
(5)装置F的作用是防止空气中的二氧化碳和水蒸气进入E装置,干扰实验,若不连接装置F,测定的过碳酸钠含量会偏低(填“偏高”或“偏低”).
0 163545 163553 163559 163563 163569 163571 163575 163581 163583 163589 163595 163599 163601 163605 163611 163613 163619 163623 163625 163629 163631 163635 163637 163639 163640 163641 163643 163644 163645 163647 163649 163653 163655 163659 163661 163665 163671 163673 163679 163683 163685 163689 163695 163701 163703 163709 163713 163715 163721 163725 163731 163739 211419
【查阅资料】
“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4,相对分子质量为122),它是一种白色粉末,易溶于水,且能与水反应,生成一种碳酸盐和一种强氧化性的物质.
【实验探究一】过碳酸钠的性质
为探究过碳酸钠的性质,同学们设计了以下实验,请按要求完成表格内容:
| 序号 | 实验步骤 | 实验现象 | 实验分步结论(或解释) |
| ① | 向盛有过碳酸钠固体的试管中加入适量水 | 固体溶解 | 过碳酸钠易溶于水, 能与水发生反应. |
| ② | 向序号①的所得溶液中加入适量的二氧化锰粉末 | 有大量气泡 产生 | |
| ③ | 将带火星的木条置于试管口 | 木条复燃 | 序号②试管中产生的气体是O2; 过碳酸钠溶于水能生成过氧化氢. |
| ④ | 取序号③试管中的上层清液加入氯化钙溶液 | 产生白色 沉淀 | 反应的化学方程式Na2CO3+CaCl2═CaCO3↓+2NaCl. |
| 小结 | 过碳酸钠与水反应的化学方程式是Na2CO4+H2O═Na2CO3+H2O2. | ||
同学们经讨论设计了如图所示的实验装置.图中装置B盛装氢氧化钠溶液,C盛装澄清石灰水,D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气).

【实验讨论】
(1)①称量装置E的质量;②组装好装置,检查气密性,装入药品;③关闭活塞K,打开活塞K1,通入氮气;④关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气;⑤依次关闭活塞K1、K3、K4,打开活塞K K2、,直到反应不再进行;⑥再次称量装置E的质量.
以上实验步骤的正确顺序是D;
A.①②③④⑤⑥B.②①④⑤③⑥C.①②④⑤③⑥D.②④①⑤③⑥
(2)关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气排出装置中原有的空气,此时装置B的作用是除去原有空气中的二氧化碳,防止空气中的二氧化碳进入E装置;
(3)反应完全后关闭活塞K,打开活塞K1,通入氮气的目的是将装置中残留的二氧化碳排出,被E装置充分吸收;
(4)同学们称取6.63g含碳酸钠杂质的过碳酸钠样品(不含其他杂质)进行实验,根据实验后E装置增重2.42g,求该样品中过碳酸钠的含量(写出计算过程,结果保留小数点后一位).
(5)装置F的作用是防止空气中的二氧化碳和水蒸气进入E装置,干扰实验,若不连接装置F,测定的过碳酸钠含量会偏低(填“偏高”或“偏低”).
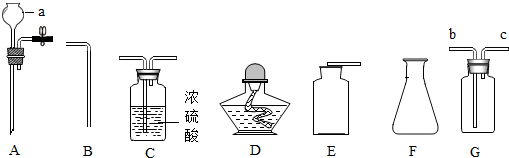
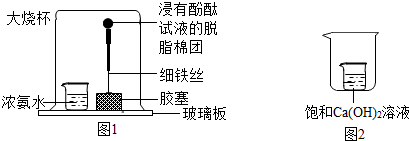
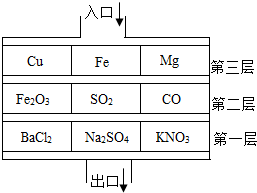 如图所示,若将稀硫酸比作初三学生在“应急演练”中,要从楼顶入口处由上至下疏散到出口处,各层都有三道门(空白处为通道),稀硫酸要在每层中打开一道门(即能与稀硫酸反应的物质)才能到达出口处,请根据图示回答以下问题.
如图所示,若将稀硫酸比作初三学生在“应急演练”中,要从楼顶入口处由上至下疏散到出口处,各层都有三道门(空白处为通道),稀硫酸要在每层中打开一道门(即能与稀硫酸反应的物质)才能到达出口处,请根据图示回答以下问题.