1.“用双氧水和二氧化锰制氧气”的反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.某同学做了该实验后,展开了下列思考与探究:
(1)催化剂MnO2的用量对反应速率有没有影响呢?他做了这样一组实验:每次均用30mL10%的H202溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
请分析表中数据回答:MnO2的用量对反应速率的影响有影响,在一定范围内,MnO2的用量越大,反应越快.
(2)H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取5mL30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验.记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
请分析表中数据回答:H2O2溶液的溶质质量分数对反应速率的影响有影响,其他条件相同时,H2O2溶液的溶质质量分数越大,反应越快.
(3)还有哪些因素可能影响该反应的速率呢?请说出你的一个猜想:MnO2颗粒大小.
(4)为了让我们的实验结论有说服力,在做对比实验时,对于实验条件的把控,我们一定要注意的原则问题是每次只改变一个实验条件,这种科学研究的方法我们称之为“控制变量法”.
(1)催化剂MnO2的用量对反应速率有没有影响呢?他做了这样一组实验:每次均用30mL10%的H202溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量(克) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间(秒) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
(2)H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取5mL30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验.记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
| MnO2粉末用量/克 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
| 收集到540mL气体时所用时间/秒 | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
| 反应后液体温度/℃ | 24 | 34 | 39 | 56 | 65 | 67 | 69 | 70 |
(3)还有哪些因素可能影响该反应的速率呢?请说出你的一个猜想:MnO2颗粒大小.
(4)为了让我们的实验结论有说服力,在做对比实验时,对于实验条件的把控,我们一定要注意的原则问题是每次只改变一个实验条件,这种科学研究的方法我们称之为“控制变量法”.
18.下列物质燃烧时能产生大量白烟的是( )
| A. | 木炭 | B. | 红磷 | C. | 硫 | D. | 氢气 |
17.下列物质中,属于纯净物的是( )
| A. | 汽水 | B. | 石油 | C. | 生鉄 | D. | 干冰 |
16.下列元素中,因摄入量不足可能导致人体骨质疏松、畸形的是( )
0 163372 163380 163386 163390 163396 163398 163402 163408 163410 163416 163422 163426 163428 163432 163438 163440 163446 163450 163452 163456 163458 163462 163464 163466 163467 163468 163470 163471 163472 163474 163476 163480 163482 163486 163488 163492 163498 163500 163506 163510 163512 163516 163522 163528 163530 163536 163540 163542 163548 163552 163558 163566 211419
| A. | 铁 | B. | 钙 | C. | 碘 | D. | 锌 |

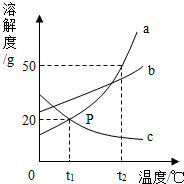 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:(1)P点的含义是t1℃时a与c的溶解度相等.
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:(1)P点的含义是t1℃时a与c的溶解度相等.
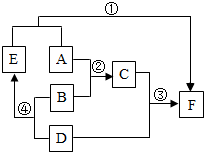 A、D均为黑色固体(D为常见金属)B为稀硫酸,D、E、F均为单质.如图为这些物质的转化关系,其中部分反应物、生成物、反应条件已省略.
A、D均为黑色固体(D为常见金属)B为稀硫酸,D、E、F均为单质.如图为这些物质的转化关系,其中部分反应物、生成物、反应条件已省略. 化学是研究物质的组成、结构,性质及其变化规律的基础自然科学,请回答下列问题:
化学是研究物质的组成、结构,性质及其变化规律的基础自然科学,请回答下列问题: