0 16246 16254 16260 16264 16270 16272 16276 16282 16284 16290 16296 16300 16302 16306 16312 16314 16320 16324 16326 16330 16332 16336 16338 16340 16341 16342 16344 16345 16346 16348 16350 16354 16356 16360 16362 16366 16372 16374 16380 16384 16386 16390 16396 16402 16404 16410 16414 16416 16422 16426 16432 16440 211419
 样品过滤→洗涤→干燥
样品过滤→洗涤→干燥 样品过滤→洗涤→干燥
样品过滤→洗涤→干燥


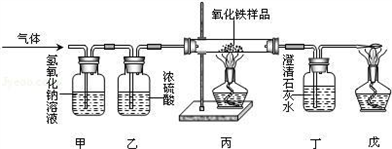
 CO↑+CO2↑+3H2O,该课题小组的同学在实验室分别进行了如下实验请回答下列问题:
CO↑+CO2↑+3H2O,该课题小组的同学在实验室分别进行了如下实验请回答下列问题: