17.Ⅰ.根据下表信息,用规范的化学用语完成表中空格:
Ⅱ.生活离不开化学,处处留心皆学问,请用下列物质的化学式填空:
①氯化钠 ②乙醇 ③碳酸氢钾 ④硝酸钾
(1)适量饮酒可促进血液循环,这里的“酒”是指C2H5OH.
(2)含作物生长所需营养元素,可作复合肥的是KNO3.
| 化学符号 | 2H | 2N2 | Al3+ | 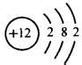 |
| 符号的意义 | 2个氢原子 | 2个氮分子 | 铝离子 | 镁原子的结构示意图 |
①氯化钠 ②乙醇 ③碳酸氢钾 ④硝酸钾
(1)适量饮酒可促进血液循环,这里的“酒”是指C2H5OH.
(2)含作物生长所需营养元素,可作复合肥的是KNO3.
16.纯碱是重要的化工原料.
制备探究:如图是工业生产纯碱的主要流程示意图.

【查阅资料】
①粗盐水中含有杂质MgCl2、CaCl2;
②常温下,NH3极易溶于水,CO2能溶于水,
③NaHCO3加热易分解,Na2CO3加热不易分解.
(1)写出除去粗盐水中MgCl2的化学方程式:MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
(2)在工业生产纯碱工艺流程中,先“氨化”后“碳酸化”的目的是使溶液显碱性,更多的吸收二氧化碳,“碳酸化”时,NaCl、NH3、CO2 和H2O相互作用析出NaHCO3,写出该反应的化学方程式NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl.
(3)煅烧制得纯碱的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
(4)某海洋化工集团生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,在把100g稀盐酸平均分成四份依次放入样品中,每次均充分反应,实验数据记录如下:
请你据此分析计算:
①第一次加入盐酸充分反应后,生成二氧化碳的质量是1.8g.
②该产品中碳酸钠的质量分数是否合格?(写出计算过程,结果精确到0.1%)
制备探究:如图是工业生产纯碱的主要流程示意图.

【查阅资料】
①粗盐水中含有杂质MgCl2、CaCl2;
②常温下,NH3极易溶于水,CO2能溶于水,
③NaHCO3加热易分解,Na2CO3加热不易分解.
(1)写出除去粗盐水中MgCl2的化学方程式:MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
(2)在工业生产纯碱工艺流程中,先“氨化”后“碳酸化”的目的是使溶液显碱性,更多的吸收二氧化碳,“碳酸化”时,NaCl、NH3、CO2 和H2O相互作用析出NaHCO3,写出该反应的化学方程式NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl.
(3)煅烧制得纯碱的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
(4)某海洋化工集团生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,在把100g稀盐酸平均分成四份依次放入样品中,每次均充分反应,实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 盐酸的质量/g | 25 | 25 | 25 | 25 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入盐酸充分反应后,生成二氧化碳的质量是1.8g.
②该产品中碳酸钠的质量分数是否合格?(写出计算过程,结果精确到0.1%)
14.将一定量的苯(C6H6)和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水和一种未知物X.测得反应前后物质的质量如下表:
则m为4.2,X中所含元素有碳、氧,其质量之比为3:4.
| 物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 6.6 | 2.7 | m |
13.下列四个图象的变化趋势,能正确描述对应操作的是( )
| A. | 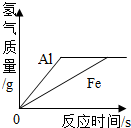 足量的铁片和铝片分别与等质量、等浓度的稀盐酸反应 | |
| B. | 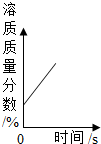 将浓盐酸敝口放置在空气中 | |
| C. | 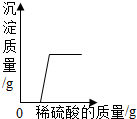 向氢氧化钾和硝酸钡的混合溶液中,逐滴滴加稀硫酸 | |
| D. | 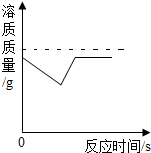 向室温下的饱和石灰水中加入生石灰 |
11.下列反应属于复分解反应的是( )
| A. |  | B. |  | ||
| C. | 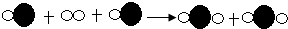 | D. | 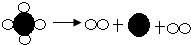 |
10.硫酸镁俗称苦盐、泻盐、硫苦,是一种医疗上治疗便秘、食物中毒的常用药.小明想要通过用稀硫酸和剂发生反应来制取硫酸镁,其中不可行的是( )
| A. | 镁粉 | B. | 氧化镁粉末 | C. | 氯化镁溶液 | D. | 氢氧化镁 |
9.pH=2的溶液与下列溶液混合后,所得溶液的pH可能为7的是( )
| A. | pH=0的溶液 | B. | pH=5的溶液 | C. | pH=7的溶液 | D. | pH=11的溶液 |
8.下列各组物质能发生反应的是( )
0 163289 163297 163303 163307 163313 163315 163319 163325 163327 163333 163339 163343 163345 163349 163355 163357 163363 163367 163369 163373 163375 163379 163381 163383 163384 163385 163387 163388 163389 163391 163393 163397 163399 163403 163405 163409 163415 163417 163423 163427 163429 163433 163439 163445 163447 163453 163457 163459 163465 163469 163475 163483 211419
| A. | 氢氧化钠溶液和氯化钾溶液 | B. | 硝酸银溶液和铜 | ||
| C. | 硝酸钾溶液和氯化钡溶液 | D. | 铁和硝酸锌溶液 |