5.某化工厂为综合利用生产过程中的副产品CaSO4,与相邻化肥厂联合设计了制备(NH4)2SO4的工艺流程(如图所示).在该流程中,沉淀池中发生的主要化学反应为:
CO2+2NH3+CaSO4+H2O=CaCO3↓+(NH4)2SO4
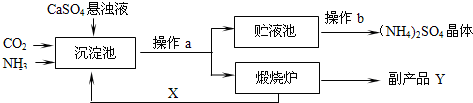
下列说法正确的是( )
CO2+2NH3+CaSO4+H2O=CaCO3↓+(NH4)2SO4

下列说法正确的是( )
| A. | 该工艺中副产品Y为硫酸钙 | |
| B. | 操作b的过程是蒸发、冷却、结晶 | |
| C. | 该工艺中可循环使用的X为二氧化碳 | |
| D. | 实验室中进行操作a时,用到的玻璃仪器除玻璃棒、烧杯外,还需酒精灯 |
4.下列各组物质间通过一步反应就能实现如图转化,则甲、乙、丙依次的组合可能是( )
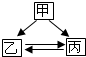

| A. | C、CO2、CO | B. | CuO、CuCl2、Cu(OH)2 | C. | NaOH、NaCl、NaNO3 | D. | H2O、H2O2、O2 |
3.区分下列物质的方法不能达到目的是( )
| A. | 用酚酞试液区分氢氧化钠溶液和碳酸钠溶液 | |
| B. | 用磁铁吸引来区分铁丝和铝丝 | |
| C. | 用灼烧闻气味的方法来区别天然纤维和合成纤维 | |
| D. | 用熟石灰区分NH4Cl和KCl |
2.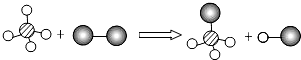 已知某两种物质在光照条件下能发生化学反应,其微观示意图如图(一种小球代表一种原子).则下列说法正确的是( )
已知某两种物质在光照条件下能发生化学反应,其微观示意图如图(一种小球代表一种原子).则下列说法正确的是( )
 已知某两种物质在光照条件下能发生化学反应,其微观示意图如图(一种小球代表一种原子).则下列说法正确的是( )
已知某两种物质在光照条件下能发生化学反应,其微观示意图如图(一种小球代表一种原子).则下列说法正确的是( )| A. | 参加反应的物质均为化合物 | B. | 该反应属于复分解反应 | ||
| C. | 该反应不符合质量守恒定律 | D. | 图示中共有4种分子 |
1.工业上侯氏制碱法制得的纯碱产品中常含有少量的氯化钠杂质,化验员要对每批次的纯碱产品进行检验.在实验室中取27g纯碱样品,平均分成五份依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应后都进行称量,得到的实验数据如表:
(1)第一次加入纯碱样品充分反应后,生成二氧化碳的质量是2.2g.
(2)第三次加入纯碱样品后恰好与100g稀盐酸完全反应,此时共反应纯碱样品16.2g.
(3)计算纯碱样品中碳酸钠的质量分数是多少?(计算结果精确到0.1%)
0 163082 163090 163096 163100 163106 163108 163112 163118 163120 163126 163132 163136 163138 163142 163148 163150 163156 163160 163162 163166 163168 163172 163174 163176 163177 163178 163180 163181 163182 163184 163186 163190 163192 163196 163198 163202 163208 163210 163216 163220 163222 163226 163232 163238 163240 163246 163250 163252 163258 163262 163268 163276 211419
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入纯碱样品的质量/g | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 |
| 电子天平的示数/g | 163.2 | 166.4 | 169.6 | 175 | 180.4 |
(2)第三次加入纯碱样品后恰好与100g稀盐酸完全反应,此时共反应纯碱样品16.2g.
(3)计算纯碱样品中碳酸钠的质量分数是多少?(计算结果精确到0.1%)
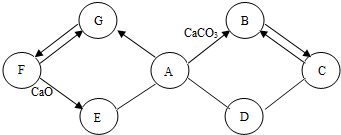
 A、B、C、D、E、F和X都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,它们的转化关系如图所示(部分生成物已省略):
A、B、C、D、E、F和X都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,它们的转化关系如图所示(部分生成物已省略): 当今,染发已经成为一种时尚,年轻人可以随自己的心情和喜好改变头发的颜色,给人眼前一亮的感觉.但是它在给予我们美丽的同时,会对我们的健康造成伤害,染发剂中的染料具有一定的毒性、刺激性和过敏性.例如,染发剂中普遍含有对苯二胺(其化学式为C6H8N2)会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用.因此,科学界告诫我们:慎用染发剂,少染发为好.
当今,染发已经成为一种时尚,年轻人可以随自己的心情和喜好改变头发的颜色,给人眼前一亮的感觉.但是它在给予我们美丽的同时,会对我们的健康造成伤害,染发剂中的染料具有一定的毒性、刺激性和过敏性.例如,染发剂中普遍含有对苯二胺(其化学式为C6H8N2)会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用.因此,科学界告诫我们:慎用染发剂,少染发为好.