9.溶液在生命活动和生产、生活中都起到十分重要的作用.在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
(1)实验a、b、c、d中,有未被溶解的KNO3固体的实验是d(填写实验编号);
(2)实验a、b、c、d所得溶液中,溶质质量分数大小关系为a<b<c=d;
(3)取实验b所得溶液,若使其溶质质量分数变为20%,在不改变温度的情况下,可以采取的操作是加入150g水.
| 实验编号 | a | b | c | d |
| 加入KNO3固体的质量 | 45 | 50 | 55 | 60 |
| 所得溶液的质量 | 95 | 100 | 105 | 105 |
(2)实验a、b、c、d所得溶液中,溶质质量分数大小关系为a<b<c=d;
(3)取实验b所得溶液,若使其溶质质量分数变为20%,在不改变温度的情况下,可以采取的操作是加入150g水.
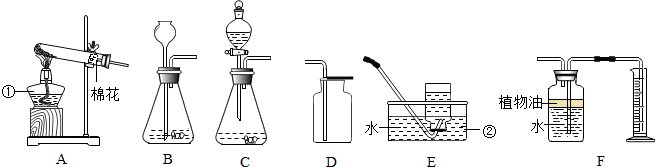
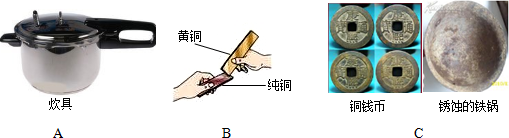
4.活动小组同学通过Al,Fe,Cu三种金属与稀盐酸反应的实验,验证它们的活动性.
【所用药品】
溶质质量分数相同的稀盐酸,大小,形状相同的铝,铁,铜
【实验记录】
【分析与结论】
(1)实验开始时铝表面几乎无气泡产生的原因是铝表面有致密的氧化膜.
(2)铜表面始终无气泡产生的原因是铜不与酸反应(或铜在金属活动性顺序表中排在H之后).
(3)根据一段时间后三种金属与稀盐酸反应的现象,可证明三种金属的活动性由强到弱依次是Al>Fe>Cu
如图是小明配制100g溶质质量分数为12%的NaCl溶液的有关实验操作示意图.
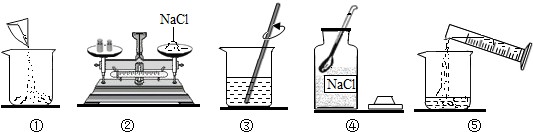
(1)配制过程中使用的四种玻璃仪器,分别是广口瓶、烧杯、玻璃棒、量筒.
(2)请你指出图中一处错误操作,并分析该操作可能造成的后果.②中物码放反了,会导致称取的氯化钠的质量减少.
(3)图②、图③表示的操作步骤分别是称量、溶解.
(4)配制时需称量氯化钠12g,如果氯化钠中含有少量不溶的杂质,溶质的质量分数会偏小(填“偏大”或“偏小”);量取水最好选择③的量筒(填序号①10mL②50mL③100mL).(水的密度为1g/cm3)
0 162981 162989 162995 162999 163005 163007 163011 163017 163019 163025 163031 163035 163037 163041 163047 163049 163055 163059 163061 163065 163067 163071 163073 163075 163076 163077 163079 163080 163081 163083 163085 163089 163091 163095 163097 163101 163107 163109 163115 163119 163121 163125 163131 163137 163139 163145 163149 163151 163157 163161 163167 163175 211419
【所用药品】
溶质质量分数相同的稀盐酸,大小,形状相同的铝,铁,铜
【实验记录】
| Al | Fe | Cu | ||
| 现象 | 开始时 | 几乎无气泡产生 | 产生气泡速率慢 | 无气泡产生 |
| 一段时间后 | 产生气泡速率快 | 产生气泡速率慢 | 无气泡产生 |
(1)实验开始时铝表面几乎无气泡产生的原因是铝表面有致密的氧化膜.
(2)铜表面始终无气泡产生的原因是铜不与酸反应(或铜在金属活动性顺序表中排在H之后).
(3)根据一段时间后三种金属与稀盐酸反应的现象,可证明三种金属的活动性由强到弱依次是Al>Fe>Cu
如图是小明配制100g溶质质量分数为12%的NaCl溶液的有关实验操作示意图.

(1)配制过程中使用的四种玻璃仪器,分别是广口瓶、烧杯、玻璃棒、量筒.
(2)请你指出图中一处错误操作,并分析该操作可能造成的后果.②中物码放反了,会导致称取的氯化钠的质量减少.
(3)图②、图③表示的操作步骤分别是称量、溶解.
(4)配制时需称量氯化钠12g,如果氯化钠中含有少量不溶的杂质,溶质的质量分数会偏小(填“偏大”或“偏小”);量取水最好选择③的量筒(填序号①10mL②50mL③100mL).(水的密度为1g/cm3)
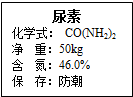 如图是一袋化肥标签的一部分,请回答:
如图是一袋化肥标签的一部分,请回答: