9.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 验证NaCl溶液中混有盐酸 | 取少量溶液,滴加无色酚酞溶液 |
| B | 比较Fe、Cu、Al的金属活动性 | 铁丝浸入CuSO4溶液,铜丝浸入AgNO3溶液 |
| C | 除去铁制品上的铁锈 | 将铁制品长时间浸泡在足量的稀硫酸中 |
| D | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
8.下列物质:①空气、②硫酸、③氧气、④硫酸钠、⑤水、⑥氢氧化钠、⑦天然气、⑧生铁、⑨碳酸钙,对其分类完全正确的一组是( )
| A. | 盐:④⑨ | B. | 酸:②④ | C. | 氧化物:③⑤ | D. | 混合物:①⑥⑦⑧ |
7.化学与生活密切相关,下列说法错误的是( )
| A. | 老人缺钙会发生骨质疏松 | B. | 人体缺铁易患贫血 | ||
| C. | 患肥胖症的病人禁止摄入油脂 | D. | 多食水果蔬菜可预防坏血病 |
6.同学们填写的“毕业生登记表”需要( )
| A. | 碳素笔 | B. | 圆珠笔 | C. | 红墨水笔 | D. | 蓝墨水笔 |
5.下列实验现象描述不正确的是( )
| A. | 红磷在空气中燃烧产生大量白烟 | |
| B. | 硫在氧气中燃烧产生淡蓝色火焰 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射 | |
| D. | 镁在氧气中燃烧,发出耀眼的白光,生成白色固体 |
4.下列物质由离子构成的是( )
| A. | 硫酸铜 | B. | 氧气 | C. | 金刚石 | D. | 汞 |
3.同学们运用对比的学习方法探究碱的性质.
(1)由实验一、二可知,氢氧化钠会吸收空气中的二氧化碳和水,因此要密封保存.
(2)实验三种观察到3个塑料瓶变瘪的程度为A>B>C,对此A瓶与C(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
(3)同学们设计如下两种方案鉴别氢氧化钠和氢氧化钙两种饱和溶液.
(4)某同学发现工业上使用的氢氧化钠固体标签如图所示,于是对其成分进行了探究:

【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】①在华工生产中,原料往往不能完全转化为产品.
②工业上制取NaOH的反应原理是:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体.
③碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
【提出猜想】氢氧化钠中含有的杂质为碳酸钠和氯化钠.
提出上述猜想的理由是原料中的NaCl未完全反应,氢氧化钠与空气中的二氧化碳反应生成碳酸钠.
【进行实验】取固体于试管中,加水溶解并向溶液中加入过滤稀盐酸.
【实验结论】溶液中有明显现象,证明杂质中一定含有碳酸钠.
【反思评价】该同学想进一步证明固体中含有氢氧化钠,实验方案是取少量固体于试管中加水溶解,加入过量的氯化钙溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液,溶液变红,则固体中含有氢氧化钠.
(5)某碳酸钠样品中含有少量氯化钠.现称量11g该样品放入烧杯中,然后加入一定量溶质的质量分数为14.6%的稀盐酸,至恰好完全反应,去除溶液中的水分,最终得到12.1g氯化钠固体.计算:
①碳酸钠样品中碳酸钠的质量;
②反应后所得溶液中溶质的质量分数.(结果精确到0.1%)
0 162721 162729 162735 162739 162745 162747 162751 162757 162759 162765 162771 162775 162777 162781 162787 162789 162795 162799 162801 162805 162807 162811 162813 162815 162816 162817 162819 162820 162821 162823 162825 162829 162831 162835 162837 162841 162847 162849 162855 162859 162861 162865 162871 162877 162879 162885 162889 162891 162897 162901 162907 162915 211419
| 实验一 观察固体表面 | 实验二 向两块固体表面滴加稀盐酸 | 实验三 振荡3个塑料瓶 |
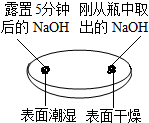 | 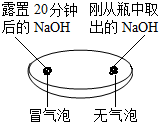 |  |
(2)实验三种观察到3个塑料瓶变瘪的程度为A>B>C,对此A瓶与C(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
(3)同学们设计如下两种方案鉴别氢氧化钠和氢氧化钙两种饱和溶液.
| 实验一 | 实验二 | 分析 |
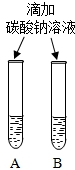 | 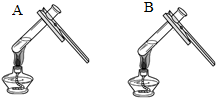 微热(不考虑水分蒸发) | 两种方案中均观察到A试管内出现白色浑浊,则A中溶液为饱和氢氧化钙溶液;方案二的设计原理是氢氧化钙的溶解度随温度升高而减小,氢氧化钠的溶解度随温度升高而增大. |

【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】①在华工生产中,原料往往不能完全转化为产品.
②工业上制取NaOH的反应原理是:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体.
③碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
【提出猜想】氢氧化钠中含有的杂质为碳酸钠和氯化钠.
提出上述猜想的理由是原料中的NaCl未完全反应,氢氧化钠与空气中的二氧化碳反应生成碳酸钠.
【进行实验】取固体于试管中,加水溶解并向溶液中加入过滤稀盐酸.
【实验结论】溶液中有明显现象,证明杂质中一定含有碳酸钠.
【反思评价】该同学想进一步证明固体中含有氢氧化钠,实验方案是取少量固体于试管中加水溶解,加入过量的氯化钙溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液,溶液变红,则固体中含有氢氧化钠.
(5)某碳酸钠样品中含有少量氯化钠.现称量11g该样品放入烧杯中,然后加入一定量溶质的质量分数为14.6%的稀盐酸,至恰好完全反应,去除溶液中的水分,最终得到12.1g氯化钠固体.计算:
①碳酸钠样品中碳酸钠的质量;
②反应后所得溶液中溶质的质量分数.(结果精确到0.1%)
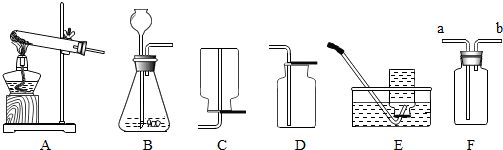
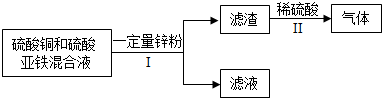
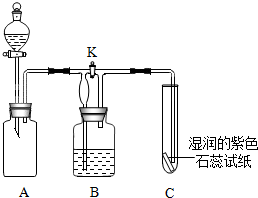 化学小组的同学利用如图所示的装置进行实验.回答相关问题:
化学小组的同学利用如图所示的装置进行实验.回答相关问题: