10.现代社会对能源和资源的需求是越来越大,下列说法正确的是( )
| A. | 提倡大量使用塑料袋 | B. | 石油属于可再生能源 | ||
| C. | 提倡回收利用废旧金属 | D. | 提倡使用含硫煤作燃料 |
9.实验室中的下列物质需要密封保存的是( )
| A. | 氯化钠 | B. | 大理石 | C. | 浓盐酸 | D. | 木炭 |
8.如图所示实验操作正确的是( )
| A. | 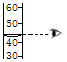 读取液体体积 | B. | 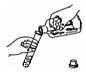 倾倒液体 | C. |  熄灭酒精灯 | D. | 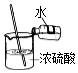 稀释浓硫酸 |
7.“遥知不是雪,为有暗香来”说明( )
| A. | 分子之间有间隔 | B. | 分子不断运动 | C. | 分子很小 | D. | 分子可分 |
6.如图是四位同学的讨论,其中错误的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
5.2017年我国在可燃冰开采技术上取得了世界性的突破.可燃冰分解出的甲烷属于( )
| A. | 混合物 | B. | 单质 | C. | 氧化物 | D. | 有机物 |
4.空气中体积分数约为21%的气体是( )
| A. | 氮气 | B. | 氧气 | C. | 稀有气体 | D. | 二氧化碳 |
3.主持测定铟、铱等元素相对原子质量新值的我国科学家是( )
| A. | 门捷列夫 | B. | 道尔顿 | C. | 张青莲 | D. | 拉瓦锡 |
2.金属材料被广泛应用于我们的生活,不仅是因为其物理性能优良,还与它们的化学性质密切相关.下面是小明同学设计测定金属铁、铜和镁的活动性的探究实验过程和实验记录,请你一起探究.
【实验目的】测定金属铁、铜和镁的活动性强弱.
【所用试剂】稀硫酸,硝酸银溶液,光亮的薄铁片、薄铜片、薄镁片.
【实验过程】
步骤Ⅰ:将铁片、铜片、镁片分别在空气中点燃片刻,观察燃烧的现象;
步骤Ⅱ:将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的稀硫酸的试管中;
步骤Ⅲ:将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的硝酸银溶液的试管中.
实验现象记录表
【实验记录】用“√”表示能观察到实验现象,用“-”表示观察不到实验现象(具体见上表).
(1)通过步骤Ⅰ可以得出三种金属中镁的金属活动性最强,判断依据是镁能够在空气中燃烧.
(2)运用“控制变量法”设计实验方案是化学研究的重要方法.步骤Ⅱ和步骤Ⅲ中,需要控制的实验条件除了金属的体积、溶液的体积、溶质质量分数以外,还需要控制的条件是温度.
【实验结论】金属铁、铜和镁的活动性由强到弱的顺序是Mg>Fe>Cu(元素符号表示).
【反思与交流】若利用上述试剂制取氢气,小明认为应该选择金属铁和稀硫酸反应,而不选择金属镁和稀硫酸反应,他的理由是镁和稀硫酸反应的速率太快,不利于控制和收集.
0 159362 159370 159376 159380 159386 159388 159392 159398 159400 159406 159412 159416 159418 159422 159428 159430 159436 159440 159442 159446 159448 159452 159454 159456 159457 159458 159460 159461 159462 159464 159466 159470 159472 159476 159478 159482 159488 159490 159496 159500 159502 159506 159512 159518 159520 159526 159530 159532 159538 159542 159548 159556 211419
【实验目的】测定金属铁、铜和镁的活动性强弱.
【所用试剂】稀硫酸,硝酸银溶液,光亮的薄铁片、薄铜片、薄镁片.
【实验过程】
步骤Ⅰ:将铁片、铜片、镁片分别在空气中点燃片刻,观察燃烧的现象;
步骤Ⅱ:将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的稀硫酸的试管中;
步骤Ⅲ:将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的硝酸银溶液的试管中.
实验现象记录表
| 金属 | 空气 | 稀硫酸 | 硝酸银溶液 |
| 铁 | - | √ | √ |
| 铜 | - | - | √ |
| 镁 | √ | √ | √ |
(1)通过步骤Ⅰ可以得出三种金属中镁的金属活动性最强,判断依据是镁能够在空气中燃烧.
(2)运用“控制变量法”设计实验方案是化学研究的重要方法.步骤Ⅱ和步骤Ⅲ中,需要控制的实验条件除了金属的体积、溶液的体积、溶质质量分数以外,还需要控制的条件是温度.
【实验结论】金属铁、铜和镁的活动性由强到弱的顺序是Mg>Fe>Cu(元素符号表示).
【反思与交流】若利用上述试剂制取氢气,小明认为应该选择金属铁和稀硫酸反应,而不选择金属镁和稀硫酸反应,他的理由是镁和稀硫酸反应的速率太快,不利于控制和收集.