16. NaNO2是-种致癌物质.某兴趣小组为研究水中NaNO2的含量,进行了如下目视比色法实验(比较溶液颜色深浅以测定物质浓度的方法),请你参与实验,并填空:
NaNO2是-种致癌物质.某兴趣小组为研究水中NaNO2的含量,进行了如下目视比色法实验(比较溶液颜色深浅以测定物质浓度的方法),请你参与实验,并填空:
(1)测定方法的研究:配制质量分数为0.07%的NaNO2标准溶液,分别取0、2、4、6、8、10mL标准溶液于6支试管,加蒸馏水至总体积均为l0mL,分别加入约0.30gM粉未(M是氨基苯磺酸),振荡后制成颜色深浅不同的标准色阶.测定时取10mL水样,加入约0.30gM粉末,振荡后与标准色阶比较,得出颜色相同的色阶所含标准溶液的毫升数,再按稀释比例计算出水样中NaNO2的质量分数(水和稀溶液的密度均按l g•cm-3计算).①配制质量分数为0.07%的NaNO2溶液l000mL,所需NaNO2的质量是0.7g;②用上述方法测定某水样,其与含2mL标准溶液的色阶颜色相同,此水样中NaNO2的质量分数为0.014%;
(2)研究某水样在不同煮沸时间后NaNO2含量的变化:
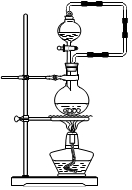
将另一水样用如图装置煮沸,测定不同煮沸时间NaNO2的质量分数,结果为:
①兴趣小组设计的如图实验装置用到了蒸气回流装置,其作用是保持水的总量不变;
②根据上述数据,可见此水样随煮沸时间的延长NaNO2的质量分数会逐渐增大.
 NaNO2是-种致癌物质.某兴趣小组为研究水中NaNO2的含量,进行了如下目视比色法实验(比较溶液颜色深浅以测定物质浓度的方法),请你参与实验,并填空:
NaNO2是-种致癌物质.某兴趣小组为研究水中NaNO2的含量,进行了如下目视比色法实验(比较溶液颜色深浅以测定物质浓度的方法),请你参与实验,并填空:(1)测定方法的研究:配制质量分数为0.07%的NaNO2标准溶液,分别取0、2、4、6、8、10mL标准溶液于6支试管,加蒸馏水至总体积均为l0mL,分别加入约0.30gM粉未(M是氨基苯磺酸),振荡后制成颜色深浅不同的标准色阶.测定时取10mL水样,加入约0.30gM粉末,振荡后与标准色阶比较,得出颜色相同的色阶所含标准溶液的毫升数,再按稀释比例计算出水样中NaNO2的质量分数(水和稀溶液的密度均按l g•cm-3计算).①配制质量分数为0.07%的NaNO2溶液l000mL,所需NaNO2的质量是0.7g;②用上述方法测定某水样,其与含2mL标准溶液的色阶颜色相同,此水样中NaNO2的质量分数为0.014%;
(2)研究某水样在不同煮沸时间后NaNO2含量的变化:
将另一水样用如图装置煮沸,测定不同煮沸时间NaNO2的质量分数,结果为:
| 煮沸时间(小时) | 0 | 2 | 4 | 8 | 12 |
| NaNO2的质量分数 | 0 | 0 | 0.014% | 0.028% | 0.056% |
②根据上述数据,可见此水样随煮沸时间的延长NaNO2的质量分数会逐渐增大.
15.隐形眼镜洗液的主要成分是 H2O2(双氧水).下列说法正确的是( )
| A. | H2O2是由氢气和氧气组成的 | |
| B. | H2O2是由氢元素和氧元素组成的 | |
| C. | H2O2是氢分子和氧分子构成的 | |
| D. | H2O2是由两个氢元素和两个氧元素构成的 |
8.生命的孕育和维系需要水,科学研究离不开水.请你完成下列探究.
探究一:用水作溶剂.在盛有5ml水和5ml汽油的两只试管中各加入1~2小粒高锰酸钾,可观察到的现象是高锰酸钾溶于水形成紫红色溶液,而高锰酸钾难溶于汽油,结论:同一种物质在不同溶剂中的溶解性不同.
探究二:用水区别物质.自选两种白色固体,用水区别它们,设计实验完成下表内容.
探究三:溶质在水中的溶解与结晶.
【查阅资料】?20℃时,五种物质的溶解度如下表.
?相同温度下,不同溶质同时溶解在同一溶剂中,溶解度不变.
【提出问题】20℃时,将11.7gNaCl和15.8gNH4HCO3同时放入盛有100g水的烧杯中,充分搅拌,静置,有晶体析出(温度仍为20℃).析出的晶体是什么?
【设计实验】设计方案,并进行实验.
(1)取少量晶体与熟石灰粉末混合、研磨,无明显现象.实验目的是证明晶体不是氯化铵.
(2)取少量晶体于试管中,加入盐酸,现象为有无色气体产生.
【实验结论】(3)析出的晶体是NaHCO3,晶体的质量为7.2g.
【实验拓展】(4)析出晶体的原因是NaCl和NH4HCO3溶于水未达饱和,所以不能以晶体析出,它们在水中解离出Na+、Cl-、NH4+、HCO3-,阴阳离子运动结合成NaHCO3和NH4Cl,由于NH4Cl溶解度较大,未达饱和,故不能析出,但NaHCO3的溶解度小,且溶液已达饱和,所以过多的NaHCO3以晶体形式析出.
0 159072 159080 159086 159090 159096 159098 159102 159108 159110 159116 159122 159126 159128 159132 159138 159140 159146 159150 159152 159156 159158 159162 159164 159166 159167 159168 159170 159171 159172 159174 159176 159180 159182 159186 159188 159192 159198 159200 159206 159210 159212 159216 159222 159228 159230 159236 159240 159242 159248 159252 159258 159266 211419
探究一:用水作溶剂.在盛有5ml水和5ml汽油的两只试管中各加入1~2小粒高锰酸钾,可观察到的现象是高锰酸钾溶于水形成紫红色溶液,而高锰酸钾难溶于汽油,结论:同一种物质在不同溶剂中的溶解性不同.
探究二:用水区别物质.自选两种白色固体,用水区别它们,设计实验完成下表内容.
| 两种白色固体 | 主要操作、现象和结论 |
| 碳酸钙、氧化钙 | 分别将两种固体加水溶解,难溶于水的是碳酸钙,与水剧烈反应且有热量放出的是氧化钙 |
【查阅资料】?20℃时,五种物质的溶解度如下表.
| 物质 | NaCl | NH4HCO3 | NH4Cl | NaHCO3 | Na2CO3 |
| 溶解度/g | 36.0 | 21.0 | 37.2 | 9.6 | 21.5 |
【提出问题】20℃时,将11.7gNaCl和15.8gNH4HCO3同时放入盛有100g水的烧杯中,充分搅拌,静置,有晶体析出(温度仍为20℃).析出的晶体是什么?
【设计实验】设计方案,并进行实验.
(1)取少量晶体与熟石灰粉末混合、研磨,无明显现象.实验目的是证明晶体不是氯化铵.
(2)取少量晶体于试管中,加入盐酸,现象为有无色气体产生.
【实验结论】(3)析出的晶体是NaHCO3,晶体的质量为7.2g.
【实验拓展】(4)析出晶体的原因是NaCl和NH4HCO3溶于水未达饱和,所以不能以晶体析出,它们在水中解离出Na+、Cl-、NH4+、HCO3-,阴阳离子运动结合成NaHCO3和NH4Cl,由于NH4Cl溶解度较大,未达饱和,故不能析出,但NaHCO3的溶解度小,且溶液已达饱和,所以过多的NaHCO3以晶体形式析出.