15.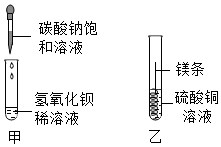 某同学进行如图两个实验:
某同学进行如图两个实验:
(l)甲实验中反应的化学方程式为Ba(OH)2+Na2CO3═BaCO3↓+2NaOH;
(2)乙实验观察到的现象是镁条表面出现红色固体,溶液由蓝色变成无色
(3)把甲、乙反应后的溶液倒入同一烧杯,发现有白色沉淀生成.他决定对白色沉淀的成分进行探究.
【查阅资料】硫酸钡不溶于酸.
【提出猜想】白色沉淀为:Ⅰ.Mg(OH)2;Ⅱ.Mg(OH)2和BaSO4;Ⅲ.Mg(OH)2和MgCO3.
【实验方案】
【拓展与思考】如果猜想Ⅲ成立,产生此结果的原因是做甲实验时滴加的碳酸钠过量;上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是甲反应后的溶液中碳酸钠与氢氧化钡不能共存.
 某同学进行如图两个实验:
某同学进行如图两个实验:(l)甲实验中反应的化学方程式为Ba(OH)2+Na2CO3═BaCO3↓+2NaOH;
(2)乙实验观察到的现象是镁条表面出现红色固体,溶液由蓝色变成无色
(3)把甲、乙反应后的溶液倒入同一烧杯,发现有白色沉淀生成.他决定对白色沉淀的成分进行探究.
【查阅资料】硫酸钡不溶于酸.
【提出猜想】白色沉淀为:Ⅰ.Mg(OH)2;Ⅱ.Mg(OH)2和BaSO4;Ⅲ.Mg(OH)2和MgCO3.
【实验方案】
| 实验操作 | 实验现象与结论 |
| 过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①若沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化学反应方程式为Mg(OH)2+2HCl=MgCl2+2H2O. ②若白色沉淀部分溶解且无气体产生,猜想Ⅱ成立. ③若沉淀完全溶解,且有气体产生,猜想Ⅲ成立. |
13.下列说法正确的是( )
| A. | 将冷蝶子放在蜡烛火焰的上方,可以得到炭黑 | |
| B. | 医疗上常采用煮沸的方法将硬水变成软水 | |
| C. | 用NH4Cl和Ca(OH)2 同时施入农田,即解决了农田的肥料问题又中和了土壤的酸性 | |
| D. | 洗涤剂和汽油都能清洗油污,二者原理相同 |
12.下列化学反应属于关系图中阴影部分的是( )


| A. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | B. | CO+CuO$\frac{\underline{\;加热\;}}{\;}$Cu+CO2 | ||
| C. | CaO+H2O═Ca(OH)2 | D. | 2NaOH+H2SO4=Na2SO4+2H2O |
11.化学就在我们身边,生活中处处有化学.根据你所学过的化学知识,判断下列说法错误的是( )
| A. | 在酱油中加适量的“铁”可预防缺铁性贫血 | |
| B. | “请往菜里加点盐”中的“盐”特指食盐--NaCl | |
| C. | 青少年正在长身体,应多吃富含蛋白质的肉类,少吃蔬菜和水果 | |
| D. | 生活中不能用工业用盐亚硝酸钠烹调食物,是因为亚硝酸钠是有毒的物质 |
10.下列叙述正确的是( )
| A. | 由同种分子构成的物质不一定是纯净物 | |
| B. | 铁制金属防盗门上的锈可以阻止防盗门再生锈 | |
| C. | 湖水经沉淀、过滤、吸附等净化处理后,即可得纯水 | |
| D. | 热塑性塑料和热固性塑料可以通过加热观察外形变化来区别 |
9.下列事实与解释相符的是( )
| A. | 干冰用作制冷剂--干冰是冰 | |
| B. | 酸雨是PH<5.6的雨水--二氧化碳是形成酸雨的主要气体 | |
| C. | 用炭黑墨汁书写的字经久不变色--常温下,碳的化学性质稳定 | |
| D. | 制糖工业用活性炭脱色制白糖--活性炭和有色物质反应 |
7.钙元素是一种重要的金属元素,它形成的物质种类很多.
(1)氢化钙(CaH2)固体是登山运动员常用的能源提供剂.
某实验探究小组的通许通过查阅资料得知:CaH2能与H2O反应生成Ca(OH)2和H2,请你写出该反应的化学方程式CaH2+2H2O═Ca(OH)2+2H2↑.
(2)生石灰溶于水可制得熟石灰,该反应过程中能量的变化是放热(填“吸热”或“放热”),实验室可以用pH试纸测定其溶液的酸碱度.
(3)实验探究小组将Na2CO3溶液滴加到Ca(OH)2溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【做出猜想】
猜想一:NaOH 猜想二:NaOH和Ca(OH)2
猜想三:NaOH和Na2CO3 猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,原因是因为氢氧化钙和碳酸钠不能共存.
【实验过程】
【拓展延伸】在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑原反应的物质是否过量.
0 157711 157719 157725 157729 157735 157737 157741 157747 157749 157755 157761 157765 157767 157771 157777 157779 157785 157789 157791 157795 157797 157801 157803 157805 157806 157807 157809 157810 157811 157813 157815 157819 157821 157825 157827 157831 157837 157839 157845 157849 157851 157855 157861 157867 157869 157875 157879 157881 157887 157891 157897 157905 211419
(1)氢化钙(CaH2)固体是登山运动员常用的能源提供剂.
某实验探究小组的通许通过查阅资料得知:CaH2能与H2O反应生成Ca(OH)2和H2,请你写出该反应的化学方程式CaH2+2H2O═Ca(OH)2+2H2↑.
(2)生石灰溶于水可制得熟石灰,该反应过程中能量的变化是放热(填“吸热”或“放热”),实验室可以用pH试纸测定其溶液的酸碱度.
(3)实验探究小组将Na2CO3溶液滴加到Ca(OH)2溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【做出猜想】
猜想一:NaOH 猜想二:NaOH和Ca(OH)2
猜想三:NaOH和Na2CO3 猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,原因是因为氢氧化钙和碳酸钠不能共存.
【实验过程】
| 实验步骤 | 现象 | 结论 |
| 实验Ⅰ:取滤液,向其中滴入适量Na2CO3溶液 | 没有明显现象 | 猜想二不成立 |
| 实验Ⅱ:另取滤液,向其中加入足量 稀盐酸 | 产生气泡 | 猜想 三成立 |
 (1)做实验时要严格遵守实验室规则.请写出“题19图”这些同学做化学实验时的违规行为(写三点):①在实验室内追逐打闹;②在实验室里吃喝食物(或尝药品的味道);③用手直接拿着试管加热.
(1)做实验时要严格遵守实验室规则.请写出“题19图”这些同学做化学实验时的违规行为(写三点):①在实验室内追逐打闹;②在实验室里吃喝食物(或尝药品的味道);③用手直接拿着试管加热.