11.下列能量的转化中,不属于物理变化的是( )
| A. | 太阳能热水器提供热水 | B. | 水力发电 | ||
| C. | 燃烧天然气做饭 | D. | 电取暖器取暖 |
7.在实验室中,仅用下表提供的仪器和药品,就能达到相应实验目的是( )
| 编号 | 仪器 | 药品 | 实验目的 |
| A | 试管、胶头滴管 | 未知溶液、Ba(NO3)2溶液、稀硝酸 | 检验未知溶液中是否含有SO42- |
| B | 试管、胶头滴管 | ZnSO4溶液、铜片、铁丝 | 证明Cu、Zn、Fe的佥属活动性 |
| C | 试管、胶头滴管 | 久置的NaOH溶液、酚酞 | 检验久置的NaOH溶液是否完全变质 |
| D | 烧杯、漏斗、滤纸、铁架台(带铁圈)、药匙 | 粗盐、蒸馏水 | 除去粗盐中的难溶性杂质 |
| A. | A | B. | B | C. | C | D. | D |
6.学习完“原子的构成”之后,萍萍同学形成了以下认识,其中错误的是( )
| A. | 原子由居于中心的原子核和核外电子构成 | |
| B. | 核外电子在离核远近不同的区域中运动 | |
| C. | 原子核的质量和电子的质量相差不大 | |
| D. | 原子核的体积与整个原子的体积相比要小很多 |
5.2017年1月27日,南京理工大学化学学院胡炳成团队成功合成世界上首个超高能全氨阴离子(N5-)钴(Co)盐【化学式为:Co(N5)2(H2O)4】.下列有关说法正确的是( )
| A. | 该物质属于混合物 | |
| B. | 该物质中钻元素的质量分数比氧元素的质量分数小 | |
| C. | 该物质中钴元素的化台价为+5价 | |
| D. | 该物质属于有机物 |
4.2017年我国海域可燃冰开采取得重大突破.下列有关可燃冰的叙述正确的是( )
| A. | 可燃冰是一种纯净物 | |
| B. | 可燃冰在常温常压下不易长久保存 | |
| C. | 可燃冰的成功开发利用使“水变油”成为可能 | |
| D. | 可燃冰作为一种清洁能源对环境没有任何危害 |
3.关于碳循环和氧循环,下列说法不正确的是( )
| A. | 碳循环和氧循环分别是指二氧化碳和氧气的循环 | |
| B. | 碳循环和氧循环过程中均发生了化学变化 | |
| C. | 绿色植物的生长过程,既涉及碳循环,又涉及氧循环 | |
| D. | 碳循环和氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定 |
2.干冰和二氧化碳气体都是由二氧化碳分子直接构成的.对于两者中的二氧化碳分子的比对结果,正确的是( )
0 157568 157576 157582 157586 157592 157594 157598 157604 157606 157612 157618 157622 157624 157628 157634 157636 157642 157646 157648 157652 157654 157658 157660 157662 157663 157664 157666 157667 157668 157670 157672 157676 157678 157682 157684 157688 157694 157696 157702 157706 157708 157712 157718 157724 157726 157732 157736 157738 157744 157748 157754 157762 211419
| A. | 分子运动速率相同 | B. | 分子之间相互作用的强弱相同 | ||
| C. | 化学性质相同 | D. | 分子之间的间隔相同 |

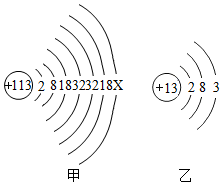 元素家族新成员--鉨(nǐ)
元素家族新成员--鉨(nǐ)