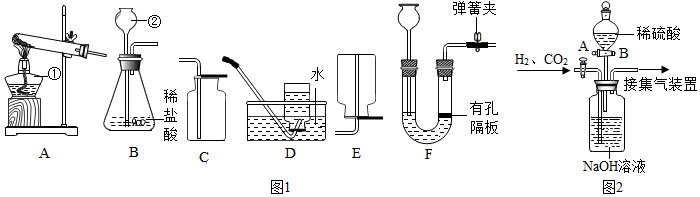
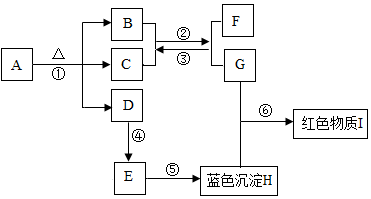
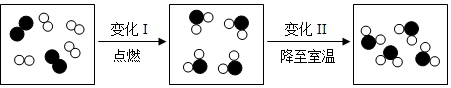
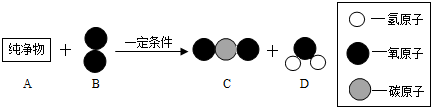
2.某兴趣小组为了研究露置于空气中的纯净生灰石(CaO)的变质情况,进行了如下实验:
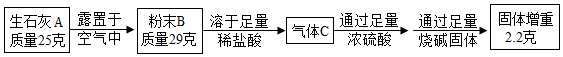
下列结论正确的是( )

下列结论正确的是( )
| A. | A转化为B过程中钙元素的质量分数逐渐增大 | |
| B. | 若无浓硫酸,则粉末B中CaO质量测定值偏小 | |
| C. | 粉末B中Ca(OH)2质量为5.0 g | |
| D. | A到B中生石灰的变质程度为33.6% |
20.某兴趣小组的同学为了探究化学反应前后反应物与生成物之间的质量关系设计了如下三个实验:
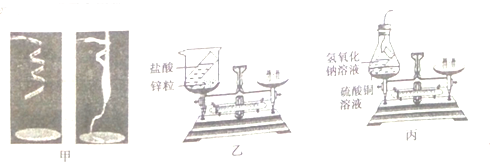
实验甲:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验乙:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会再称量.(化学方程式是:Zn+2HCl=ZnCl2+H2↑)
实验丙:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥形瓶口塞上橡皮塞,称量,然后设法将两种溶液接触,过一会再称量.(化学方程式是:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4)
他们得到三次实验的数据如表:
(1)在实验甲中反应后的质量比反应前明显增加了,请解释原因:镁燃烧时,和空气中的氧气反应生成了氧化镁,因此氧化镁的质量大于反应的镁的质量.
(2)由上表中数据分析可知实验甲中参加反应的氧气质量为3.2g,实验乙中生成氢气的质量为0.2g.
(3)在上述三个实验中都遵循(填“遵循”或者“不遵循”)质量守恒定律,但只有实验丙正确反映了反应物与生成物之间的总质量关系,因此,用实验来探究化学反应前后反应物与生成物之间的总质量关系时,当有气体参加或生成时,必须在密闭容器中进行.
(4)请从分子、原子的角度解释反应前后质量相等的原因:反应前后原子的种类、总个数、质量都不变.
(5)在化学反应前后,肯定不会变化的是①③④.
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类 ⑥物质的体积 ⑦物质的状态
(6)质量守恒定律这条结论的获得对化学研究的重大意义在于可以定量进行化学反应.

实验甲:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验乙:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会再称量.(化学方程式是:Zn+2HCl=ZnCl2+H2↑)
实验丙:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥形瓶口塞上橡皮塞,称量,然后设法将两种溶液接触,过一会再称量.(化学方程式是:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4)
他们得到三次实验的数据如表:
| 编号 | 实验甲 | 实验乙 | 实验丙 |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
(2)由上表中数据分析可知实验甲中参加反应的氧气质量为3.2g,实验乙中生成氢气的质量为0.2g.
(3)在上述三个实验中都遵循(填“遵循”或者“不遵循”)质量守恒定律,但只有实验丙正确反映了反应物与生成物之间的总质量关系,因此,用实验来探究化学反应前后反应物与生成物之间的总质量关系时,当有气体参加或生成时,必须在密闭容器中进行.
(4)请从分子、原子的角度解释反应前后质量相等的原因:反应前后原子的种类、总个数、质量都不变.
(5)在化学反应前后,肯定不会变化的是①③④.
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类 ⑥物质的体积 ⑦物质的状态
(6)质量守恒定律这条结论的获得对化学研究的重大意义在于可以定量进行化学反应.
17.如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,下列说法正确是( )
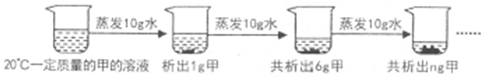

| A. | 蒸发前原溶液是饱和溶液 | B. | 甲的溶解度随温度的升高而减小 | ||
| C. | n的数值是11 | D. | 20℃时甲的溶解度是6g |
16.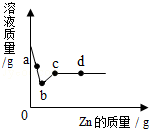 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法不正确的是( )
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法不正确的是( )
0 157230 157238 157244 157248 157254 157256 157260 157266 157268 157274 157280 157284 157286 157290 157296 157298 157304 157308 157310 157314 157316 157320 157322 157324 157325 157326 157328 157329 157330 157332 157334 157338 157340 157344 157346 157350 157356 157358 157364 157368 157370 157374 157380 157386 157388 157394 157398 157400 157406 157410 157416 157424 211419
 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法不正确的是( )
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法不正确的是( )| A. | 取a点溶液,滴加稀盐酸,产生白色沉淀 | |
| B. | 图标上b~c段质量增加的原因是Zn与Cu(NO3)2溶液反应 | |
| C. | b点时溶液中金属离子有Zn2+、Cu2+,金属单质有Zn、Cu、Ag | |
| D. | c点和d点溶质种类相同,金属单质种类不同 |