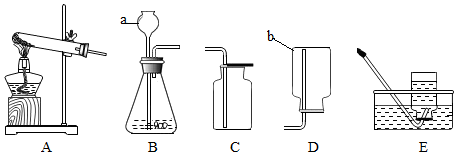
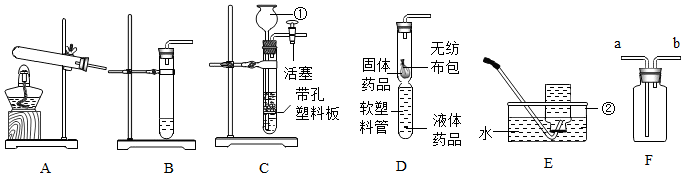
10.(1)实验室制得的二氧化碳中常含有水蒸气和少量酸 雾,为了获得纯净的二氧化碳可选用如图中的C套装置来净化.
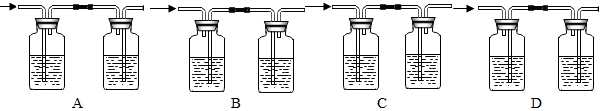
其中左瓶中应盛碳酸氢钠溶液;右瓶中应盛浓硫酸.
(2)向氢氧化钠溶液中通入适量二氧化碳后,仅使溶液中 50%的氢氧化钠反应,反应后溶液中 CO${\;}_{3}^{2-}$和 OH的个数比为1:2.
(3)现将石灰石样品 15g 与 105.4g 稀盐酸放入烧杯中充分反应(杂质不溶于水也不与稀 盐酸反应),反应时间与反应前后烧杯内物质的质量变化如表所示:
请计算回答:①样品中碳酸钙的质量分数.(计算结果保留 1 位小数)
②反应后所得溶液中溶质的质量分数.

其中左瓶中应盛碳酸氢钠溶液;右瓶中应盛浓硫酸.
(2)向氢氧化钠溶液中通入适量二氧化碳后,仅使溶液中 50%的氢氧化钠反应,反应后溶液中 CO${\;}_{3}^{2-}$和 OH的个数比为1:2.
(3)现将石灰石样品 15g 与 105.4g 稀盐酸放入烧杯中充分反应(杂质不溶于水也不与稀 盐酸反应),反应时间与反应前后烧杯内物质的质量变化如表所示:
| 反应时间/s | 20 | 40 | 60 | 80 | 100 | 120 |
| 质量/g | 119.52 | 118.64 | 117.76 | 116.88 | 116 | 116 |
②反应后所得溶液中溶质的质量分数.
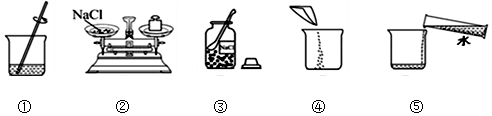
7.下列四个实验方案设计不合理的是( )
| 选项 | 实验目的 | 方案 |
| A | 鉴别硝酸钠溶液和硫酸钾溶液 | 取样,滴加 Ba(NO3)2 溶液,观察现象 |
| B | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、蒸发 |
| D | 除去 CaO 中的 CaCO3 | 高温加热到固体质量不变 |
| D | 探究 Mg、Ag、Cu 金属的活动性顺序 | 将两根光亮的镁条分别伸入硫酸铜溶液和硝酸银溶液中 |
| A. | A | B. | B | C. | C | D. | D |
6.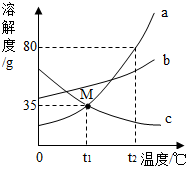 如图是不含结晶水的 a、b、c 三种物质的溶解度曲线,下列说法正确的是( )
如图是不含结晶水的 a、b、c 三种物质的溶解度曲线,下列说法正确的是( )
0 157078 157086 157092 157096 157102 157104 157108 157114 157116 157122 157128 157132 157134 157138 157144 157146 157152 157156 157158 157162 157164 157168 157170 157172 157173 157174 157176 157177 157178 157180 157182 157186 157188 157192 157194 157198 157204 157206 157212 157216 157218 157222 157228 157234 157236 157242 157246 157248 157254 157258 157264 157272 211419
 如图是不含结晶水的 a、b、c 三种物质的溶解度曲线,下列说法正确的是( )
如图是不含结晶水的 a、b、c 三种物质的溶解度曲线,下列说法正确的是( )| A. | t2℃时,将 50g a 物质加入到 50g 水中充分搅拌,得到 100g a 的饱和溶液 | |
| B. | 用等质量的 a、b、c 三种固体配制成 t2℃时的饱和溶液,所得溶液质量的大小关系是:c 溶液>b 溶液>a 溶液 | |
| C. | 将 t1℃时三种物质的饱和溶液升温到 t2℃时,所得溶液中溶质的质量分数的大小关系是:b>a=c | |
| D. | 将 t2℃时 a、b 两种物质的饱和溶液降温到 t1℃时,析出晶体的质量:a>b |