10. 碱式碳酸铜是一种难溶于水的绿色固体,受热易分解为氧化铜、水和二氧化碳.利用如图装置加热碱式碳酸铜一段时间,下列有关 描述正确的是( )
碱式碳酸铜是一种难溶于水的绿色固体,受热易分解为氧化铜、水和二氧化碳.利用如图装置加热碱式碳酸铜一段时间,下列有关 描述正确的是( )
 碱式碳酸铜是一种难溶于水的绿色固体,受热易分解为氧化铜、水和二氧化碳.利用如图装置加热碱式碳酸铜一段时间,下列有关 描述正确的是( )
碱式碳酸铜是一种难溶于水的绿色固体,受热易分解为氧化铜、水和二氧化碳.利用如图装置加热碱式碳酸铜一段时间,下列有关 描述正确的是( )| A. | 试管口有水珠生成 | |
| B. | 试管内的固体由绿色变为红色 | |
| C. | 烧杯内盛放 NaOH 溶液检验生成的 CO2 | |
| D. | 实验结束后应先停止加热,后将导管移出烧杯 |
9.归纳与比较”是化学学习的主要方法.下列关于CO2与CO的不同点比较错误的是( )
| A. | 组成:组成元素相同,碳元素的化合价不同 | |
| B. | 性质:CO2能溶于水,与水反应生成碳酸; CO难溶于水,但能燃烧 | |
| C. | 用途:CO2可用于光合作用、灭火等; CO可作气体燃料,还可用于人工降雨 | |
| D. | 危害:CO2会造成“温室效应”; CO易与血液中的血红蛋白结合引起中毒 |
5.元素钴(Co)有多种化合价,将11.9gCoCO3在纯净氧气中加热可得到8.3g钴的氧化物,则CoCO3在纯氧中受强热发生反应的化学方程式是( )
| A. | CoCO3+O2$\frac{\underline{\;强热\;}}{\;}$CoCO2+CO2 | B. | 2CoCO3+O2$\frac{\underline{\;强热\;}}{\;}$2CoCO2+2CO2 | ||
| C. | 4CoCO3+O2$\frac{\underline{\;强热\;}}{\;}$2Co2O3+4CO2 | D. | 4CoCO2+3O2$\frac{\underline{\;强热\;}}{\;}$2Co2O3+4CO2 |
4.越来越多的人开始关注雾霾天气与健康的问题,关于雾和霾的认识,下列说法中正确的是( )
| A. | 霾是大量的小水滴或冰晶浮游在近地面空气层中形成的 | |
| B. | 雾和霾是两种不同的天气现象 | |
| C. | 雾是由悬浮在大气中的大量微小尘粒、烟粒或盐粒等颗粒形成的 | |
| D. | 雾对人体健康影响不大,但霾有害健康 |
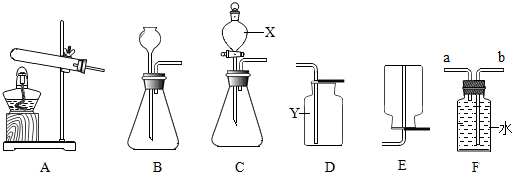
2. 利用如图装置可进行气体性质的探究实验.a处通入无色气体(可能是H2、CO或CO2);b处玻璃管中盛放黑色粉末(可能是CuO或C),c处试管中盛放澄清石灰水.下列说法正确的是( )
利用如图装置可进行气体性质的探究实验.a处通入无色气体(可能是H2、CO或CO2);b处玻璃管中盛放黑色粉末(可能是CuO或C),c处试管中盛放澄清石灰水.下列说法正确的是( )
 利用如图装置可进行气体性质的探究实验.a处通入无色气体(可能是H2、CO或CO2);b处玻璃管中盛放黑色粉末(可能是CuO或C),c处试管中盛放澄清石灰水.下列说法正确的是( )
利用如图装置可进行气体性质的探究实验.a处通入无色气体(可能是H2、CO或CO2);b处玻璃管中盛放黑色粉末(可能是CuO或C),c处试管中盛放澄清石灰水.下列说法正确的是( )| A. | 若为H2与CuO的反应,b处玻璃管观察到现象为:黑色氧化铜变成红色的铜 | |
| B. | 若为H2与CuO的反应,为了进一步确定另一产物是水,需要b、c之间增加一个盛有硫酸铜溶液的试剂瓶 | |
| C. | 若为CO与CuO的反应,化学方程式为:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | |
| D. | 若为CO2与C的反应,d处导管尖嘴口需用酒精灯点燃主要目的是:证明高温下CO2与C能反应,且产物为CO,并进行尾气处理 |
1.实验室有一瓶长期放置的氢氧化钠固体,某兴趣小组同学欲对该固体变质情况进行探究.
【提出问题】该瓶氢氧化钠固体是否变质,变质情况如何?
【查阅资料】①氢氧化钠在空气中容易变质但不会转化为NaHCO3;
②CaCl2溶液呈中性
③盐酸加入到氢氧化钠和碳酸钠的混合溶液中,盐酸先和氢氧化钠反应
【提出猜想】猜想Ⅰ:固体未变质
猜想Ⅱ:固体全部变质
猜想Ⅲ:固体部分变质
【原因分析】氢氧化钠在空气中变质的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示).
【进行实验】
小聪同学取少量样品于烧杯中,用足量水溶解,再向溶液中滴入几滴酚酞试液,溶液变红,由此他得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是碳酸钠溶液显碱性,也能使酚酞试液变红色;
小玲同学也取少量样品于烧杯中,用足量水溶解,再向溶液中滴加几滴稀盐酸,未发现有气泡产生.据此现象小玲认为NaOH未变质.你认为该结论是否正确?不正确请说明理由若固体为氢氧化钠和碳酸钠的混合物,滴加少量盐酸,如果盐酸不能把氢氧化钠完全消耗时,也不会产生气泡.
为了进一步得出结论,该兴趣小组同学结合所给资料分工合作,集思广益,设计了下列实验进行验证.请将下表补充完整.
【反思评价】
(1)在实验步骤 ①中为什么要加入过量的CaCl2溶液?检验并除去碳酸钠
(2)小玲同学认为在实验步骤 ①中可以用Ca(OH)2 溶液代替CaCl2证明这一瓶中是否含有NaOH,你认为呢?并说明理由不可行,因为氢氧化钙和碳酸钠反应会生成氢氧化钠,干扰对样品中氢氧化钠的检验.
0 156713 156721 156727 156731 156737 156739 156743 156749 156751 156757 156763 156767 156769 156773 156779 156781 156787 156791 156793 156797 156799 156803 156805 156807 156808 156809 156811 156812 156813 156815 156817 156821 156823 156827 156829 156833 156839 156841 156847 156851 156853 156857 156863 156869 156871 156877 156881 156883 156889 156893 156899 156907 211419
【提出问题】该瓶氢氧化钠固体是否变质,变质情况如何?
【查阅资料】①氢氧化钠在空气中容易变质但不会转化为NaHCO3;
②CaCl2溶液呈中性
③盐酸加入到氢氧化钠和碳酸钠的混合溶液中,盐酸先和氢氧化钠反应
【提出猜想】猜想Ⅰ:固体未变质
猜想Ⅱ:固体全部变质
猜想Ⅲ:固体部分变质
【原因分析】氢氧化钠在空气中变质的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示).
【进行实验】
小聪同学取少量样品于烧杯中,用足量水溶解,再向溶液中滴入几滴酚酞试液,溶液变红,由此他得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是碳酸钠溶液显碱性,也能使酚酞试液变红色;
小玲同学也取少量样品于烧杯中,用足量水溶解,再向溶液中滴加几滴稀盐酸,未发现有气泡产生.据此现象小玲认为NaOH未变质.你认为该结论是否正确?不正确请说明理由若固体为氢氧化钠和碳酸钠的混合物,滴加少量盐酸,如果盐酸不能把氢氧化钠完全消耗时,也不会产生气泡.
为了进一步得出结论,该兴趣小组同学结合所给资料分工合作,集思广益,设计了下列实验进行验证.请将下表补充完整.
| 实验步骤 | 反应方程式 | 实验现象 | 结论 |
| ①将该样品配制成溶液,滴加过量CaCl2溶液 | CaCl2+Na2CO3═CaCO3↓+2NaCl | 产生白色沉淀 | 猜想Ⅲ正确 |
| ②对①进行过滤,向滤液中滴加 酚酞试液 | 溶液变红 |
(1)在实验步骤 ①中为什么要加入过量的CaCl2溶液?检验并除去碳酸钠
(2)小玲同学认为在实验步骤 ①中可以用Ca(OH)2 溶液代替CaCl2证明这一瓶中是否含有NaOH,你认为呢?并说明理由不可行,因为氢氧化钙和碳酸钠反应会生成氢氧化钠,干扰对样品中氢氧化钠的检验.