8.下列条件下的石灰水中,溶质的质量分数最大的是( )
| A. | 20℃的饱和溶液 | B. | 20℃的不饱和溶液 | C. | 60℃的饱和溶液 | D. | 60℃的不饱和溶液 |
7.农业生产中常用溶质质量分数为16%的氯化钠溶液来选种.对该溶液理解正确的是( )
| A. | 溶液中含氯化钠10克 | B. | 溶液质量为100克 | ||
| C. | 每100克溶液中含氯化钠16克 | D. | 每100克水中含氯化钠16克 |
6.20℃时,某物质在50克水中,最多溶解0.8克,则该物质的溶解性为( )
| A. | 可溶 | B. | 易溶 | C. | 微溶 | D. | 难溶 |
5.下列加速固体溶解的措施中,能改变固体溶解度的是( )
| A. | 加热 | B. | 把固体研细 | C. | 搅拌 | D. | 振荡 |
4.下列因素对固体物质的溶解度没有影响的是( )
| A. | 溶质的性质 | B. | 溶剂的性质 | C. | 温度 | D. | 搅拌 |
3.能证明20℃时硝酸钾的溶液已达到饱和的方法是( )
| A. | 向20℃时的该溶液中加入硝酸钾固体,固体不溶解 | |
| B. | 取少量溶液降温到0℃,有固体析出 | |
| C. | 取出少量溶液升温到50℃,无固体析出 | |
| D. | 向20℃时的该溶液中加入少量水,溶液变稀 |
2.下列方法能使海水转化为饮用水的是( )
| A. | 过滤 | B. | 吸附 | C. | 搅拌 | D. | 蒸馏 |
1.漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应.Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
(1)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小 (填“增大”或“减小”或“不变”).
(2)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2+2HCl=CaCl2+2HClO.
(3)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器,盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
(4)现有实验后的HCl与CaCl2的混合溶液,为了分析混合溶液中HCl和CaCl2的质量分数,设计了如图实验方案:
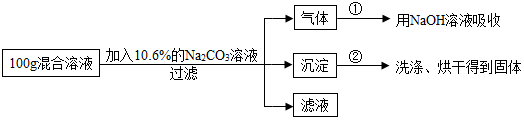
【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
(1)m=200.
(2)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为多少?(不考虑过滤中的损失,计算结果保留到小数点后一位.)
(1)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小 (填“增大”或“减小”或“不变”).
(2)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2+2HCl=CaCl2+2HClO.
(3)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器,盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中, 加入足量的稀盐酸,塞上带导管的单孔塞,把导管插入另一盛有澄清石灰水的试管中 | 有气体产生, 气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后试管中加少量 品红溶液 | 品红溶液褪色 |

【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
(1)m=200.
(2)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为多少?(不考虑过滤中的损失,计算结果保留到小数点后一位.)
20.甲、乙、丙三种金属,分别投入稀盐酸中,只有甲能产生气体;将乙投入丙的硝酸盐溶液中,无现象.则甲、乙、丙三种金属的活动性顺序为( )
| A. | 甲>乙>丙 | B. | 乙>甲>丙 | C. | 丙>乙>甲 | D. | 甲>丙>乙 |
19.下列粗盐提纯所用的仪器中不属于玻璃仪器的是( )
0 156699 156707 156713 156717 156723 156725 156729 156735 156737 156743 156749 156753 156755 156759 156765 156767 156773 156777 156779 156783 156785 156789 156791 156793 156794 156795 156797 156798 156799 156801 156803 156807 156809 156813 156815 156819 156825 156827 156833 156837 156839 156843 156849 156855 156857 156863 156867 156869 156875 156879 156885 156893 211419
| A. | 玻璃棒 | B. | 漏斗 | C. | 蒸发皿 | D. | 烧杯 |