9.下列各组物质中按酸、碱、盐、氧化物的顺序排列的是( )
| A. | H2SO4、Na2O、MgCl2、CO | B. | NaHCO3、Ba(OH)2、NaCl、O2 | ||
| C. | HNO3、KOH、Na2CO3、MnO2 | D. | HCl、NaOH、K2CO3、KMnO4 |
6. 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示.下列说法中正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示.下列说法中正确的是( )
 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示.下列说法中正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示.下列说法中正确的是( )| A. | 该反应为分解反应 | |
| B. | 丙一定为该反应的催化剂 | |
| C. | 该反应中,乙、丁的质量变化之比为7:5 | |
| D. | 该反应中,甲、乙的质量变化之比为4:5 |
5.下列实验现象的描述不正确的是( )
| A. | 在汽油中加入少量高锰酸钾,高锰酸钾溶解呈紫红色 | |
| B. | 硫在氧气中燃烧产生蓝紫色火焰 | |
| C. | 加热饱和石灰水,出现白色浑浊 | |
| D. | 把洁净的铜丝放入硝酸银溶液中,溶液由无色逐渐变蓝色 |
2.菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某班学习小组进行了实验探究,取10g菱镁矿样品,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如表:
注:菱镁矿中的杂质不溶于水,不与酸发生反应、不含镁元素.请回答:
(1)10g菱镁矿与稀硫酸完全反应,生成气体的质量为4.4g.
(2)计算该菱镁矿中镁元素的质量分数.(写出计算过程)
(3)吸收反应生成的气体,不用石灰水的原因是氢氧化钙的溶解度常温下很小,所以等质量的石灰水和氢氧化钠溶液中,氢氧化钠溶液的质量分数更大,可吸收更多的二氧化碳.
0 155794 155802 155808 155812 155818 155820 155824 155830 155832 155838 155844 155848 155850 155854 155860 155862 155868 155872 155874 155878 155880 155884 155886 155888 155889 155890 155892 155893 155894 155896 155898 155902 155904 155908 155910 155914 155920 155922 155928 155932 155934 155938 155944 155950 155952 155958 155962 155964 155970 155974 155980 155988 211419
| 分组 | 1 | 2 | 3 | 4 |
| 加入H2SO4溶液质量/g | 50 | 100 | 150 | 200 |
| NaOH溶液增加质量/g | 2.2 | 4.4 | 4.4 | 4.4 |
(1)10g菱镁矿与稀硫酸完全反应,生成气体的质量为4.4g.
(2)计算该菱镁矿中镁元素的质量分数.(写出计算过程)
(3)吸收反应生成的气体,不用石灰水的原因是氢氧化钙的溶解度常温下很小,所以等质量的石灰水和氢氧化钠溶液中,氢氧化钠溶液的质量分数更大,可吸收更多的二氧化碳.
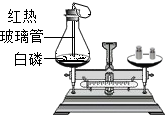 如图是白磷燃烧前后质量测定的实验装置图,请你分析并回答下列问题:
如图是白磷燃烧前后质量测定的实验装置图,请你分析并回答下列问题: 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: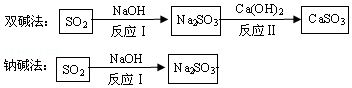
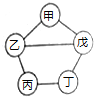 如图所示,甲、乙、丙、丁、戊五种物质分别是铁、盐酸、氢氧化钙、硫酸铜、碳酸钠中的一种,连线两端的物质间能发生化学反应,甲与戊反应产生的气体能使澄清石灰水变浑浊.请回答.
如图所示,甲、乙、丙、丁、戊五种物质分别是铁、盐酸、氢氧化钙、硫酸铜、碳酸钠中的一种,连线两端的物质间能发生化学反应,甲与戊反应产生的气体能使澄清石灰水变浑浊.请回答.