18.用下列实验方案及所选玻璃仪器就能实现相应目的是( )
| 实验目的 | 实验方案 | 所选玻璃仪器 | |
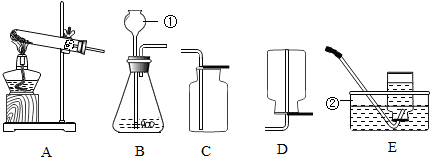
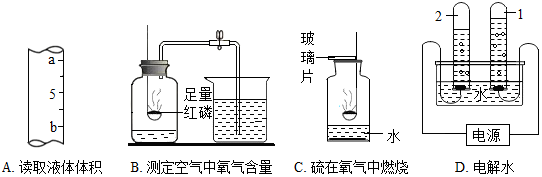
| A | 证明分子之间有间隔 | 把一滴红墨水滴到一杯清水中 | 烧杯 |
| B | 证明CO2与H2O反应化学反应 | 把CO2通入水中,一会儿再往混合液中滴加紫色石蕊溶液 | 导管、烧杯、滴管 |
| C | 配制50g4%的氯化钠溶液 | 用天平称量2g氯化钠固体,再用50mL的量筒量取48mL的水,然后混合溶解 | 烧杯、滴管、量筒 |
| D | 稀释浓硫酸 | 把水倒入到浓硫酸中 | 烧杯、玻璃棒 |
| A. | A | B. | B | C. | C | D. | D |
16.根据物质的特性,运用实验的方法,可以鉴别末知的物质.现有一包可能含有碳酸钠、硫酸钠和硝酸钡的固体样品(至少含有两种物质).请你设计实验方案,探究其成分,并将相关内容填在下表.(不一定填满,也可以补充)限选试剂:稀HNO3、BaCl2溶液、蒸馏水
| 实验操作 | 预期现象与结论 |
| 步骤1:取少量固体样品于 试管中,加入足量的蒸馏水, 充分振荡. | 若得到澄清溶液,说明样品中含有碳酸钠和硫酸钠; 若产生白色沉淀,则继续进行实验. |
步骤2:往步骤1的试管中继续加入足量的稀HNO3 | 若沉淀完全溶解,说明样品中含有硝酸钡和碳酸钠; 若沉淀完全不溶解,说明样品中含有硝酸钡和硫酸钠; 若沉淀部分溶解且有气泡产生,说明样品中含有碳酸钠、硫酸钠和硝酸钡 |
14.同学们利用“硫酸、硝酸钡、氢氧化钠、碳酸钾”四种物质的溶液进行探究学习,完成下列各问:
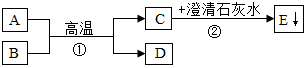
【实验探究】A、B、C、D四组同学分别进行了图1实验:
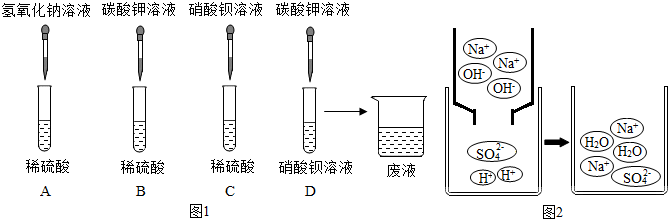
写出下列的两个方程式:
?A中的反应2NaOH+H2SO4=Na2SO4+2H2O
?B中的反应K2CO3+H2SO4═K2SO4+H2O+CO2↑
【挖掘实质】图2是A组反应的微观过程示意图该化学反应的实质可以表示为H++OH-=H2O,完成试验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀,向无色溶液中滴加紫色石蕊试剂,变为红色.
(1)溶液中的白色沉淀一定是硫酸钡,理由是无色溶液滴加紫色石蕊试剂,变为红色,说明得到无色溶液为酸性,酸过量,亦说明白色沉淀不能溶于酸
(2)废液中一定不含有的离子是OH-和CO32-
(3)为了验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证
0 155009 155017 155023 155027 155033 155035 155039 155045 155047 155053 155059 155063 155065 155069 155075 155077 155083 155087 155089 155093 155095 155099 155101 155103 155104 155105 155107 155108 155109 155111 155113 155117 155119 155123 155125 155129 155135 155137 155143 155147 155149 155153 155159 155165 155167 155173 155177 155179 155185 155189 155195 155203 211419
【实验探究】A、B、C、D四组同学分别进行了图1实验:

写出下列的两个方程式:
?A中的反应2NaOH+H2SO4=Na2SO4+2H2O
?B中的反应K2CO3+H2SO4═K2SO4+H2O+CO2↑
【挖掘实质】图2是A组反应的微观过程示意图该化学反应的实质可以表示为H++OH-=H2O,完成试验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀,向无色溶液中滴加紫色石蕊试剂,变为红色.
(1)溶液中的白色沉淀一定是硫酸钡,理由是无色溶液滴加紫色石蕊试剂,变为红色,说明得到无色溶液为酸性,酸过量,亦说明白色沉淀不能溶于酸
(2)废液中一定不含有的离子是OH-和CO32-
(3)为了验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证
| 溶液中可能含有的离子 | 实验步骤 | 实验现象 | 实验结论 |
| ?①可能含有Ba2+ | ②取滤液滴加硫酸钠溶液 | 现象明显 | 含有该离子 |