9.下列关于氧气的说法错误的是( )
| A. | 氧气的体积约占空气体积的21% | |
| B. | 空气中氧气主要来自植物的光合作用 | |
| C. | 利用氧炔焰割断金属,说明氧气具有可燃性 | |
| D. | 工业上可用分离空气法制氧气 |
8.在古代,我国化学工艺制造在世界举世闻名的是( )
| A. | 玻璃 | B. | 光导纤维 | C. | 瓷器 | D. | 不锈钢 |
7.已知X和Y可发生化合反应,现进行了两次实验,测得数据如表所示:
若将①和②的反应混合,最多可生成产物( )
| 实验序号 | 反应物的质量/g | 产物的质量/g | |
| X | Y | ||
| ① | 7.2 | 1.6 | 8.0 |
| ② | 8.0 | 2.4 | 10.0 |
| A. | 18.0g | B. | 18.8g | C. | 19.0g | D. | 19.2g |
5.实验室制取二氧化碳的方法是:石灰石与稀盐酸反应.某化学兴趣小组同学对石灰石与稀盐酸反应后所得的溶液进行探究,如下:
【问题】:溶液中含有哪些溶质?
【猜想】:①可能含有:CaCl2、HCl ②可能含有CaCl2 CaCO3 ③可能只含有CaCl2该小组同学小林认为猜想②不合理;理由是碳酸钙难溶于水.
【实验】:
用方程式表示上述实验过程中发生的反应Na2CO3+2HCl=2NaCl+H2O+CO2↑.
【问题】:溶液中含有哪些溶质?
【猜想】:①可能含有:CaCl2、HCl ②可能含有CaCl2 CaCO3 ③可能只含有CaCl2该小组同学小林认为猜想②不合理;理由是碳酸钙难溶于水.
【实验】:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于一只试管中,滴加过量的碳酸钠溶液. | 有气泡产生 | 猜想①成立 |
3.红枣包装中常使用一种“504双吸剂”,其成分为铁粉、生石灰等.实验小组同学对一包使用过的“504双吸剂”进行了如下探究.
【提出问题】久置后,固体的成分是什么?
【查阅资料】(1)铁与氯化铁溶液在常温下发生反应生成氯化亚铁;
(2)铁可以被磁铁吸引,Fe2O3、CaO、Ca(OH)2、CaCO3均不被磁铁吸引.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究】实验方案一:
【实验分析】
(1)酚酞溶液颜色发生改变是因为溶液中含有OH-(填离子符号)离子;甲同学认为通过实验不能得出一定含Ca(OH)2的结论,理由是CaO+H2O=Ca(OH)2(用化学方程式表示),该反应的基本类型为化合反应.
(2)乙同学认为通过实验不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.她设计实验方案二继续进行探究.
实验方案二:
【实验分析】
(1)④中发生的两个复分解反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑、Fe2O3+6HCl=2FeCl3+3H2O.
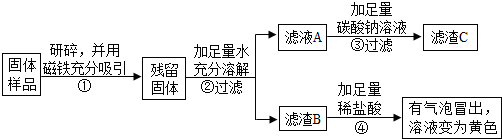
(2)通过实验二可确定固体样品中一定还含有Fe2O3.
(3)为确定固体样品中是否含有氢氧化钙,实验小组同学又经过实验测得上述残留固体总质量为1.66g,滤渣B质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,可判断实验小组同学们的猜想成立(填“成立”或“不成立”).
【实验反思】探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂紫色石蕊试液.
【提出问题】久置后,固体的成分是什么?
【查阅资料】(1)铁与氯化铁溶液在常温下发生反应生成氯化亚铁;
(2)铁可以被磁铁吸引,Fe2O3、CaO、Ca(OH)2、CaCO3均不被磁铁吸引.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究】实验方案一:
| 实验操作 | 实验现象 | 实验结论 |
| (1)取适量固体放于烧杯中,加足量蒸馏水溶解,静置后取上层清液,滴加无色酚酞溶液 | 固体溶解时烧杯外壁发烫 | 固体中一定含有①氧化钙 |
| 酚酞溶液变为②红色 | 固体中一定含有氢氧化钙 | |
| (2)另取少量固体放于试管中,滴加足量的盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有③铁,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有④CaCO3 |
(1)酚酞溶液颜色发生改变是因为溶液中含有OH-(填离子符号)离子;甲同学认为通过实验不能得出一定含Ca(OH)2的结论,理由是CaO+H2O=Ca(OH)2(用化学方程式表示),该反应的基本类型为化合反应.
(2)乙同学认为通过实验不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.她设计实验方案二继续进行探究.
实验方案二:
【实验分析】
(1)④中发生的两个复分解反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑、Fe2O3+6HCl=2FeCl3+3H2O.

(2)通过实验二可确定固体样品中一定还含有Fe2O3.
(3)为确定固体样品中是否含有氢氧化钙,实验小组同学又经过实验测得上述残留固体总质量为1.66g,滤渣B质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,可判断实验小组同学们的猜想成立(填“成立”或“不成立”).
【实验反思】探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂紫色石蕊试液.
2.“过氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应放出氧气.实验室有一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分及其质量.
【提出问题】变质的过氧化钠粉末中有哪些成分,它们的质量是多少?
【查阅资料】
①2Na2O2+2H2O═4NaOH+O2↑ 2Na2O2+2CO2═2Na2CO3+O2
②碳酸钠溶液显碱性,氯化钙溶液显中性.
【猜想与假设】
(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是Na2O2和Na2CO3的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物
…
【设计实施方案】
【解释与结论】同学们经过认真分析,得出了以下结论.
粉末中含有的成分及质量
【反思与评价】
(1)实验室在保存过氧化钠时应注意密封保存.
(2)有同学提出把第②步实验中足量的石灰水改为足量氯化钙溶液,至沉淀不再生成时过滤,向滤液中滴加无色酚酞试液,若液体变红,则证明原粉末中有NaOH.你认为该方案是否合理并说明理由不合理,因为过氧化钠与水反应能生成氢氧化钠,不能判断原来是否存在氢氧化钠..
【提出问题】变质的过氧化钠粉末中有哪些成分,它们的质量是多少?
【查阅资料】
①2Na2O2+2H2O═4NaOH+O2↑ 2Na2O2+2CO2═2Na2CO3+O2
②碳酸钠溶液显碱性,氯化钙溶液显中性.
【猜想与假设】
(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是Na2O2和Na2CO3的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物
…
【设计实施方案】
| 实验步骤 | 实验现象 |
| ①取3.00g变质粉末于一支大试管内,加入适量的水,共收集到0.32g气体,然后用带火星木条检验生成的气体. | 固体完全溶解,带火星木条复燃, 不用填 |
| ②继续向上述试管中加入足量的石灰水,充分反应. | 有白色沉淀生成 |
| ③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g. |
粉末中含有的成分及质量
| Na2O2 | NaOH | Na2CO3 | |
| 成分(填“有”或“没有”) | |||
| 质量(g) |
(1)实验室在保存过氧化钠时应注意密封保存.
(2)有同学提出把第②步实验中足量的石灰水改为足量氯化钙溶液,至沉淀不再生成时过滤,向滤液中滴加无色酚酞试液,若液体变红,则证明原粉末中有NaOH.你认为该方案是否合理并说明理由不合理,因为过氧化钠与水反应能生成氢氧化钠,不能判断原来是否存在氢氧化钠..
8.下列化学反应与反应类型不相符的是( )
0 154940 154948 154954 154958 154964 154966 154970 154976 154978 154984 154990 154994 154996 155000 155006 155008 155014 155018 155020 155024 155026 155030 155032 155034 155035 155036 155038 155039 155040 155042 155044 155048 155050 155054 155056 155060 155066 155068 155074 155078 155080 155084 155090 155096 155098 155104 155108 155110 155116 155120 155126 155134 211419
| A. | NH4HCO3═NH3↑+CO2↑+H2O(分解反应) | B. | CuO+H2SO4═CuSO4+H2O(中和反应) | ||
| C. | 2Na+2H2O═2NaOH+H2↑(置换反应) | D. | CaO+H2O═Ca(OH)2(化合反应) |
 东海原甲藻(简称甲藻)是我国东海引发赤潮的藻种之一,研究甲藻光合作用的特点可为认识赤潮发生机理提供重要信息.某研究小组探究pH对甲藻光合作用的影响,设计了以下实验:将生长旺盛的甲藻等量分成5组培养,各组藻液初始状态的pH分别设定为6.0、7.0、8.0、9.0、10.0,在黑暗中放置12h,然后在适宜光照等相同条件下培养,每小时测定各组氧气释放量并计算平均值,将实验结果绘制成右图.
东海原甲藻(简称甲藻)是我国东海引发赤潮的藻种之一,研究甲藻光合作用的特点可为认识赤潮发生机理提供重要信息.某研究小组探究pH对甲藻光合作用的影响,设计了以下实验:将生长旺盛的甲藻等量分成5组培养,各组藻液初始状态的pH分别设定为6.0、7.0、8.0、9.0、10.0,在黑暗中放置12h,然后在适宜光照等相同条件下培养,每小时测定各组氧气释放量并计算平均值,将实验结果绘制成右图.
