9.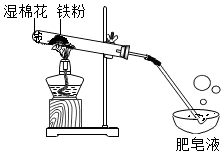 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
(1)探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是H2.
(2)探究试管中剩余固体成分是什么?
【查阅资料】
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是Fe3O4.
【实验探究】
 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.(1)探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是H2.
(2)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 能否与盐酸反应 | 能 | 能 | 能 |
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是Fe3O4.
| 实验操作 | 实验现象及结论 |
| 取少量黑色固体于试管中,加入足量的稀盐酸. | 若固体不溶解,也没有气泡冒出,剩余固体是Fe3O4.若固体部分溶解,有气泡冒出,剩余固体是Fe与Fe3O4. |
8.新闻中报道了某家长带小孩在下水道井盖小孔上点燃鞭炮发生爆炸.现要探究某下水道的可燃性气体成分:
[猜想](I)含可燃性气体CO; (II)含可燃性气体CH4; (III)含可燃性气体CO和CH4.
[收集气体]用大的可乐塑料瓶装满水,打开瓶盖用绳子吊入下水道中,用铁钩将矿泉水瓶倒转,
使瓶内水倒完,将瓶提到井口迅速盖好瓶备用.
[进行实验]
[作出判断]根据上述实验现象,甲同学认为猜想III正确;而乙同学认为甲的判断不严谨.因为猜想Ⅱ也有相同的现象.如需进一步确认还应检验CO的存在,其方法是将气体通过炽热的氧化铜粉末,看粉末是否变红.
[拓展]若需要工人进入下水道清理淤泥,打开下水道井盖后应首先进行的操作是通风.
[猜想](I)含可燃性气体CO; (II)含可燃性气体CH4; (III)含可燃性气体CO和CH4.
[收集气体]用大的可乐塑料瓶装满水,打开瓶盖用绳子吊入下水道中,用铁钩将矿泉水瓶倒转,
使瓶内水倒完,将瓶提到井口迅速盖好瓶备用.
[进行实验]
| 步骤 | 实验搡作 | 实验现象 | 结论 |
| (1) | 导出瓶中气体,通过装有 氢氧化钠溶液的洗气瓶. | 目的是除CO2等 酸性气体. | |
| (2) | 再通过装有浓硫酸的洗气瓶. | 目的是除去H2O. | |
| (3) | 将步骤(2)的气体导出点燃; ①用吸附少量无水硫酸铜粉末的石棉贴在小烧杯内壁,再把小烧杯斜罩于火焰上方; ②用内壁粘有澄清石灰水的小烧杯罩于火焰上方. | ?无水硫酸铜 变蓝; ?烧杯内壁变浑浊. | ?证明有H2O生成; ?证明有CO2生成. |
[拓展]若需要工人进入下水道清理淤泥,打开下水道井盖后应首先进行的操作是通风.
7.纯碱广泛应用于工业生产.现取某纯碱样品(含氯化钠杂质),为确定其中碳酸钠的质量分数,甲、乙两个研究小组分别设计如下实验装置进行探究.
(1)同学们先在实验室把98%的浓硫酸稀释成9.8%的稀硫酸200g,并用其和纯碱样品反应测定碳酸钠的质量分数.
①配制稀硫酸的步骤有:计算、称量、溶解、冷却至室温装瓶并贴上标签,其中用到的下班仪器有量筒、烧杯和玻璃棒.
②需加入水的体积为180mL(水的密度近似看作1g/cm3).
(2)甲组同学采用图1装置,通过测量生成CO2的体积测定碳酸钠的质量分数,(不考虑植物油中溶解CO2产生的影响,碱石灰是氢氧化钠固体与生石灰的混合物).

①若其他操作均正确,仅因下列因素可使碳酸钠的质量分数测定结果偏大的是a(填字母序号);
a.反应后俯视量筒读数b.样品未反应完全即停止验
c.B中未装满液体
②甲组同学测得3组数据如表所示.取3组数据的平均值得到CO2的体积为22.4mL,又知常温常压下CO2的密度为1.964g/L,据此计算碳酸钠的质量分数为53%.
(3)乙组同学采用图2装置,通过测量装置D在反应前后的质量差来测定碳酸钠的质量分数.
①若其他操作均正确,结果仍然偏高的可能原因是碱石灰具有吸水性,若要测定结果列准确需要将装置(如图3所示)接入上述装置的(填编号)A、B之间,装置图3中的液体名称是浓硫酸.
②乙组同学们改进实验装置后(改进装置图略),取21g该纯碱样品加入9.8%的稀硫酸至不再产生气泡,测得反应前后装置D增加了4.4g,求消耗稀硫酸的质量100g(写出计算过程).
(1)同学们先在实验室把98%的浓硫酸稀释成9.8%的稀硫酸200g,并用其和纯碱样品反应测定碳酸钠的质量分数.
①配制稀硫酸的步骤有:计算、称量、溶解、冷却至室温装瓶并贴上标签,其中用到的下班仪器有量筒、烧杯和玻璃棒.
②需加入水的体积为180mL(水的密度近似看作1g/cm3).
(2)甲组同学采用图1装置,通过测量生成CO2的体积测定碳酸钠的质量分数,(不考虑植物油中溶解CO2产生的影响,碱石灰是氢氧化钠固体与生石灰的混合物).

①若其他操作均正确,仅因下列因素可使碳酸钠的质量分数测定结果偏大的是a(填字母序号);
a.反应后俯视量筒读数b.样品未反应完全即停止验
c.B中未装满液体
②甲组同学测得3组数据如表所示.取3组数据的平均值得到CO2的体积为22.4mL,又知常温常压下CO2的密度为1.964g/L,据此计算碳酸钠的质量分数为53%.
| 组别 | 样品质量 | CO2体积 |
| 第1组 | 0.20g | 22.3mL |
| 第2组 | 0.20g | 22.4mL |
| 第3组 | 0.20g | 22.5mL |
①若其他操作均正确,结果仍然偏高的可能原因是碱石灰具有吸水性,若要测定结果列准确需要将装置(如图3所示)接入上述装置的(填编号)A、B之间,装置图3中的液体名称是浓硫酸.
②乙组同学们改进实验装置后(改进装置图略),取21g该纯碱样品加入9.8%的稀硫酸至不再产生气泡,测得反应前后装置D增加了4.4g,求消耗稀硫酸的质量100g(写出计算过程).
6.学习了金属的化学性质后,某兴趣小组进行了如下实验:将足量镁条加入到氯化铁溶液中,观察到镁条表面有气泡产生,一段时间后,有黑色固体粉末生成.
【提出问题】产生气体是什么物质?
【作出猜想】猜想一:可能是氧气;猜想二:可能是氢气;猜想三:可能是二氧化碳.
【交流讨论】(1)大家思考后,一致认为猜想三不合理,其理由是反应物中不含碳元素,不符合质量守恒定律.
【实验与结论】
【继续探究】用pH试纸测得氯化铁溶液pH约为2,说明氯化铁溶液呈(4)酸性(选填“酸性”、“碱性”或“中性”).
【提出问题】产生气体是什么物质?
【作出猜想】猜想一:可能是氧气;猜想二:可能是氢气;猜想三:可能是二氧化碳.
【交流讨论】(1)大家思考后,一致认为猜想三不合理,其理由是反应物中不含碳元素,不符合质量守恒定律.
【实验与结论】
| 实验步骤 | 现象 | 结论 |
| ①先用试管收集该气体,再将带火星的木条伸入试管 | (2)带火星的木条没有复燃 | 猜想一不成立 |
| ②用尖嘴导管将气体导出并引燃,同时在上方放一块干冷的玻璃片 | 该气体能燃烧,且玻璃片上有 (3)水雾出现 | 猜想二成立 |
5.甲乙小组按如图1所示实验探究蜡烛的燃烧产物,获得了不同的实验现象.
甲组:烧杯内壁有无色液滴
乙组:烧杯内壁有无色液滴,烧杯底部附着有黑色固体
【提出问题】同学们查阅教材实验,得知无色液滴是水,
但黑色固体是什么呢?
【提出猜想】黑色固体是碳
【实验验证】利用如图2所示装置,甲,乙小组的同学分别设计了以下方案进行验证.
【分析与结论】
(1)实验结束时,停止通入气体,后续实验操作顺序应是BA(填字母序号).
A.熄灭酒精灯,停止加热 B.将试管b移走
(2)b中的实验现象说明黑色固体燃烧生成了二氧化碳,由此可推断猜想正确,理由是化学反应前后元素种类不变,二氧化碳的碳元素一定来自黑色固体.
【实验反思】
(1)进一步实验发现,罩在火焰上方的烧杯位置越低,产生黑色固体越多.查阅资料可知:蜡烛+氧气(足量)→二氧化碳+水;蜡烛+氧气(少量)→一氧化碳+水;…(反应条件均为“点燃”)由此推测乙组实验产生黑色固体的原因是烧杯位置降低使氧气的量减少,氧气的量少到一定程度时蜡烛和氧气反应产生黑色固体碳.
(2)甲、乙小组最终证明了蜡烛中一定含有C(填字母序号).
A.碳、氢和氧三种元素B.碳和氧两种元素C.碳和氢两种元素
(3)石蜡的主要成分为C25H52,写出石蜡完全燃烧的符号表达式:C25H52+38O2$\frac{\underline{\;点燃\;}}{\;}$25CO2+26H2O.
【实验拓展】
小组同学以“研究不同高度的蜡烛哪只先熄灭”为课题设计了以下实验:
查阅资料:二氧化碳的密度比空气大
实验步骤:①点燃两支高低不同的蜡烛②用一只大烧杯同时倒扣在两支燃烧的蜡烛上,用秒表计时.③重复实验四次,实验记录如下:实验结论:分析表中数据,你得到的结论是在同样大小的倒扣的烧杯中,较高的蜡烛燃烧的时间短;
分析反思:二氧化碳的密度比空气大,为什么实验结果与我们的猜想不符呢?通过讨论,同学们一致认为原因可能是燃烧产生的二氧化碳温度较高,密度较小,不易沉降到烧杯底部,反而聚集到烧杯的上部,致使高蜡烛先熄灭.学以致用:当室内发生火灾,应用湿毛巾捂住口鼻,并伏低(填“直立”或“伏低”)身子前行寻找逃生出口.

甲组:烧杯内壁有无色液滴
乙组:烧杯内壁有无色液滴,烧杯底部附着有黑色固体
【提出问题】同学们查阅教材实验,得知无色液滴是水,
但黑色固体是什么呢?
【提出猜想】黑色固体是碳
【实验验证】利用如图2所示装置,甲,乙小组的同学分别设计了以下方案进行验证.
| 实验操作 | 实验现象 | |
| 甲组 | 取少量该黑色固体于a中,通入空气,点燃酒精灯加热. | 黑色固体燃烧,发出红光,b中溶液变浑浊. |
| 乙组 | 取少量该黑色固体于a中,通入氧气(或O2),点燃酒精灯加热. | 黑色固体剧烈燃烧,发出白光,b中溶液变浑浊. |
(1)实验结束时,停止通入气体,后续实验操作顺序应是BA(填字母序号).
A.熄灭酒精灯,停止加热 B.将试管b移走
(2)b中的实验现象说明黑色固体燃烧生成了二氧化碳,由此可推断猜想正确,理由是化学反应前后元素种类不变,二氧化碳的碳元素一定来自黑色固体.
【实验反思】
(1)进一步实验发现,罩在火焰上方的烧杯位置越低,产生黑色固体越多.查阅资料可知:蜡烛+氧气(足量)→二氧化碳+水;蜡烛+氧气(少量)→一氧化碳+水;…(反应条件均为“点燃”)由此推测乙组实验产生黑色固体的原因是烧杯位置降低使氧气的量减少,氧气的量少到一定程度时蜡烛和氧气反应产生黑色固体碳.
(2)甲、乙小组最终证明了蜡烛中一定含有C(填字母序号).
A.碳、氢和氧三种元素B.碳和氧两种元素C.碳和氢两种元素
(3)石蜡的主要成分为C25H52,写出石蜡完全燃烧的符号表达式:C25H52+38O2$\frac{\underline{\;点燃\;}}{\;}$25CO2+26H2O.
【实验拓展】
小组同学以“研究不同高度的蜡烛哪只先熄灭”为课题设计了以下实验:
查阅资料:二氧化碳的密度比空气大
实验步骤:①点燃两支高低不同的蜡烛②用一只大烧杯同时倒扣在两支燃烧的蜡烛上,用秒表计时.③重复实验四次,实验记录如下:实验结论:分析表中数据,你得到的结论是在同样大小的倒扣的烧杯中,较高的蜡烛燃烧的时间短;
| 实验次数 | 高蜡烛燃烧的时间 | 矮蜡烛燃烧的时间 |
| 第一次 | 23秒18 | 26秒06 |
| 第二次 | 23秒19 | 24秒94 |
| 第三次 | 20秒02 | 21秒45 |
| 第四次 | 15秒16 | 19秒10 |
4.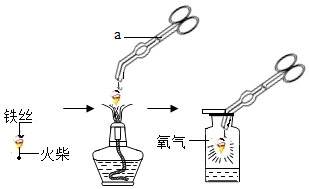 实验是研究化学的基本手段.在实验室,小冬同学进行了“铁在氧气中燃烧”的实验,请回答下列问题:
实验是研究化学的基本手段.在实验室,小冬同学进行了“铁在氧气中燃烧”的实验,请回答下列问题:
(1)图中仪器a的名称是坩埚钳,实验中火柴的作用是引燃铁丝;写出该反应的化学方程式:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;集气瓶中装少量水的目的是防止溅落的熔化物炸裂瓶底.
(2)做完实验后,小冬同学有两个疑惑不解的问题,于是她进行了以下途径活动,请你一同参与.
【问题1】铁燃烧时溅落下来的黑色物质中还有没有铁呢?
【查阅资料1】
①自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
②铁的氧化物均能溶于稀盐酸和稀硫酸.
【实验探究】
将冷却后的黑色物质碾碎,装入试管,加入稀盐酸溶液,观察到的现象是固体逐渐溶解,表面有气泡产生,说明铁燃烧时溅落下来的黑色物质中含有铁.
【问题2】铁燃烧的产物为什么不是Fe2O3呢?
【查阅资料2】
①Fe3O4和Fe2O3的分解温度、铁的熔点见表;
②Fe2O3高温时分解成Fe3O4.
【理论探讨】
根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在l535℃~l538℃之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产生是Fe3O4.
【拓展延伸】:
(1)Fe2O3高温时会分解成Fe3O4和一种气体,请写出此反应的化学方程式6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑;
(2)有些超市的食品密封包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色变为红色,就说明包装盒破损进气,这样售货员就能及时发现并处理.
 实验是研究化学的基本手段.在实验室,小冬同学进行了“铁在氧气中燃烧”的实验,请回答下列问题:
实验是研究化学的基本手段.在实验室,小冬同学进行了“铁在氧气中燃烧”的实验,请回答下列问题:(1)图中仪器a的名称是坩埚钳,实验中火柴的作用是引燃铁丝;写出该反应的化学方程式:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;集气瓶中装少量水的目的是防止溅落的熔化物炸裂瓶底.
(2)做完实验后,小冬同学有两个疑惑不解的问题,于是她进行了以下途径活动,请你一同参与.
【问题1】铁燃烧时溅落下来的黑色物质中还有没有铁呢?
【查阅资料1】
①自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
②铁的氧化物均能溶于稀盐酸和稀硫酸.
【实验探究】
将冷却后的黑色物质碾碎,装入试管,加入稀盐酸溶液,观察到的现象是固体逐渐溶解,表面有气泡产生,说明铁燃烧时溅落下来的黑色物质中含有铁.
【问题2】铁燃烧的产物为什么不是Fe2O3呢?
【查阅资料2】
①Fe3O4和Fe2O3的分解温度、铁的熔点见表;
②Fe2O3高温时分解成Fe3O4.
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在l535℃~l538℃之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产生是Fe3O4.
【拓展延伸】:
(1)Fe2O3高温时会分解成Fe3O4和一种气体,请写出此反应的化学方程式6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑;
(2)有些超市的食品密封包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色变为红色,就说明包装盒破损进气,这样售货员就能及时发现并处理.
3.如表列出了除去物质中所含少量杂质的方法,其中错误的是( )
0 154827 154835 154841 154845 154851 154853 154857 154863 154865 154871 154877 154881 154883 154887 154893 154895 154901 154905 154907 154911 154913 154917 154919 154921 154922 154923 154925 154926 154927 154929 154931 154935 154937 154941 154943 154947 154953 154955 154961 154965 154967 154971 154977 154983 154985 154991 154995 154997 155003 155007 155013 155021 211419
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | CO2 | CO | 点燃 |
| B | MnO2粉 | C粉 | 在空气中充分灼烧 |
| C | FeSO4溶液 | CuSO4溶液 | 加入足量的铁粉,过滤 |
| D | NaCl固体 | 泥沙 | 溶解、过滤 |
| A. | A | B. | B | C. | C | D. | D |

 ”表示有可循环利用的物质)
”表示有可循环利用的物质)