6.为测定石灰石中碳酸钙的纯度,取是会是样品与足量的稀盐酸在烧杯中反应(杂质不反应也不溶于水),有关数据如表.
请计算:
(1)根据质量守恒定律,反应生成CO2的质量为3.3g.
(2)该石灰石样品中碳酸钙的质量分数.(写出计算过程)
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 153.4克 | 10g | 160.1g | |
(1)根据质量守恒定律,反应生成CO2的质量为3.3g.
(2)该石灰石样品中碳酸钙的质量分数.(写出计算过程)
4.a、b两种物质的溶解度曲线如图所示,下列说法不正确的是( )


| A. | 将t1℃时b的饱和溶液加水可变为不饱和溶液 | |
| B. | 将t2℃时a的饱和溶液降温至t1℃,溶液质量不变 | |
| C. | t2℃时,a物质的溶解度大于b物质的溶解度 | |
| D. | 当a物质中含少量b物质时,可用冷却热饱和溶液的方法提纯a物质 |
3.下列依据实验目的所设计的实验操作中,正确的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 检验二氧化碳 | 将二氧化碳通入紫色石蕊溶液中 |
| B | 鉴别氢气、一氧化碳和甲烷 | 观察气体的颜色 |
| C | 除去FeCl2溶液中的CuCl2 | 加入过量铁粉,充分反应后过滤 |
| D | 除去CO2中的少量CO | 向混合气体中鼓入过量氧气,点燃 |
| A. | A | B. | B | C. | C | D. | D |
2.下列坐标图分别表示实验过程中某些量的变化,其中正确的是( )
| A. |  一定温度下,向硝酸钾溶液中加入硝酸钾固体 | |
| B. |  将水通电一段时间 | |
| C. |  将等质量的镁片和铁片投入到足量的稀H2SO4中 | |
| D. |  用等质量、等浓度的过氧化氢溶液分别制取氧气 |
1.下列实验现象描述正确的是( )
| A. | 氢气在空气中燃烧时,产生淡蓝色火焰 | |
| B. | 细铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 | |
| C. | 用力振荡盛有水和植物油的试管,得到澄清透明的液体 | |
| D. | 把银片插入硫酸铜溶液中,一段时间后取出,银片表面有一层红色物质 |
20.下列归纳中,完全正确的是( )
| A.性质与用途 | B.实验操作 |
| ①氦气的化学性质稳定-食品防腐 ②稀有气体通电时能发出不同颜色的光-霓虹灯 ③氦气的密度很小且稳定-气球 | ①金属与酸反应前应先用砂纸打磨除去表面的氧化膜 ②用高锰酸钾制取氧气实验完毕,先熄灭酒精灯,再把导管移出水面 ③H2还原CuO实验应先通H2,再加热 |
| C.能量变化 | D.资源利用 |
| ①在化学反应中只有燃烧才能放出热量 ②煤燃烧是将化学能转化为内能 ③高温时,碳可以还原CO2 | ①废旧电池回收 ②提倡使用乙醇汽油 ③实验后剩余药品放回原瓶 |
| A. | A | B. | B | C. | C | D. | D |
19.我国科学家屠呦呦因为“发现青蒿素(化学式为C15H22O5)”-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而获诺贝尔奖.下列关于青蒿素的说法不正确的是( )
| A. | 一个青蒿素分子中含有42个原子 | |
| B. | 青蒿素的相对分子质量为282 | |
| C. | 28.2g青蒿素中含碳量为18g | |
| D. | 青蒿素中C、H、O三种元素的质量比为15:22:5 |
18.甲、乙两个化学反应的微观过程如图,下列说法正确的是( )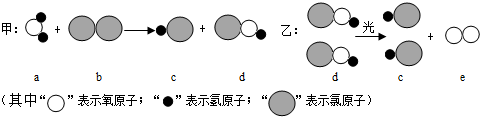
0 154048 154056 154062 154066 154072 154074 154078 154084 154086 154092 154098 154102 154104 154108 154114 154116 154122 154126 154128 154132 154134 154138 154140 154142 154143 154144 154146 154147 154148 154150 154152 154156 154158 154162 154164 154168 154174 154176 154182 154186 154188 154192 154198 154204 154206 154212 154216 154218 154224 154228 154234 154242 211419

| A. | 如图中包含两种单质和两种氧化物 | |
| B. | 气体b能用排水法收集 | |
| C. | 甲、乙两个化学反应中原子的种类和个数不变 | |
| D. | 乙反应的化学方程式为2HClO=2HCl+O2 |
