17.实验室里用过氧化氢溶液与二氧化锰制取氧气,相关数据如表:
请计算:
Ⅰ.制得氧气的物质的量为0.1mol.
Ⅱ.该实验中反应的过氧化氢的物质的量(根据化学方程式计算).
Ⅲ.理论上该实验所用过氧化氢溶液的溶质质量分数为5%.
| 反应前物质的质量/g | 充分反应后物质的质量/g | |
| 过氧化氢溶液 | 二氧化锰 | 固体与液体混合物质量 |
| 136.0 | 0.2 | 133.0 |
Ⅰ.制得氧气的物质的量为0.1mol.
Ⅱ.该实验中反应的过氧化氢的物质的量(根据化学方程式计算).
Ⅲ.理论上该实验所用过氧化氢溶液的溶质质量分数为5%.
15.图示的四个图象分别对应四个变化过程的一种趋势,下列分析正确的是( )
| A. | 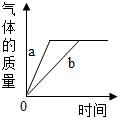 可能是双氧水溶液制氧气,a未使用催化剂,b使用了催化剂 | |
| B. | 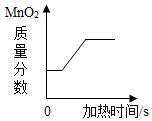 可能是加热一定质量的氯酸钾和二氧化锰固体混合物制取氧气过程 | |
| C. | 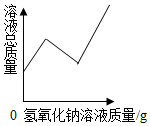 可能是硫酸铜溶液中滴加氢氧化钠溶液 | |
| D. | 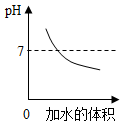 可能是向一定量的氢氧化钠溶液中加水稀释,溶液的pH变化 |
12.1mol燃料完全燃烧放出的热量见表.
①上述燃料中属于绿色能源的是氢气(H2).从等物质的量燃料完全燃烧放出热量多少来分析,目前最适合家庭使用的气体燃料是甲烷.
②充分燃烧等物质的量的上述燃料,排放出二氧化碳的量最多的是酒精.
③煤气(主要成分是CO)与其它燃料相比的主要缺点是有毒性,写出一氧化碳燃烧的化学方程式2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
④酒精中质量分数最高的元素是碳(C),0.5mol酒精中含有.806×1024.个氢原子.
| 燃料 | 一氧化碳(CO) | 氢气(H2) | 甲烷(CH4) | 酒精(C2H5OH) |
| 状态 | 气体 | 气体 | 气体 | 液体 |
| 热量(kJ) | 282.6 | 285.8 | 890.3 | 1367 |
②充分燃烧等物质的量的上述燃料,排放出二氧化碳的量最多的是酒精.
③煤气(主要成分是CO)与其它燃料相比的主要缺点是有毒性,写出一氧化碳燃烧的化学方程式2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
④酒精中质量分数最高的元素是碳(C),0.5mol酒精中含有.806×1024.个氢原子.
10.空气中体积分数约为78%的物质是( )
| A. | O2 | B. | N2 | C. | CO2 | D. | H2O |
9.属于化学变化的是( )
| A. | 冰川融化 | B. | 衣服晒干 | C. | 蜡烛燃烧 | D. | 酒精挥发 |
8. 水是地球上一种最普通、最常见的物质.
水是地球上一种最普通、最常见的物质.
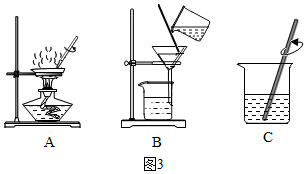
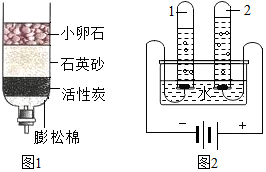
①图1所示的是简易净水器,其中活性炭的作用是过滤和吸附.
②水厂处理水时,有时会向水中加生石灰,此过程中发生的化学方程式为CaO+H2O═Ca(OH)2.
③图2是电解水的简易装置,试管1中生成的气体是氢气,反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
④将少量下面的调味品加入水中,不能形成溶液的是D.
A.食盐B.蔗糖C.味精D.芝麻油
⑤碘酒中的溶剂为酒精(质名称)
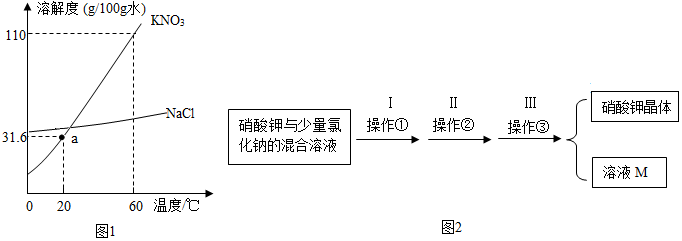
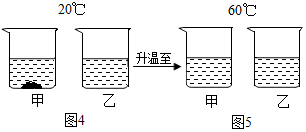
⑥在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
①实验a、b、c、d中,有未被溶解的KNO3固体析出的实验是d(填写实验编号).
②该温度下KNO3的溶解度是110g.
③实验a、b、c、d所得溶液中质量分数大小关系为:a<b<c=d.
④取实验b所得溶液,若使其质量分数变为20%,在不改变温度的情况下,可以采取的操作是加入150g水.
0 153879 153887 153893 153897 153903 153905 153909 153915 153917 153923 153929 153933 153935 153939 153945 153947 153953 153957 153959 153963 153965 153969 153971 153973 153974 153975 153977 153978 153979 153981 153983 153987 153989 153993 153995 153999 154005 154007 154013 154017 154019 154023 154029 154035 154037 154043 154047 154049 154055 154059 154065 154073 211419
 水是地球上一种最普通、最常见的物质.
水是地球上一种最普通、最常见的物质.①图1所示的是简易净水器,其中活性炭的作用是过滤和吸附.
②水厂处理水时,有时会向水中加生石灰,此过程中发生的化学方程式为CaO+H2O═Ca(OH)2.
③图2是电解水的简易装置,试管1中生成的气体是氢气,反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
④将少量下面的调味品加入水中,不能形成溶液的是D.
A.食盐B.蔗糖C.味精D.芝麻油
⑤碘酒中的溶剂为酒精(质名称)
⑥在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
| 实验编号 | a | b | c | d |
| 加入KNO3固体的质量 | 45 | 50 | 55 | 60 |
| 所得溶液的质量 | 95 | 100 | 105 | 105 |
②该温度下KNO3的溶解度是110g.
③实验a、b、c、d所得溶液中质量分数大小关系为:a<b<c=d.
④取实验b所得溶液,若使其质量分数变为20%,在不改变温度的情况下,可以采取的操作是加入150g水.