7.不少家庭养观赏鱼,有时会在鱼缸里放点“鱼浮灵”,可使水中的含氧量迅速增加.请你和小欣同学一起完成这项探究活动.

【查阅资料】过碳酸钠,白色结晶颗粒,易溶于水并迅速放出氧气.
【猜想假设】“鱼浮灵”的主要成分是过碳酸钠.
【性质探究】
【结果分析】主要成分是过碳酸钠,根据化学反应方程式:X+H2O═Na2CO3+H2O2,推出过碳酸钠的化学式X为Na2CO4.
【工业制备】(如图2)
(3)稳定剂的作用是防止H2O2分解(或防止过碳酸钠分解),稳定剂中MgCl2和Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子包裹住,该反应的化学方程式为MgCl2+Na2SiO3=MgSiO3↓+2NaCl.
(4)浊液中加入异丙醇的作用是降低过碳酸钠的溶解度(或减少过碳酸钠的溶解或提高产率等).
【测定纯度】
实验资料:过碳酸钠样品中的杂质不溶于水且不与水反应.
实验原理:2Na2CO4+4HCl═4NaCl+2CO2↑+O2↑+2H2O
实验装置:如图3所示
交流与讨论
Ⅰ.甲同学认为测定产物中O2的体积即可测定样品(含有的杂质不溶于水且不与酸反应)的纯度(样品中过碳酸钠的质量分数).
(5)装置②的作用是:吸收二氧化碳和氯化氢气体;
(6)装置③的作用是:检验二氧化碳是否完全被吸收;
(7)称取适量样品与足量浓盐酸充分反应后,收集到的氧气的体积为0.25L(已知该实验条件下氧气的密度为1.28g/L),则称取的样品质量应大于2.44g.
Ⅱ.乙同学认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度.但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是ABC(填序号).
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
Ⅲ.丙同学提出了一种新方案,得到了大家的一致认可:称取样品12.5g,滴加足量浓盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,称得氯化钠固体11.7g,则该样品的纯度为多少?(写出计算过程)

【查阅资料】过碳酸钠,白色结晶颗粒,易溶于水并迅速放出氧气.
【猜想假设】“鱼浮灵”的主要成分是过碳酸钠.
【性质探究】
| 实验 | 主要操作步骤(如图1) | 主要实验现象 | 结论 |
| (1) | 在集气瓶中加入少量MnO2(黑色固体),在仪器a中加入新配制的“鱼浮灵”的饱和水溶液;打开仪器a的活塞,放出适量溶液后,在导管口放一根带火星的木条 | 有气泡逸出,能使带火星木条复燃 | “鱼浮灵”溶于水生成过氧化氢 |
| (2) | 关闭仪器a,在仪器b中加入稀盐酸,打开活塞,放出适量溶液后,在导管口放一燃着的木条 | 生成大量无色气泡,木条熄灭 | “鱼浮灵”溶于水生成碳酸钠 |
【工业制备】(如图2)
(3)稳定剂的作用是防止H2O2分解(或防止过碳酸钠分解),稳定剂中MgCl2和Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子包裹住,该反应的化学方程式为MgCl2+Na2SiO3=MgSiO3↓+2NaCl.
(4)浊液中加入异丙醇的作用是降低过碳酸钠的溶解度(或减少过碳酸钠的溶解或提高产率等).
【测定纯度】
实验资料:过碳酸钠样品中的杂质不溶于水且不与水反应.
实验原理:2Na2CO4+4HCl═4NaCl+2CO2↑+O2↑+2H2O
实验装置:如图3所示
交流与讨论
Ⅰ.甲同学认为测定产物中O2的体积即可测定样品(含有的杂质不溶于水且不与酸反应)的纯度(样品中过碳酸钠的质量分数).
(5)装置②的作用是:吸收二氧化碳和氯化氢气体;
(6)装置③的作用是:检验二氧化碳是否完全被吸收;
(7)称取适量样品与足量浓盐酸充分反应后,收集到的氧气的体积为0.25L(已知该实验条件下氧气的密度为1.28g/L),则称取的样品质量应大于2.44g.
Ⅱ.乙同学认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度.但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是ABC(填序号).
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
Ⅲ.丙同学提出了一种新方案,得到了大家的一致认可:称取样品12.5g,滴加足量浓盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,称得氯化钠固体11.7g,则该样品的纯度为多少?(写出计算过程)
4.下列说法正确的是 ( )
| A. | 原子失去电子形成带正电的阳离子;钠原子和钠离子具有相同的电子数 | |
| B. | 洗洁精能洗去油污是因为它能溶解油脂;在水中加入食盐能增强溶液的导电性 | |
| C. | 有发热、发光现象的不一定是燃烧;酸碱中和后溶液不一定呈中性 |
3.实验小组同学通过以下实验研究二氧化碳的性质.
(1)该实验可以说明分子具有的性质是分子是不断运动的.
(2)烧杯内壁上贴干的紫色石蕊纸条的目的是证明干燥的二氧化碳不能使紫色的石蕊试液变红色.
(3)该实验得出的结论是二氧化碳与水反应生成了碳酸.
(4)写出二氧化碳遇到石灰水发生反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
| 实验装置 | 实验操作 | 实验现象 |
 | ①在烧杯内壁上贴上干的和用水润湿的紫色石蕊纸条 ②将充满二氧化碳的敞口集气瓶轻轻放入烧杯中 | 一段时间后,湿的紫色石蕊纸条变为红色 |
(2)烧杯内壁上贴干的紫色石蕊纸条的目的是证明干燥的二氧化碳不能使紫色的石蕊试液变红色.
(3)该实验得出的结论是二氧化碳与水反应生成了碳酸.
(4)写出二氧化碳遇到石灰水发生反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
2.下列图示的实验操作不正确的是( )
| A. |  给液体加热 | B. |  测溶液的pH | C. |  稀释浓硫酸 稀释浓硫酸 | D. |  蒸发食盐水 |
1.下列两种物质的溶液能发生反应.且反应后溶液的总质量不变的是( )
| A. | 碳酸钠溶液和稀盐酸 | B. | 氢氧化钠溶液和稀盐酸 | ||
| C. | 氯化钠溶液和稀硫酸 | D. | 稀硫酸和氯化钡溶液 |
20.把一定质量的锌和镁分别投入到适量的稀盐酸中,充分反应后,生成等质量的氢气,则投入的锌和镁的质量比是( )
| A. | 1:1 | B. | 65:24 | C. | 24:65 | D. | 无法确定 |
19.某合金由两种金属元素组成,取该合金60g投入足量稀硫酸中,反应完全后,测得生成H2 2g,则合金的组成不可能是( )
0 153602 153610 153616 153620 153626 153628 153632 153638 153640 153646 153652 153656 153658 153662 153668 153670 153676 153680 153682 153686 153688 153692 153694 153696 153697 153698 153700 153701 153702 153704 153706 153710 153712 153716 153718 153722 153728 153730 153736 153740 153742 153746 153752 153758 153760 153766 153770 153772 153778 153782 153788 153796 211419
| A. | Fe与Zn | B. | Mg与Cu | C. | Zn与Al | D. | Al与Fe |
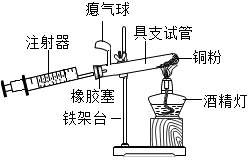 为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为50mL的试管作反应容器,将过量的铜粉放入试管,用橡皮塞塞紧试管口,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.请回答下列问题:
为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为50mL的试管作反应容器,将过量的铜粉放入试管,用橡皮塞塞紧试管口,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.请回答下列问题: