18.下列实验的先后顺序关系正确的是( )
| A. | 制取气体时,先装药品后检查装置的气密性 | |
| B. | 用排水法收集满氧气后,先将集气瓶从水中取出正放于桌面,再盖上玻璃片 | |
| C. | 加热高锰酸钾制氧气,停止加热时,先熄灭酒精灯再把导管移出水面后 | |
| D. | 铁与稀硫酸反应时,先向试管中加入铁钉,再加入硫酸铜溶液 |
17.下列化学方程式正确的是( )
| A. | H2O$\frac{\underline{\;通电\;}}{\;}$H2+O2 | B. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | ||
| C. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2↑ | D. | CuSO4+2NaOH═Na2SO4+Cu(OH)2↓ |
14.下列实验基本操作正确的是( )
| A. | 检查装置气密性时,先用手握住试管,然后将导气管伸入水中 | |
| B. | 用托盘天平称量固体药品时,先加质量小的砝码后加质量大的砝码 | |
| C. | 连接玻璃管和橡胶管时,现将玻璃管口的水润湿,然后对准橡胶塞上的孔稍稍加力转动插入 | |
| D. | 用量筒量一定量液体药品时,先用胶头滴管滴加,然后倾倒液体 |
13.下列各组物质汇总,前者属于纯净物,后者属于混合物的是( )
| A. | 冰水混合物,五氧化二磷 | B. | 二氧化碳、澄清石灰水 | ||
| C. | 矿泉水、河水 | D. | 净化后的空气,受污染的空气 |
12.空气中体积分数最大的气体是( )
| A. | 稀有气体 | B. | 氧气 | C. | 二氧化碳 | D. | 氮气 |
11.人教版新化学教材关于“分解过氧化氢制氧气的反应中二氧化锰的催化作用“以及”寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣.
【实验探究】
实验Ⅰ的A试管中若伸入燃烧的硫,则产生明亮的蓝紫色火焰,实验Ⅲ中“将实验Ⅱ中的剩余物小心过滤”时使用的玻璃棒,其作用是引流.
【实验结论】实验Ⅱ、Ⅲ证明:氧化铁(Fe2O3)的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢分解的催化剂.
写出氧化铁(Fe2O3)催化过氧化氢分解的化学符号表达式2H2O2$\frac{\underline{\;三氧化二铁\;}}{\;}$2H2O+O2↑.
【实验评价】设计实验Ⅳ的目的是探究氧化铁的催化效果是否比二氧化锰的更好.
若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰更适合做过氧化氢分解生成氧气的催化剂.
【实验拓展】
查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂.下列有关催化剂的说法中正确的是B(填序号).
A.MnO2只能作为过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其它反应的反应物或生成物.
若答对下列问题将奖励4分,但化学试卷总分不超过60分.为探究“二氧化锰的质量对过氧化氢分解反应速率的影响”,小组同学在老师的指导下又进行了如下实验:
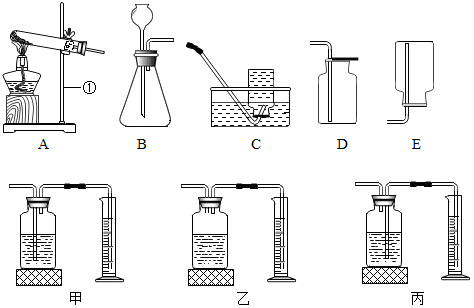
Ⅰ.按图甲组装实验仪器并进行气密性检测
Ⅱ.取10毫升溶质质量分数为3%的过氧化氢溶液和0.03克二氧化锰装入容器,塞紧橡皮塞,接上压强测量仪(如图乙)
Ⅲ.倾斜装置,使过氧化氢溶液和二氧化锰充分混合,用压强测量仪测量容器内的气压
Ⅳ.分别用0.06克、0.09克和0.12克相同的二氧化锰重复上述实验,整理相关数据如图丙.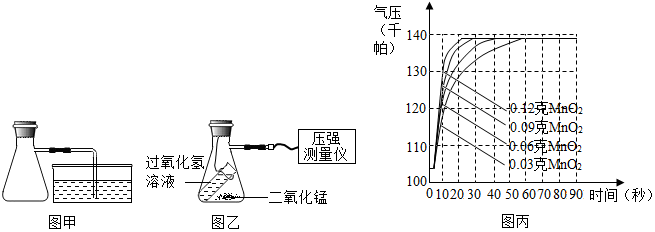
①写出步骤Ⅰ中检查装置气密性的具体操作及气密性良好的判断依据:用手捂住锥形瓶,导管口出现气泡,说明装置不漏气.
②实验中,小组同学用容器内压强的大小来反映产生氧气的多少.
③该探究过程得出的结论是二氧化锰的质量对反应速率的影响.
0 153517 153525 153531 153535 153541 153543 153547 153553 153555 153561 153567 153571 153573 153577 153583 153585 153591 153595 153597 153601 153603 153607 153609 153611 153612 153613 153615 153616 153617 153619 153621 153625 153627 153631 153633 153637 153643 153645 153651 153655 153657 153661 153667 153673 153675 153681 153685 153687 153693 153697 153703 153711 211419
【实验探究】
| 实验步骤 | 实验现象 |
| Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁( Fe2O3)粉末,并分别在A、B两支试管中插入带火星木条,观察现象. | A试管中产生气泡,带火星木条复燃,B试管中无明显现象. |
| Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象. | 试管中均产生气泡,带火星木条均复燃. |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得虑渣进行洗涤、干燥、称量,所得固体质量仍为a克. | / |
| Ⅳ.在装有a克氧化铁粉末的C试管、装有a克二氧化锰粉末的D中分别放入5mL5%过氧化氢溶液,观察现象. | / |
【实验结论】实验Ⅱ、Ⅲ证明:氧化铁(Fe2O3)的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢分解的催化剂.
写出氧化铁(Fe2O3)催化过氧化氢分解的化学符号表达式2H2O2$\frac{\underline{\;三氧化二铁\;}}{\;}$2H2O+O2↑.
【实验评价】设计实验Ⅳ的目的是探究氧化铁的催化效果是否比二氧化锰的更好.
若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰更适合做过氧化氢分解生成氧气的催化剂.
【实验拓展】
查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂.下列有关催化剂的说法中正确的是B(填序号).
A.MnO2只能作为过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其它反应的反应物或生成物.
若答对下列问题将奖励4分,但化学试卷总分不超过60分.为探究“二氧化锰的质量对过氧化氢分解反应速率的影响”,小组同学在老师的指导下又进行了如下实验:
Ⅰ.按图甲组装实验仪器并进行气密性检测
Ⅱ.取10毫升溶质质量分数为3%的过氧化氢溶液和0.03克二氧化锰装入容器,塞紧橡皮塞,接上压强测量仪(如图乙)
Ⅲ.倾斜装置,使过氧化氢溶液和二氧化锰充分混合,用压强测量仪测量容器内的气压
Ⅳ.分别用0.06克、0.09克和0.12克相同的二氧化锰重复上述实验,整理相关数据如图丙.

①写出步骤Ⅰ中检查装置气密性的具体操作及气密性良好的判断依据:用手捂住锥形瓶,导管口出现气泡,说明装置不漏气.
②实验中,小组同学用容器内压强的大小来反映产生氧气的多少.
③该探究过程得出的结论是二氧化锰的质量对反应速率的影响.


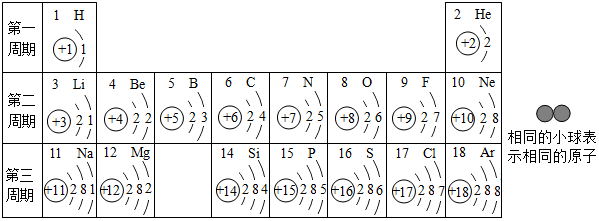
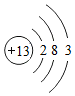 ,它在化学反应中容易失去(填“得到”或“失去”)电子.11号和17号元素组成的物质是氯化钠,构成该物质的微粒是离子(填“分子”、“原子”或“离子”)
,它在化学反应中容易失去(填“得到”或“失去”)电子.11号和17号元素组成的物质是氯化钠,构成该物质的微粒是离子(填“分子”、“原子”或“离子”) ”相似的物质的化学式N2(或 O2或 Cl2).
”相似的物质的化学式N2(或 O2或 Cl2).