10.2008年9月,三鹿婴幼儿奶粉被检出含三聚氰胺,引起全社会的强烈谴责,三聚氰胺的化学式为C3H6N6,根据该化学式你不能获得的信息是( )
| A. | 三聚氰胺是化合物 | |
| B. | 三聚氰胺由碳元素、氢元素和氮元素组成 | |
| C. | 三聚氰胺中碳元素,氢元素和氮元素的质量比为1:2:2 | |
| D. | 一个三聚氰胺分子中有15个原子 |
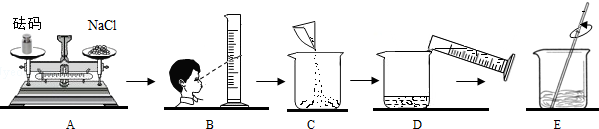
9.如图所示实验操作中,不正确的是( )
| A. | 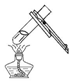 加热液体 | B. | 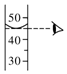 读取液体体积 | C. | 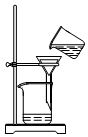 过滤 | D. | 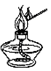 点燃酒精灯 |
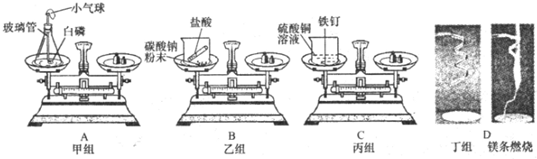
8.下列实验现象描述正确的是( )
| A. | 镁在空气中燃烧时,发出耀眼的白光,生成白色固体,放出热量 | |
| B. | 在碳酸钠粉末中加入稀盐酸,有大量白烟生成,固体粉末逐渐减少 | |
| C. | 白磷在密闭的容器中燃烧时,产生大量的黄烟 | |
| D. | 将铁钉放入硫酸铜溶液中,铁钉表面覆盖一层红色的物质,溶液由蓝色变为无色 |
6.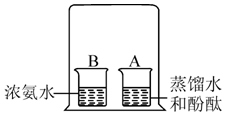 如图所示,在小烧杯A中装入30mL蒸馏水,再滴入3滴酚酞,在小烧杯B中装入30mL浓氨水.用一大烧杯把A、B两个烧杯罩在一起,过一段时间后看到的现象是A烧杯中液体变红,该实验说明分子是不断运动的.
如图所示,在小烧杯A中装入30mL蒸馏水,再滴入3滴酚酞,在小烧杯B中装入30mL浓氨水.用一大烧杯把A、B两个烧杯罩在一起,过一段时间后看到的现象是A烧杯中液体变红,该实验说明分子是不断运动的.
一些同学对上述结论有不同看法,主要有以下两种猜测:
第一种:A烧杯中的蒸馏水使酚酞试液变红;
第二种:B烧杯中的浓氨水挥发出氨气,扩散到A烧
杯的溶液中使酚酞试液变红.
①你认为第二种猜测正确;
②为证明这两种猜测,现设计如下的实验:(请填空)
③上述探究在设计上采用了对比实验,证明出不同的分子,其化学性质不同(填“化学”或“物理”).
 如图所示,在小烧杯A中装入30mL蒸馏水,再滴入3滴酚酞,在小烧杯B中装入30mL浓氨水.用一大烧杯把A、B两个烧杯罩在一起,过一段时间后看到的现象是A烧杯中液体变红,该实验说明分子是不断运动的.
如图所示,在小烧杯A中装入30mL蒸馏水,再滴入3滴酚酞,在小烧杯B中装入30mL浓氨水.用一大烧杯把A、B两个烧杯罩在一起,过一段时间后看到的现象是A烧杯中液体变红,该实验说明分子是不断运动的.一些同学对上述结论有不同看法,主要有以下两种猜测:
第一种:A烧杯中的蒸馏水使酚酞试液变红;
第二种:B烧杯中的浓氨水挥发出氨气,扩散到A烧
杯的溶液中使酚酞试液变红.
①你认为第二种猜测正确;
②为证明这两种猜测,现设计如下的实验:(请填空)
| 实验内容和方法 | 现象 | 结论 |
| 用洁净的小烧杯取20mL水,滴入2~3滴酚酞试液,观察现象 | 不变色 | 水不能(填“能”或“不能”)使酚酞变色 |
| 取一张滤纸,滴上酚酞试液,待晾干后,放在装有浓氨水的试剂瓶上方 | 酚酞不变色 | 氨气不能使酚酞变色(填“能”或“不能”) |
| 将少量氨气通入含有酚酞试液的蒸馏水中 | 溶液变成 红色 | 氨气溶解在水中形成氨水能使酚酞变色 |
2.下列诗词句或典故描述的主要是物理变化的是( )
| A. | 水滴石穿,金石可镂 | B. | 爆竹声中一岁除,春风送暖入屠苏 | ||
| C. | 野火烧不尽,春风吹又生 | D. | 春蚕到死丝方尽,蜡炬成灰泪始干 |
1.化学用语是一套国际通用的符号,是我们表达化学意义的工具.
(1)正确运用化学用语是学好化学的基础,请用化学符号完成如表.
(2)用相应粒子的化学符号填空
①从微观的角度看,水是由H2O构成的,氯化钠是由Na+、Cl-构成的.
②保持氧气化学性质的最小粒子是O2.
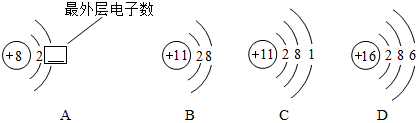
(3)离子结构示意图可简明、方便地表示粒子的结构.A图示表示氧原子,其最外层上电子数为6(填数字);下列四种粒子中具有相对稳定结构的是B(填序号);表示同种元素的是B和C(填序号).
(4)按要求写出下列化学反应的方程式:
①有水参与的分解反应2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
②有白烟生成的反应4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
③酒精(C2H5OH)燃烧生成水和二氧化碳的反应C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
0 153298 153306 153312 153316 153322 153324 153328 153334 153336 153342 153348 153352 153354 153358 153364 153366 153372 153376 153378 153382 153384 153388 153390 153392 153393 153394 153396 153397 153398 153400 153402 153406 153408 153412 153414 153418 153424 153426 153432 153436 153438 153442 153448 153454 153456 153462 153466 153468 153474 153478 153484 153492 211419
(1)正确运用化学用语是学好化学的基础,请用化学符号完成如表.
| 地壳中含量最多的金属元素 | 氦气 | 2个亚铁离子 | 3个氮分子 | 硫酸锌中+2价的锌元素 |
| Al | He | 2Fe2+ | 3N2 | $\stackrel{+2}{Zn}SO$4 |
①从微观的角度看,水是由H2O构成的,氯化钠是由Na+、Cl-构成的.
②保持氧气化学性质的最小粒子是O2.
(3)离子结构示意图可简明、方便地表示粒子的结构.A图示表示氧原子,其最外层上电子数为6(填数字);下列四种粒子中具有相对稳定结构的是B(填序号);表示同种元素的是B和C(填序号).

(4)按要求写出下列化学反应的方程式:
①有水参与的分解反应2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
②有白烟生成的反应4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
③酒精(C2H5OH)燃烧生成水和二氧化碳的反应C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
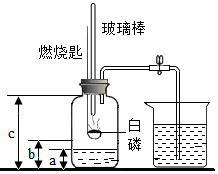 某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下:
某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下: