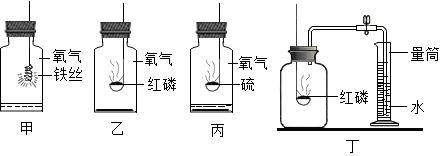
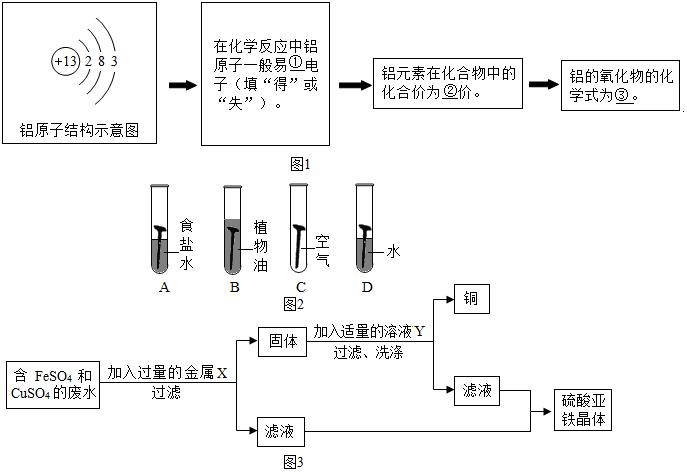
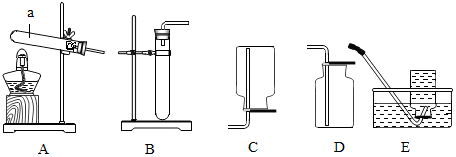
20.某单位发生了一起亚硝酸钠中毒事件.亚硝酸钠外观酷似食盐且有咸味,亚硝酸钠和食盐的有关资料如表:
(1)根据上表,请你写出亚硝酸钠的一个物理性质和一个化学性质.
物理性质:易溶于水;化学性质:能与稀盐酸反应生成二氧化氮.
(2)鉴别亚硝酸钠和食盐的方法是分别取少量亚硝酸钠和食盐,向其中加入稀盐酸,有红棕色气体生成的是亚硝酸钠,无明显现象的是食盐;
分别取少量亚硝酸钠和食盐,加热至320℃以上,放出有臭味的气体的为亚硝酸钠,无明显现象的为食盐;.
| 物质 | 亚硝酸钠 | 氯化钠 |
| 水溶性 | 易溶,在15℃时100g水中溶解亚硝酸钠81.5g | 易溶,在15℃时100g水中溶解氯化钠35.8g |
| 熔点 | 271℃ | 801℃ |
| 沸点 | 320℃会分解,放出有臭味的气体 | 1 413℃ |
| 跟稀盐酸反应 | 放出红棕色的气体二氧化氮 | 无现象 |
物理性质:易溶于水;化学性质:能与稀盐酸反应生成二氧化氮.
(2)鉴别亚硝酸钠和食盐的方法是分别取少量亚硝酸钠和食盐,向其中加入稀盐酸,有红棕色气体生成的是亚硝酸钠,无明显现象的是食盐;
分别取少量亚硝酸钠和食盐,加热至320℃以上,放出有臭味的气体的为亚硝酸钠,无明显现象的为食盐;.
17.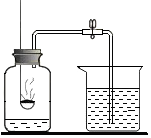 实验室可用如图所示装置来测定空气中氧气的含量.实验时可观察到:当红磷在集气瓶中燃烧停止后,集气瓶内水面上升大约$\frac{1}{5}$体积.请你回答:
实验室可用如图所示装置来测定空气中氧气的含量.实验时可观察到:当红磷在集气瓶中燃烧停止后,集气瓶内水面上升大约$\frac{1}{5}$体积.请你回答:
(1)集气瓶内水面上升约$\frac{1}{5}$体积,由此你得到的结论是:氧气约占空气总体积的五分之一.
(2)实验中的红磷需要稍微过量,目的是完全消耗瓶内氧气.请写出红磷燃烧这一反应的(文字或符号)表达式:磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(3)通过这个实验,我们还可以认识氮气的一些性质.请将你的分析结果填在如表
的横线上.
 实验室可用如图所示装置来测定空气中氧气的含量.实验时可观察到:当红磷在集气瓶中燃烧停止后,集气瓶内水面上升大约$\frac{1}{5}$体积.请你回答:
实验室可用如图所示装置来测定空气中氧气的含量.实验时可观察到:当红磷在集气瓶中燃烧停止后,集气瓶内水面上升大约$\frac{1}{5}$体积.请你回答:(1)集气瓶内水面上升约$\frac{1}{5}$体积,由此你得到的结论是:氧气约占空气总体积的五分之一.
(2)实验中的红磷需要稍微过量,目的是完全消耗瓶内氧气.请写出红磷燃烧这一反应的(文字或符号)表达式:磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(3)通过这个实验,我们还可以认识氮气的一些性质.请将你的分析结果填在如表
的横线上.
| 实 验 现 象 | 分 析 结 果(即氮气的性质) |
| ①燃烧着的红磷慢慢熄灭了 | 氮气不支持燃烧 |
| ③集气瓶内的水面上升一定高度后不再上升 | 氮气不易溶于水 |
16.通常情况下,人体呼出的气体中部分气体含量和空气中部分气体的含量如表:
请你根据所学的知识,完成如表实验报告.
0 153173 153181 153187 153191 153197 153199 153203 153209 153211 153217 153223 153227 153229 153233 153239 153241 153247 153251 153253 153257 153259 153263 153265 153267 153268 153269 153271 153272 153273 153275 153277 153281 153283 153287 153289 153293 153299 153301 153307 153311 153313 153317 153323 153329 153331 153337 153341 153343 153349 153353 153359 153367 211419
| 空气中的含量(%体积分数) | 呼出气体中的含量(%体积分数) | |
| 氧气 | 21 | 15.7 |
| 二氧化碳 | 0.03 | 3.6 |
| 水蒸气 | <0.03 | 6.2 |
| 操作步骤 | 现象 | 结论 |
| 将燃着的木条分别伸入装有 呼出气体和空气的集气瓶中. | (1)伸入呼出气体中的本条熄灭了,伸入空气中的木条继续燃烧. | 呼出气体中氧气的含量 比空气中的少. |
| (2)将相同滴数的澄清石灰水分别滴入装有呼出气体和空气的集气瓶中,振荡. | 呼出气体中澄清石灰水变白色 浑浊,而空气中的无明显现象. | (3)呼出气体中二氧化碳含量比空气中的多. |
| (4)取两片干燥的玻璃片,对着其中一片哈气,另一片放在空气中做对比. | (5)对着哈气的玻璃片上有水珠出现,放在空气中的那片则没有. | (6)呼出气体中水蒸气含量比空气中的多. |