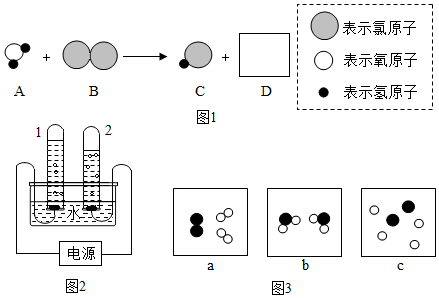
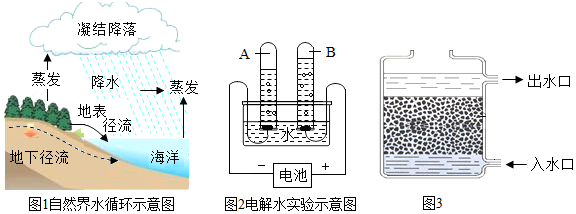
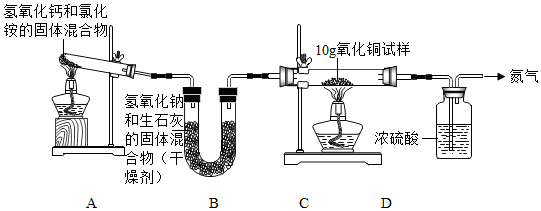
15.某化学活动小组用如图所示实验装置探究氨气(NH3)的性质、测定氧化铜试样中氧化铜的质量分数(其中杂质不发生变化,装置中的每一步处理都是完全的),充分反应后观察到C装置中的固体由黑色转变为亮红色.
试回答下列问题:
(1)氮气的密度和空气相似,难溶解于水,实验室收集氮气的方法是A
A.排水集气法 B.向上排空气集气法 C.向下排空气集气法
(2)A装置中的试管口要略低于试管底部的原因是防止冷凝水倒流炸裂试管;
(3)反应前后C、D装置的质量为:
10g氧化铜样品中氧化铜的质量是8g;
(4)写出C装置的玻璃管内发生反应的化学方程式:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.

试回答下列问题:
(1)氮气的密度和空气相似,难溶解于水,实验室收集氮气的方法是A
A.排水集气法 B.向上排空气集气法 C.向下排空气集气法
(2)A装置中的试管口要略低于试管底部的原因是防止冷凝水倒流炸裂试管;
(3)反应前后C、D装置的质量为:
| C装置总质量 | D装置总质量 | |
| 实验前 | 160g | 200g |
| 实验后 | 158.4g | 201.8g |
(4)写出C装置的玻璃管内发生反应的化学方程式:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.
13.碘元素(符号为I)具有预防和治疗甲状腺肿的作用,人体缺碘时易患大脖子病.为了消除碘缺乏病,我国政府规定居民的食用盐必须是加碘盐,简称碘盐.所谓碘盐就是在食盐中加入碘酸钾.下表是江西省盐业公司专营的精制碘盐包装袋上的部分说明文字.请回答下列问题:
(1)已知碘酸钾的化学式为KIO3,试计算:
①碘酸钾中碘元素(I)的化合价.
②碘酸钾中碘元素的质量分数
(2)由食用方法和贮藏指南可以推测碘酸钾的性质之一是:受热易分解.
(3)若1000g碘盐中含20mg碘.
①这里标明的碘的含量是指B
A.碘单质 B.碘元素 C.碘原子 D.碘分子
②已知成人每天约需要0.15mg碘,假设这些碘主要是从碘盐中摄取的,则成人每天需要食用碘盐多少克?
0 152541 152549 152555 152559 152565 152567 152571 152577 152579 152585 152591 152595 152597 152601 152607 152609 152615 152619 152621 152625 152627 152631 152633 152635 152636 152637 152639 152640 152641 152643 152645 152649 152651 152655 152657 152661 152667 152669 152675 152679 152681 152685 152691 152697 152699 152705 152709 152711 152717 152721 152727 152735 211419
| 配料表 | 食用盐、碘酸钾 |
| 含碘量 | (20mg~40mg)/kg |
| 保质期 | 18个月 |
| 食用方法 | 待食物烹调好后再放入碘盐,勿长时间炖炒 |
| 贮藏指南 | 避热、避光、密封、防潮 |
①碘酸钾中碘元素(I)的化合价.
②碘酸钾中碘元素的质量分数
(2)由食用方法和贮藏指南可以推测碘酸钾的性质之一是:受热易分解.
(3)若1000g碘盐中含20mg碘.
①这里标明的碘的含量是指B
A.碘单质 B.碘元素 C.碘原子 D.碘分子
②已知成人每天约需要0.15mg碘,假设这些碘主要是从碘盐中摄取的,则成人每天需要食用碘盐多少克?