1. 兴趣小组进行氧气制取与性质检验的实验.
兴趣小组进行氧气制取与性质检验的实验.
(1)下表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据
①写出该反应的符号表达式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
②据上表可知二氧化锰与氯酸钾的质量比为时,反应速率最快.
③二氧化锰的用量过少时产生氧气的速率很慢,原因是二者的接触面积小,MnO2的催化效果不明显.
④通过分析可知,在化学反应中催化剂的用量不是(填“是”或“不是”)越多越好.
⑤向盛满氧气的集气瓶中倒入迅速冷却的沸水(其中几乎不含氧气),立即塞紧两端开口的细玻璃管的橡皮塞,用注射器向玻璃管中注水至P 处,装置如图所示.
A.手拿集气瓶在水平面上摇晃数十次后,看到玻璃管中的液面将下降(填“上升”、“下降”或“不变”).
B.下列有关该实验的说法正确的是ab.
a.可说明有少量氧气溶于水中
b.应保证装置有良好的气密性
(2)以过氧化氢溶液为原料制取并收集氧气.
①写出该反应的符号表达式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②实验中,用装有一定量水的集气瓶进行排水法收集氧气,能使带火星木条复燃,那么使带火星的木条复燃的氧气体积分数的最低值是多少呢?进一步展开探究.
第一组实验:5只容积均为100毫升的集气瓶,分别装入一定体积的水,再用排水法收集氧气,恰好把5只集气瓶中的水排去,将带火星的木条依次伸入5只集气瓶中,记录实验现象.
第二组实验:以相同方法完成.
两组实验的数据和现象见下表(已知空气中氧气的体积分数为21%).
Ⅰ.第一组实验D 瓶,集气结束时氧气的体积分数为52.6%.
Ⅱ.经计算,第二组实验C 瓶的氧气体积分数为48.65%,由此得出“使带火星的木条复燃的氧气体积分数的最低值只能是48.65%”的结论.请结合第一组和第二组实验,对此结论和过程进行评价:该结论不严密,可省去第二组中编号的实验,应补充一个实验,该实验是集气前装入集气瓶内水的体积为34 毫升.
 兴趣小组进行氧气制取与性质检验的实验.
兴趣小组进行氧气制取与性质检验的实验.(1)下表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据
| 二氧化锰和氯酸钾的质量比 | 1:40 | 1:20 | 1:10 | 1:5 | 1:3 | 1:2 | 2:3 | 1:1 | 2:1 |
| 生成1L 氧气所需时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
②据上表可知二氧化锰与氯酸钾的质量比为时,反应速率最快.
③二氧化锰的用量过少时产生氧气的速率很慢,原因是二者的接触面积小,MnO2的催化效果不明显.
④通过分析可知,在化学反应中催化剂的用量不是(填“是”或“不是”)越多越好.
⑤向盛满氧气的集气瓶中倒入迅速冷却的沸水(其中几乎不含氧气),立即塞紧两端开口的细玻璃管的橡皮塞,用注射器向玻璃管中注水至P 处,装置如图所示.
A.手拿集气瓶在水平面上摇晃数十次后,看到玻璃管中的液面将下降(填“上升”、“下降”或“不变”).
B.下列有关该实验的说法正确的是ab.
a.可说明有少量氧气溶于水中
b.应保证装置有良好的气密性
(2)以过氧化氢溶液为原料制取并收集氧气.
①写出该反应的符号表达式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②实验中,用装有一定量水的集气瓶进行排水法收集氧气,能使带火星木条复燃,那么使带火星的木条复燃的氧气体积分数的最低值是多少呢?进一步展开探究.
第一组实验:5只容积均为100毫升的集气瓶,分别装入一定体积的水,再用排水法收集氧气,恰好把5只集气瓶中的水排去,将带火星的木条依次伸入5只集气瓶中,记录实验现象.
第二组实验:以相同方法完成.
两组实验的数据和现象见下表(已知空气中氧气的体积分数为21%).
| 第一组 | 第二组 | |||||||||
| 集气瓶编号 | A | B | C | D | E | A | B | C | D | E |
| 集气前装入集气瓶内水的体积(毫升) | 10 | 20 | 30 | 40 | 50 | 31 | 33 | 35 | 37 | 39 |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 |
Ⅱ.经计算,第二组实验C 瓶的氧气体积分数为48.65%,由此得出“使带火星的木条复燃的氧气体积分数的最低值只能是48.65%”的结论.请结合第一组和第二组实验,对此结论和过程进行评价:该结论不严密,可省去第二组中编号的实验,应补充一个实验,该实验是集气前装入集气瓶内水的体积为34 毫升.
17.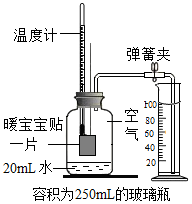 下列说法错误的是( )
下列说法错误的是( )
 下列说法错误的是( )
下列说法错误的是( )| A. | 实验前必须检查装置的气密性 | |
| B. | 通过本次实验数据测得空气中氧气的体积分数为18% | |
| C. | 若实验测得空气中氧气体积分数偏低,可能是暖宝宝贴的使用数量不足 | |
| D. | 必须等温度计的读数恢复至实验前的温度后才能记录量筒内剩余水的体积 |
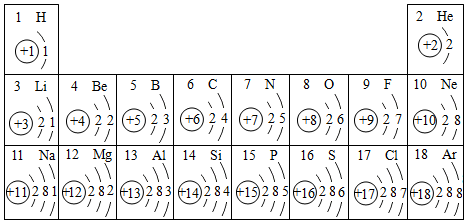
15.2015年10月,中国科学家屠呦呦凭借对青蒿素的研究成果获得了诺贝尔生理学或医学奖,青蒿素(化学式为:C15H22O5)是一种用于治疗疟疾的药物,曾拯救全球数百万生命,下列关于青蒿素的说法错误的是( )
| A. | C15H22O5表示青蒿素这种物质 | B. | 青蒿素是由C、H、O三种原子构成 | ||
| C. | 青蒿素是由C、H、O三种元素组成 | D. | 1个青蒿素分子中含有42个原子 |
14.下列对有关事实的解释,错误的是( )
0 152492 152500 152506 152510 152516 152518 152522 152528 152530 152536 152542 152546 152548 152552 152558 152560 152566 152570 152572 152576 152578 152582 152584 152586 152587 152588 152590 152591 152592 152594 152596 152600 152602 152606 152608 152612 152618 152620 152626 152630 152632 152636 152642 152648 152650 152656 152660 152662 152668 152672 152678 152686 211419
| A. | 酒精需要密封保存--酒精分子在不停运动 | |
| B. | 冰水共存物属于纯净物--冰和水都由相同分子构成 | |
| C. | 过氧化氢分解属于化学变化--过氧化氢分子本身发生改变 | |
| D. | 用水壶烧水,水开时壶盖被顶开--水分子分解成氢原子和氧原子,粒子数目增多了 |

 ”表示氮原子,“
”表示氮原子,“ ”表示氧原子.
”表示氧原子. ”可表示的微粒是氮分子(填名称).
”可表示的微粒是氮分子(填名称).



