8.现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn一119,Ni一59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
试求:①合金中铜的质量分数.②合金中另一金属为何种金属.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn一119,Ni一59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
| 次数 | l | 2 | 3 | 4 |
| 加入酸质量/g | 5.0 | 5.0 | 5.0 | 5.0 |
| 剩余固态质量/g | 4.5 | 4 | 3.5 | 3.2 |
2.小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题.她设计并完成了如表所示的探究实验:
(1)请你帮小丽同学填写上表中未填完的空格.
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用是对比.
(3)小英补充设计两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验实验前称量二氧化锰的质量,试验后过滤出二氧化锰烘干后重新称量,其目的是:比较MnO2在过氧化氢分解前后的质量;
第二方面的实验是利用“实验三”反应后试管内的剩余物固体再次加入过氧化氢,观察到过氧化氢迅速分解产生大量氧气,带火星木条复燃.该实验的目的是:证明MnO2仍然能加快过氧化氢的分解速率(化学性质没变).
| 实验操作 | 实验现象 | 实验结论或总结 | ||
| 结论 | 总结 | |||
| 实验一 | 取5mL 5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是反应慢. 反应的文字表达式为: 过氧化氢$\stackrel{二氧化锰}{→}$水+氧气 | 二氧化锰是过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | 二氧化锰加入水中不产生氧气 | |
| 实验三 | 向盛有5mL5%的过氧化氢溶液的试管中,加入二氧化锰,伸入带火星的木条 | 大量气泡产生,带火星的木条迅速复燃 | 二氧化锰能加快过氧化氢的分解 | |
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用是对比.
(3)小英补充设计两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验实验前称量二氧化锰的质量,试验后过滤出二氧化锰烘干后重新称量,其目的是:比较MnO2在过氧化氢分解前后的质量;
第二方面的实验是利用“实验三”反应后试管内的剩余物固体再次加入过氧化氢,观察到过氧化氢迅速分解产生大量氧气,带火星木条复燃.该实验的目的是:证明MnO2仍然能加快过氧化氢的分解速率(化学性质没变).
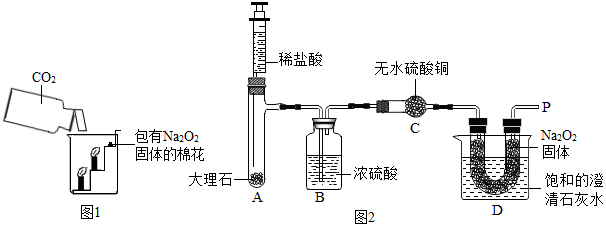
1.过氧化钠(Na2O2)是一种淡黄色固体.在一次科技活动中,某化学兴趣小组的同学将包有Na2O2固体的棉花放入了如图1的实验中,发现了高低不同的两根蜡烛,下面的蜡烛先熄灭,上面的蜡烛后熄灭;同时也惊奇地发现棉花燃烧了起来.
(一).探究棉花燃烧的原因
(1)实验中“下面的蜡烛先熄灭,上面的蜡烛后熄灭”的现象说明二氧化碳具有密度比空气大、不能燃烧、不支持燃烧的性质.
(2)棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知识,推理出棉花要燃烧,除了满足“棉花是可燃物”这一条件,还另需满足a:与氧气接触、b:温度达到棉花的着火点两个条件.
【提出问题】在上述实验中是如何给棉花提供a和b这两个燃烧条件的呢?
【查阅资料】在常温下Na2O2和CO2能发生化学反应.
【设计实验】经过讨论后,小组同学设计了如图2的实验进行探究.
【实验步骤】
①检查整套装置的气密性;
②把相关的试剂放入对应的仪器内,并按图2组装整套实验仪器;
③用力推动针筒的活塞,把稀盐酸注入试管内;
④一段时间后,在P处放置一根带火星的小木条,观察现象.
【实验现象】①无水硫酸铜没有变蓝色;②带火星的小木条复燃;③饱和的澄清石灰水出现白色不溶物.
【实验分析】①A装置中发生的化学反应方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑;
②D装置的烧杯内出现白色不溶物的原因是过氧化钠和二氧化碳反应放热,导致氢氧化钙溶解度减小.
③为了保证进入D装置的气体中不含水蒸气,小组设计的实验装置中B装置的作用是吸收水蒸气;C装置的作用是检验二氧化碳中是否含有水蒸气.
【得出结论】①“小木条复燃”说明Na2O2和CO2反应产生了氧气,使图1中的棉花满足了燃烧条件a;②“饱和的澄清石灰水变浑浊”说明Na2O2和CO2反应要放出(填“吸收”或“放出”)热量,使图1中的棉花满足了燃烧条件b.
请帮着完成过氧化钠与二氧化碳反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.
【拓展延伸】兴趣小组的同学用脱脂棉包住少量过氧化钠(Na2O2),放在石棉网上.在脱脂棉上滴加几滴水,发现脱脂棉也燃烧起来.说明过氧化钠(Na2O2)还能与水反应.过氧化钠(Na2O2)与水反应生成了什么?他们向盛有过氧化钠粉末的试管中加入水,发现有气泡,将带火星木条伸入试管中,木条复燃,充分反应后,取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,液体变成红色,说明溶液中有NaOH生成.
过氧化钠与水反应方程式为:2Na2O2+2H2O=4NaOH+O2↑
过氧化钠久置于空气中会变质产生氢氧化钠和碳酸钠两种杂质.
(二).测定久置于空气中的过氧化钠样品中过氧化钠纯度
【实验过程】称量156g样品放在铜网中,按图3示装置组装后(药水瓶底部留有小孔),称量仪器及药品总质量,将铜网插入足量水中,反应完全后称量仪器及反应后物质总质量.测得实验数据如下表.
【问题讨论】
(1)药水瓶中碱石灰的作用为吸收水蒸气.
(2)本实验测得过氧化钠含量可能会偏小的原因是反应生成的氧气不能全部排出.
(3)根据实验数据计算:①生成氧气16g.
②样品中过氧化钠的质量分数是50%.
(三)测定久置过氧化钠样品中碳酸钠含量
【测定方案】
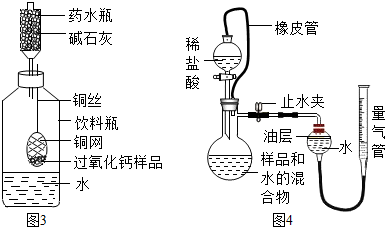
①如图4所示,连接好装置,检查装置气密性;
②精确称量一袋样品质量置于烧杯中并加入适量水混合,再全部倒入烧瓶中,并在分液漏斗中加入足量稀盐酸;
③将液面调节到量气管的“0”刻度,并使两边液面相平,打开止水夹和分液漏斗活塞;
④反应结束后,再次调节量气管两边液面相平,读出气体体积;
⑤计算样品中碳酸钠含量(CO2的密度为1.97g/L).
【问题讨论】
(1)图4中油层的作用为防止二氧化碳溶于水,用橡皮管将分液漏斗和烧瓶连接起来,其作用是使烧瓶和分液漏斗中的气体压强相等.
中和反应放热,滴加稀盐酸后,发生装置中的中和反应的化学方程式为NaOH+HCl═NaCl+H2O,这个反应的发生可能使测定结果偏大(填“偏大”、“偏小”或“无影响”).
(2)若测得量气管读数为896ml,则实验中选用的量气管规格合适的是B(填字母序号)
A、100ml B、1L C、2L
(3)步骤2中将样品和水混合的目的是使过氧化钠和水反应.
0 152034 152042 152048 152052 152058 152060 152064 152070 152072 152078 152084 152088 152090 152094 152100 152102 152108 152112 152114 152118 152120 152124 152126 152128 152129 152130 152132 152133 152134 152136 152138 152142 152144 152148 152150 152154 152160 152162 152168 152172 152174 152178 152184 152190 152192 152198 152202 152204 152210 152214 152220 152228 211419

(一).探究棉花燃烧的原因
(1)实验中“下面的蜡烛先熄灭,上面的蜡烛后熄灭”的现象说明二氧化碳具有密度比空气大、不能燃烧、不支持燃烧的性质.
(2)棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知识,推理出棉花要燃烧,除了满足“棉花是可燃物”这一条件,还另需满足a:与氧气接触、b:温度达到棉花的着火点两个条件.
【提出问题】在上述实验中是如何给棉花提供a和b这两个燃烧条件的呢?
【查阅资料】在常温下Na2O2和CO2能发生化学反应.
【设计实验】经过讨论后,小组同学设计了如图2的实验进行探究.
【实验步骤】
①检查整套装置的气密性;
②把相关的试剂放入对应的仪器内,并按图2组装整套实验仪器;
③用力推动针筒的活塞,把稀盐酸注入试管内;
④一段时间后,在P处放置一根带火星的小木条,观察现象.
【实验现象】①无水硫酸铜没有变蓝色;②带火星的小木条复燃;③饱和的澄清石灰水出现白色不溶物.
【实验分析】①A装置中发生的化学反应方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑;
②D装置的烧杯内出现白色不溶物的原因是过氧化钠和二氧化碳反应放热,导致氢氧化钙溶解度减小.
③为了保证进入D装置的气体中不含水蒸气,小组设计的实验装置中B装置的作用是吸收水蒸气;C装置的作用是检验二氧化碳中是否含有水蒸气.
【得出结论】①“小木条复燃”说明Na2O2和CO2反应产生了氧气,使图1中的棉花满足了燃烧条件a;②“饱和的澄清石灰水变浑浊”说明Na2O2和CO2反应要放出(填“吸收”或“放出”)热量,使图1中的棉花满足了燃烧条件b.
请帮着完成过氧化钠与二氧化碳反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.
【拓展延伸】兴趣小组的同学用脱脂棉包住少量过氧化钠(Na2O2),放在石棉网上.在脱脂棉上滴加几滴水,发现脱脂棉也燃烧起来.说明过氧化钠(Na2O2)还能与水反应.过氧化钠(Na2O2)与水反应生成了什么?他们向盛有过氧化钠粉末的试管中加入水,发现有气泡,将带火星木条伸入试管中,木条复燃,充分反应后,取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,液体变成红色,说明溶液中有NaOH生成.
过氧化钠与水反应方程式为:2Na2O2+2H2O=4NaOH+O2↑
过氧化钠久置于空气中会变质产生氢氧化钠和碳酸钠两种杂质.
(二).测定久置于空气中的过氧化钠样品中过氧化钠纯度
【实验过程】称量156g样品放在铜网中,按图3示装置组装后(药水瓶底部留有小孔),称量仪器及药品总质量,将铜网插入足量水中,反应完全后称量仪器及反应后物质总质量.测得实验数据如下表.
| 样品质量 | 装置及药品总质量 | 装置及反应后物质总质量 | |
| 实验数据 | 156 | 394g | 378g |
(1)药水瓶中碱石灰的作用为吸收水蒸气.
(2)本实验测得过氧化钠含量可能会偏小的原因是反应生成的氧气不能全部排出.
(3)根据实验数据计算:①生成氧气16g.
②样品中过氧化钠的质量分数是50%.
(三)测定久置过氧化钠样品中碳酸钠含量
【测定方案】

①如图4所示,连接好装置,检查装置气密性;
②精确称量一袋样品质量置于烧杯中并加入适量水混合,再全部倒入烧瓶中,并在分液漏斗中加入足量稀盐酸;
③将液面调节到量气管的“0”刻度,并使两边液面相平,打开止水夹和分液漏斗活塞;
④反应结束后,再次调节量气管两边液面相平,读出气体体积;
⑤计算样品中碳酸钠含量(CO2的密度为1.97g/L).
【问题讨论】
(1)图4中油层的作用为防止二氧化碳溶于水,用橡皮管将分液漏斗和烧瓶连接起来,其作用是使烧瓶和分液漏斗中的气体压强相等.
中和反应放热,滴加稀盐酸后,发生装置中的中和反应的化学方程式为NaOH+HCl═NaCl+H2O,这个反应的发生可能使测定结果偏大(填“偏大”、“偏小”或“无影响”).
(2)若测得量气管读数为896ml,则实验中选用的量气管规格合适的是B(填字母序号)
A、100ml B、1L C、2L
(3)步骤2中将样品和水混合的目的是使过氧化钠和水反应.

