19.有关水的认识正确的是( )
| A. | 电解水得到H2和O2,可知水是由氢原子和氧原子构成 | |
| B. | 生活中用过滤的方法可以得到纯净水 | |
| C. | 净水的方法有沉降、过滤、吸附、蒸馏 | |
| D. | 水循环中的降水是指降雨或降雪 |
18.过碳酸钠(Na2CO4)是一种常见的漂白杀菌剂,其水溶液显碱性,能和盐酸发生下列反应:2Na2CO4+4HCl═4NaCl+2CO2↑+O2↑+2H2O.工业用的过碳酸钠往往含有少量的碳酸钠.根据以上信息,下列说法正确的是( )
| A. | 过碳酸钠的水溶液能使无色酚酞变红,所以过碳酸钠是一种碱 | |
| B. | 过碳酸钠(Na2CO4)漂白杀菌时,发生了化学变化 | |
| C. | 过碳酸钠(Na2CO4)中碳元素的化合价为+4价 | |
| D. | 测定与盐酸反应后气体的总体积,可推算出过碳酸钠的纯度 |
17.下列实验方案能达到目的是( )
| A. | 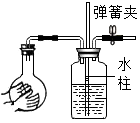 打开弹簧夹,检查装置的气密性 | |
| B. | 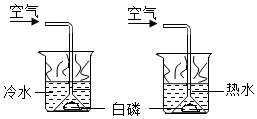 探究白磷燃烧的条件 | |
| C. |  探究反应物接触面积对反应速率的影响 | |
| D. |  探究某化肥是不是铵态氮肥 |
16. 一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
 一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )| A. | 丁是该反应的催化剂 | B. | 该反应的基本类型是分解反应 | ||
| C. | 反应中乙、丙的质量比为3:17 | D. | 若丙为氧气,则该反应为氧化反应 |
15.下列关于常见气体的说法正确的是( )
| A. | H2是目前发现的最清洁的燃料能源 | |
| B. | 用赤铁矿炼铁时,常用CO作氧化剂 | |
| C. | SO2主要危害是形成pH≤6.5的酸雨 | |
| D. | 干燥的CO2不能使紫色石蕊试液变红色 |
14.下列对有关实验现象的描述正确的是( )
| A. | 生锈的铁钉放入足量的稀硫酸中,溶液变成浅绿色,无气体产生 | |
| B. | 用玻璃棒沾氢氧化钠溶液涂在pH试纸上,试纸显示红色 | |
| C. | 浓硝酸银溶液中滴加稀硫酸,出现浑浊现象,滴加稀硝酸,浑浊消失 | |
| D. | 硫酸铜溶液中滴加氢氧化钠溶液,出现浑浊现象 |
13.化学小组同学取一定量碳酸钙固体高温煅烧一段时间,冷却后,对剩余固体成分进行如下探究.
【提出问题】剩余固体成分是什么?
【查阅资料】工业上通常采用高温煅烧石灰石的方法制生石灰,化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
【猜想与假设】剩余固体成分:
I.全部是氧化钙Ⅱ.氧化钙和碳酸钙Ⅲ.全部是碳酸钙
在老师指导下,小组同学设计如下实验,探究上述猜想是否成立.
【进行试验】
①甲同学取一定量的剩余固体于试管中,加入一定量的水振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅲ成立.乙同学认为上述实验不足以证明猜想Ⅲ成立,其理由是氧化钙与水反应生成的氢氧化钙微溶于水,也可能出现白色不溶物.
②乙同学取一定量的剩余固体于试管中,加入一定量的水,触摸试管外壁感觉发热,继续向试管中加入几滴稀盐酸,没有气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是即使有碳酸钙,加入的少量稀盐酸先消耗氢氧化钙,也不会出现气泡.
③丙同学利用水、无色酚酞溶液和稀盐酸证明了猜想Ⅱ成立,请完成实验报告.
【反思拓展】
工业制生石灰的过程中同时得到副产品二氧化碳.下列用途是利用二氧化碳化学性质的是ACD.
A.气体肥料 B.制干冰 C.制纯碱 D.制碳酸饮料.
0 151785 151793 151799 151803 151809 151811 151815 151821 151823 151829 151835 151839 151841 151845 151851 151853 151859 151863 151865 151869 151871 151875 151877 151879 151880 151881 151883 151884 151885 151887 151889 151893 151895 151899 151901 151905 151911 151913 151919 151923 151925 151929 151935 151941 151943 151949 151953 151955 151961 151965 151971 151979 211419
【提出问题】剩余固体成分是什么?
【查阅资料】工业上通常采用高温煅烧石灰石的方法制生石灰,化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
【猜想与假设】剩余固体成分:
I.全部是氧化钙Ⅱ.氧化钙和碳酸钙Ⅲ.全部是碳酸钙
在老师指导下,小组同学设计如下实验,探究上述猜想是否成立.
【进行试验】
①甲同学取一定量的剩余固体于试管中,加入一定量的水振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅲ成立.乙同学认为上述实验不足以证明猜想Ⅲ成立,其理由是氧化钙与水反应生成的氢氧化钙微溶于水,也可能出现白色不溶物.
②乙同学取一定量的剩余固体于试管中,加入一定量的水,触摸试管外壁感觉发热,继续向试管中加入几滴稀盐酸,没有气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是即使有碳酸钙,加入的少量稀盐酸先消耗氢氧化钙,也不会出现气泡.
③丙同学利用水、无色酚酞溶液和稀盐酸证明了猜想Ⅱ成立,请完成实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量剩余固体于试管中,加水振荡,过滤 取滤液滴加无色酚酞溶液 取滤渣滴加足量的稀盐酸 | 溶液变红 有气泡产生 | 猜想Ⅱ成立 |
工业制生石灰的过程中同时得到副产品二氧化碳.下列用途是利用二氧化碳化学性质的是ACD.
A.气体肥料 B.制干冰 C.制纯碱 D.制碳酸饮料.

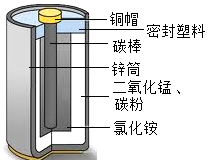 锌锰电池(俗称干电池)在生活中的用量很大,锌锰电池的构造如图所示,回答下列问题.
锌锰电池(俗称干电池)在生活中的用量很大,锌锰电池的构造如图所示,回答下列问题.