1.溶液与人类的生活息息相关,溶液的配制是日常生活和化学实验中的常见操作.下表是硫酸溶液和氨水的密度与其溶质的质量分数对照表(20℃).
请仔细分析后回答下列问题:
(1)20℃时,随着溶液中溶质的质量分数逐渐增大,硫酸溶液的密度逐渐增大(填“增大”、“减小”或“不变”),氨水的密度逐渐减小(填“增大”、“减小”或“不变”).
(2)取12%的硫酸溶液100g配制成6%的硫酸溶液,需加水的质量应为100g.
(3)向100g 24%的氨水中加入100g水,摇匀,溶液的体积是210.5mL(精确0.1mL).
| 溶液中溶质的质量分数(%) | 4 | 12 | 16 | 24 | 28 |
| 硫酸溶液的密度(g/mL) | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度(g/mL) | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
(1)20℃时,随着溶液中溶质的质量分数逐渐增大,硫酸溶液的密度逐渐增大(填“增大”、“减小”或“不变”),氨水的密度逐渐减小(填“增大”、“减小”或“不变”).
(2)取12%的硫酸溶液100g配制成6%的硫酸溶液,需加水的质量应为100g.
(3)向100g 24%的氨水中加入100g水,摇匀,溶液的体积是210.5mL(精确0.1mL).
2.学习了二氧化锰(MnO2)对过氧化氢分解有催化作用的知识后,某同学想:氧化铜(CuO)能否起到类似二氧化锰的催化作用呢?于是进行了以下探究.
【猜想】
Ⅰ.氧化铜(CuO)不是催化剂,也不参与反应,反应前后质量和化学性质不变;
Ⅱ.参与反应产生氧气(O2),反应前后质量和化学性质发生了改变;
Ⅲ.氧化铜(CuO)是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2g氧化铜(CuO),取5mL 5%的过氧化氢溶液于试管中,进行如下实验:
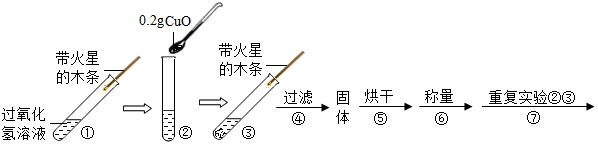
(1)填写下表:
(2)步骤①的目的是与步骤③对照.
(3)过氧化氢能被氧化铜催化分解放出氧气的文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气.
【猜想】
Ⅰ.氧化铜(CuO)不是催化剂,也不参与反应,反应前后质量和化学性质不变;
Ⅱ.参与反应产生氧气(O2),反应前后质量和化学性质发生了改变;
Ⅲ.氧化铜(CuO)是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2g氧化铜(CuO),取5mL 5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 有气泡产生,带火星的木条复燃 | 称量的氧化铜的质量仍为0.2g | 溶液中有气泡放出,带火星的木条复燃 | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立 |
(3)过氧化氢能被氧化铜催化分解放出氧气的文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气.
1.我们身边的下列物质中,属于纯净物的是( )
0 151447 151455 151461 151465 151471 151473 151477 151483 151485 151491 151497 151501 151503 151507 151513 151515 151521 151525 151527 151531 151533 151537 151539 151541 151542 151543 151545 151546 151547 151549 151551 151555 151557 151561 151563 151567 151573 151575 151581 151585 151587 151591 151597 151603 151605 151611 151615 151617 151623 151627 151633 151641 211419
| A. | 新鲜的空气 | B. | 医用酒精 | C. | 果汁 | D. | 蒸馏水 |

 硝酸钾与氯化钾的溶解度曲线如图所示,回答下列问题:
硝酸钾与氯化钾的溶解度曲线如图所示,回答下列问题: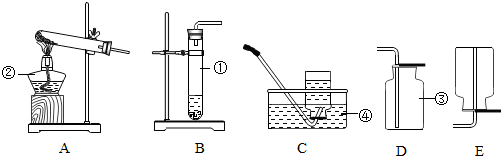
 在一个具有刻度和可以左右滑动的玻璃容器里放入一粒白磷(适量),将玻璃容器固定好(见图,固定装置已省略),放在盛有80℃水的烧杯上(白磷燃烧所需的最低温度为40℃).如图进行实验,试回答:
在一个具有刻度和可以左右滑动的玻璃容器里放入一粒白磷(适量),将玻璃容器固定好(见图,固定装置已省略),放在盛有80℃水的烧杯上(白磷燃烧所需的最低温度为40℃).如图进行实验,试回答: