2.下列化学用既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A. | 2O | B. | Fe | C. | O | D. | CH4 |
20.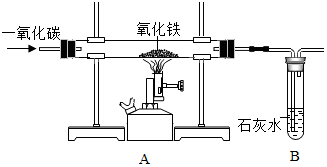 某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物.所用装置如图所示.
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物.所用装置如图所示.
(1)如果实验成功,请回答下列问题:
①实验过程中的现象:红色固体粉末变成黑色、澄清石灰水变浑浊.
②B装置中发生反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
③为保证安全和实验成功,该实验的操作步骤:badc.(填序号)
a.点燃A处酒精喷灯 b.通入CO气体
c.停止通入CO气体d.熄灭酒精喷灯.
④该装置设计有一个明显缺陷,你认为是没有尾气处理装置.
(2)兴趣小组用上图装置想计算12克赤铁矿样品中氧化铁的质量分数,他们收集了以下两组数据(假设所有能发生的反应都反应完全,矿石中杂质不参与化学反应):
数据A:玻璃管和固体样品在反应前后质量变化了a g;
数据B:整个实验中,实际通入玻璃管中的一氧化碳质量为b g.
你认为他们应该选用了A(填“A”或“B”)组数据来计算赤铁矿石中氧化铁的质量分数,不选用另一组数据计算的原因CO要先通后撤,没有全部参加反应.
(3)实验时准确称取一定质量纯净的Fe2O3固体和相关装置的质量按上图进行实验,当固体全部变黑后,继续通入CO直到玻璃管冷却.将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生.实验测得部分数据如下:
(4)实验分析
查阅资料:a.铁的氧化物在足量的稀盐酸中均能全部溶解.
b.Fe2O3与CO反应的固体生成物可能情况如下:
Fe2O3$\stackrel{400℃-500℃}{→}$Fe3O4$\stackrel{500℃-600℃}{→}$FeO(黑色)$\stackrel{700℃-800℃}{→}$Fe
分析推断:①装置B试管中增加的质量一定小于理论产生的CO2质量,可能原因是AB(填写字母代号).
A.未参加反应的CO通过B时带走了水蒸气;
B.石灰水浓度小没有将二氧化碳完全吸收;
C.石灰水吸收了空气中的二氧化碳气体.
②根据实验现象可确定反应后的固体中一定不存在Fe(填“一定”或“一定不”或“可能”).
理由:黑色固体中加入盐酸后没有气泡生成.
(5)实验结论:根据可靠实验数据计算出反应后的固体的成分.
过程:m(Fe)=32×$\frac{112}{160}$=22.4g;m(O)=28.8-22.4=6.4g56x:16y=22.4:6.4,解得x:y=1:1
成分:FeO
此时发生反应的化学方程式:Fe2O3+CO$\frac{\underline{\;高温\;}}{\;}$2FeO+CO2.
0 151348 151356 151362 151366 151372 151374 151378 151384 151386 151392 151398 151402 151404 151408 151414 151416 151422 151426 151428 151432 151434 151438 151440 151442 151443 151444 151446 151447 151448 151450 151452 151456 151458 151462 151464 151468 151474 151476 151482 151486 151488 151492 151498 151504 151506 151512 151516 151518 151524 151528 151534 151542 211419
 某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物.所用装置如图所示.
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物.所用装置如图所示.(1)如果实验成功,请回答下列问题:
①实验过程中的现象:红色固体粉末变成黑色、澄清石灰水变浑浊.
②B装置中发生反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
③为保证安全和实验成功,该实验的操作步骤:badc.(填序号)
a.点燃A处酒精喷灯 b.通入CO气体
c.停止通入CO气体d.熄灭酒精喷灯.
④该装置设计有一个明显缺陷,你认为是没有尾气处理装置.
(2)兴趣小组用上图装置想计算12克赤铁矿样品中氧化铁的质量分数,他们收集了以下两组数据(假设所有能发生的反应都反应完全,矿石中杂质不参与化学反应):
数据A:玻璃管和固体样品在反应前后质量变化了a g;
数据B:整个实验中,实际通入玻璃管中的一氧化碳质量为b g.
你认为他们应该选用了A(填“A”或“B”)组数据来计算赤铁矿石中氧化铁的质量分数,不选用另一组数据计算的原因CO要先通后撤,没有全部参加反应.
(3)实验时准确称取一定质量纯净的Fe2O3固体和相关装置的质量按上图进行实验,当固体全部变黑后,继续通入CO直到玻璃管冷却.将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生.实验测得部分数据如下:
| 玻璃管中固体的质量 | 装置B试管及其中物质的总质量 | |
| 反应前 | 32g | 300g |
| 反应后 | 28.8g | 308g |
查阅资料:a.铁的氧化物在足量的稀盐酸中均能全部溶解.
b.Fe2O3与CO反应的固体生成物可能情况如下:
Fe2O3$\stackrel{400℃-500℃}{→}$Fe3O4$\stackrel{500℃-600℃}{→}$FeO(黑色)$\stackrel{700℃-800℃}{→}$Fe
分析推断:①装置B试管中增加的质量一定小于理论产生的CO2质量,可能原因是AB(填写字母代号).
A.未参加反应的CO通过B时带走了水蒸气;
B.石灰水浓度小没有将二氧化碳完全吸收;
C.石灰水吸收了空气中的二氧化碳气体.
②根据实验现象可确定反应后的固体中一定不存在Fe(填“一定”或“一定不”或“可能”).
理由:黑色固体中加入盐酸后没有气泡生成.
(5)实验结论:根据可靠实验数据计算出反应后的固体的成分.
过程:m(Fe)=32×$\frac{112}{160}$=22.4g;m(O)=28.8-22.4=6.4g56x:16y=22.4:6.4,解得x:y=1:1
成分:FeO
此时发生反应的化学方程式:Fe2O3+CO$\frac{\underline{\;高温\;}}{\;}$2FeO+CO2.
 实验室常用制取氧气的方法有:a.加热氯酸钾和二氧化锰粉末; b.加热高锰酸钾固体;c.用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生氧气.其实验装置如图所示.
实验室常用制取氧气的方法有:a.加热氯酸钾和二氧化锰粉末; b.加热高锰酸钾固体;c.用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生氧气.其实验装置如图所示. 某化学兴趣小组的同学用洁净的塑料瓶从一河流中取回一定量的水样,然后进行如下研究分析:
某化学兴趣小组的同学用洁净的塑料瓶从一河流中取回一定量的水样,然后进行如下研究分析: 测定空气中氧气含量的实验如图,回答问题:
测定空气中氧气含量的实验如图,回答问题: