12.空气是一种宝贵的自然资源.下列有关说法中错误的是( )
| A. | 法国化学家拉瓦锡研究了空气的成分,并得出氧气约占空气总体积$\frac{4}{5}$的结论 | |
| B. | 空气是由氮气、氧气、稀有气体、二氧化碳等物质组成的混合物 | |
| C. | 稀有气体都没有颜色、没有气味,在通电时能发出不同颜色的光 | |
| D. | 氮气是制造硝酸和氮肥的重要原料 |
11.如图所示的基本实验操作中正确的是( )
| A. | 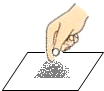 取用固体 | B. | 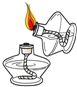 点燃酒精灯 | C. | 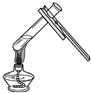 加热液体 | D. | 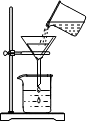 过滤 |
10.小丹同学在学习酸的性质时,从同一卷镁带中剪取相等的两根镁带,分别与室温下H+浓度相同的稀盐酸、稀硫酸反应.观察发现:镁带在稀盐酸中放出气泡的速率明显快于在稀硫酸中放出气泡的速率.
【查阅资料】
(1)金属与酸发生置换反应,其本质是金属单质与H+反应.
(2)生产H2速率主要取决于:①金属的表面积 ②溶液中H+浓度 ③温度等条件.
(3)H+的浓度与1L溶液中H+数目成正比.
(4)溶液中除H+外的其它离子可能会影响反应速率.
【提出问题】
①小丹同学在进行上述实验时,控制了镁带与酸反应的哪几个条件?(回答两条即可)金属的表面积,溶液中H+浓度;
②上述反应中Cl-、SO42-如何影响反应速率?
【猜想假设】
Ⅰ、Cl-促进了镁与酸的反应,SO42-对反应无影响.
Ⅱ、SO42-抑制了镁与酸的反应,Cl-对反应无影响.
Ⅲ、硫酸根抑制了镁与酸的反应,氯离子加速了镁与酸的反应.
请回答问题①,完成猜想Ⅲ.
【实验探究】
为了证明猜想,小丹设计了如下实验:
试剂B是NaCl(化学式)固体.
【结论】
结论A为钠离子、硫酸根离子对反应无影响.
【反思】
将试剂B改用HCl气体,不能达到实验目的,其原因是通入HCl气体时,形成盐酸增加了氢离子的浓度,改变了实验的条件.
【查阅资料】
(1)金属与酸发生置换反应,其本质是金属单质与H+反应.
(2)生产H2速率主要取决于:①金属的表面积 ②溶液中H+浓度 ③温度等条件.
(3)H+的浓度与1L溶液中H+数目成正比.
(4)溶液中除H+外的其它离子可能会影响反应速率.
【提出问题】
①小丹同学在进行上述实验时,控制了镁带与酸反应的哪几个条件?(回答两条即可)金属的表面积,溶液中H+浓度;
②上述反应中Cl-、SO42-如何影响反应速率?
【猜想假设】
Ⅰ、Cl-促进了镁与酸的反应,SO42-对反应无影响.
Ⅱ、SO42-抑制了镁与酸的反应,Cl-对反应无影响.
Ⅲ、硫酸根抑制了镁与酸的反应,氯离子加速了镁与酸的反应.
请回答问题①,完成猜想Ⅲ.
【实验探究】
为了证明猜想,小丹设计了如下实验:
| 实验编号 | 铝片长度 | H+浓度相同的酸 | 反应片刻后添加少量试剂 | 产生气泡的速率 | 结论 |
| A | 2cm | 5mL | Na2SO4固体 | 无明显变化 | (结论A) |
| B | 2cm | 5mL | (试剂B) | 明显变快 | Cl-对反应有促进作用 |
【结论】
结论A为钠离子、硫酸根离子对反应无影响.
【反思】
将试剂B改用HCl气体,不能达到实验目的,其原因是通入HCl气体时,形成盐酸增加了氢离子的浓度,改变了实验的条件.
6.下列反应中,氢离子实质上没有参加反应的是( )
0 151062 151070 151076 151080 151086 151088 151092 151098 151100 151106 151112 151116 151118 151122 151128 151130 151136 151140 151142 151146 151148 151152 151154 151156 151157 151158 151160 151161 151162 151164 151166 151170 151172 151176 151178 151182 151188 151190 151196 151200 151202 151206 151212 151218 151220 151226 151230 151232 151238 151242 151248 151256 211419
| A. | 镁与稀盐酸反应 | B. | 氧化铜与稀硫酸反应 | ||
| C. | 碳酸钙与稀盐酸反应 | D. | 硝酸银溶液与稀盐酸反应 |
 多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界.
多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界.