17.“洋河美酒飘香”,当走近洋河酒厂时就能闻到特殊的香味,这表明( )
| A. | 分子间有间隔 | |
| B. | 分子是保持物质化学性质的最小粒子 | |
| C. | 分子在不停地运动着 | |
| D. | 同种物质的性质相同 |
16.下列变化中属于化学变化的是( )
| A. | 石墨制成铅笔芯 | B. | 木炭使红墨水腿色 | ||
| C. | 生铁的冶炼 | D. | 食盐的溶解 |
14.化学兴趣小组的同学分成甲、乙两组对溶液的鉴别进行探究,请你分析并填空.
【实验目的】Na2CO3溶液、NaOH溶液、Ca(OH)2溶液、稀盐酸四种溶液的鉴别.
【实验药品】未贴标签的四瓶溶液[Na2CO3溶液、NaOH溶液、Ca(OH)2溶液、稀盐酸]和紫色石蕊试剂.
【实验仪器】试管、胶头滴管等.
【设计并实验】甲组同学利用紫色石蕊试剂鉴别四种溶液:
乙组同学经讨论认为,不用紫色石蕊试剂也能鉴别出四种溶液.各自分别做了如下实验:
乙组三位同学经过交流后发现本组小勇同学的结论是错误的,所滴加的溶液应是Ca(OH)2溶液,由此鉴别出了四种溶液.
【反应与体会】
①物质的鉴别有多种方法;
②鉴别物质的关键是利用物质的特征性质等.
【实验目的】Na2CO3溶液、NaOH溶液、Ca(OH)2溶液、稀盐酸四种溶液的鉴别.
【实验药品】未贴标签的四瓶溶液[Na2CO3溶液、NaOH溶液、Ca(OH)2溶液、稀盐酸]和紫色石蕊试剂.
【实验仪器】试管、胶头滴管等.
【设计并实验】甲组同学利用紫色石蕊试剂鉴别四种溶液:
| 实验操作和步骤 | 实验现象与结论 |
| (1)用4支试管,各取少量四种溶液,分别滴加紫色石蕊试剂; | 一支试管中溶液变为红色,则原溶液是稀盐酸. |
| (2)另用3支试管,各取少量未确定的三种溶液,分别滴加步骤(1)检验出的溶液. | 一支试管中溶液有气泡放出,则原溶液是Na2CO3溶液 |
| (3)另用2支试管,各取少量未确定的二种溶液,分别滴加步骤(2)检验出的溶液 | 一支试管溶液中有白色沉淀析出,则原溶液是Ca(OH)2溶液,其反应的化学方程式 为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;剩下的就是最后一种溶液. |
| 同学 | 实验操作 | 实现现象 | 结论 |
| 小红 | 用3支试管,各取少量三种溶液,分别滴加另一种溶液. | 一支试管溶液中有气泡放出,其余两支试管溶液中无现象. | 所滴加的溶液是稀盐酸. |
| 小勇 | 一支试管溶液中有白色沉淀析出,其余两支试管溶液中无现象. | 所滴加的溶液是Na2CO3溶液. | |
| 小新 | 三支试管溶液中都无现象. | 所滴加的溶液是NaOH溶液 |
【反应与体会】
①物质的鉴别有多种方法;
②鉴别物质的关键是利用物质的特征性质等.
13.某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖.对于该溶液是否变质,同学们开始实验探究.
【猜想假设】猜想
(1)该溶液没有变质,为NaOH溶液.
(2)该溶液全部变质,为Na2CO3溶液.
(3)该溶液部分变质,为NaOH和Na2CO3的混合溶液.
【查阅资料】Na2CO3溶液呈碱性
【设计方案】请你完善下表几组同学探讨的设计方案
【探究实验】综合各小组的方案后,动手实验.
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存.
【拓展延伸】同学们设计了下列两套装置进行实验:
用胶头滴管吸取某种液体,锥形瓶中充入一种气体或放入一种固体物质,挤压胶头滴管.一段时间后,两装置中气球明显胀大.
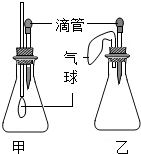
(1)甲装置中可能发生反应的方程式是2NaOH+CO2═Na2CO3+H2O.
(2)若乙装置中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是铁.
【猜想假设】猜想
(1)该溶液没有变质,为NaOH溶液.
(2)该溶液全部变质,为Na2CO3溶液.
(3)该溶液部分变质,为NaOH和Na2CO3的混合溶液.
【查阅资料】Na2CO3溶液呈碱性
【设计方案】请你完善下表几组同学探讨的设计方案
| 1 | 实验操作 | 可能出现的现象与结论 | 同学评价 |
| 第1组 | 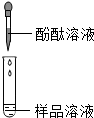 | 若溶液变红,则猜想(2)不成立 | 第2组同学认为:此方案结论不正确,理由是:碳酸钠溶液能使酚酞试液变红色. |
| 第2组 | 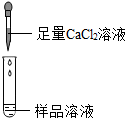 | 若产生白色沉淀,反应方程式是:Na2CO3+CaCl2═CaCO3↓+2NaCl,则猜想(1)不成立. | 第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立. |
| 第3组 | 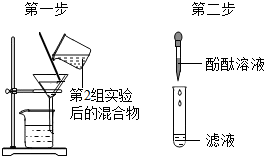 | 若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立. | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是:第2组实验结束后,静置一会儿后,滴加酚酞试液,酚酞试液变红色,说明猜想(3)成立 |
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存.
【拓展延伸】同学们设计了下列两套装置进行实验:
用胶头滴管吸取某种液体,锥形瓶中充入一种气体或放入一种固体物质,挤压胶头滴管.一段时间后,两装置中气球明显胀大.

(1)甲装置中可能发生反应的方程式是2NaOH+CO2═Na2CO3+H2O.
(2)若乙装置中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是铁.
12.复习时,老师引导我们回顾了几个探究实验.
探究1:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
探究2:在化学实验室里,小亮发现有一瓶敞口的标有固体NaOH的药品,已变成了白色粉末,他大胆的猜想并设计如下实验进行验证,请一起完成:
[提出假设]:白色粉末可能是:①NaOH ②Na2CO3③NaOH与Na2CO3混合物
【部分实验用品】:稀盐酸,BaCl2溶液、澄清石灰水、酚酞试液、PH试纸(供选)
探究1:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入锌粒 | 有气泡生成 | 证明研究结论正确 |
[提出假设]:白色粉末可能是:①NaOH ②Na2CO3③NaOH与Na2CO3混合物
【部分实验用品】:稀盐酸,BaCl2溶液、澄清石灰水、酚酞试液、PH试纸(供选)
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| ①取少量白色粉末,滴加稀盐酸溶液 | 有气体生成 | 该白色粉末中一定含有碳酸钠 |
| ②另取少量白色粉末溶于水,滴加酚酞 溶液 | 溶液变红色 | 表明溶液呈碱性性,结合实验步骤①可推知假设中②或③均可能成立. |
| ③另取少量白色粉末来溶于水,滴加氯化钡溶液直到不再产生沉淀为止.过滤,取少量滤液用酚酞试液来实验. | 酚酞试液没有变色 | 该白色粉末一定是Na2CO3 |
10.学习热情和学习方法是成才的必备条件,灵活掌握不同的学习方法可以取得事半功倍的效果.请用以下方法解决下列问题:
(1)分类法:利用下列4组物质
A.ZnO、MgO、CO2、Na2O B.Cu、N2、O2、Cl2
C.KNO3、NaHCO3、KClO3、Fe(OH)3 D.H2SO4、H2O、HCl、HNO3
请按要求填写下表空白(填写物质的化学式或分类标准)
(2)对比法: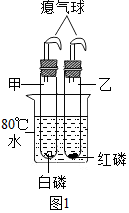
A.通过对CO2+H2O═H2CO3;6CO2+6H2O$\frac{\underline{\;光照\;}}{\;}$ C6H12O6+6O2两个化学反应的对比,你能得出的结论是相同的反应物在不同的反应条件下生成的产物可能不同.
B.如图1所示:小海同学将盛有干燥白磷的甲试管和干燥红磷的乙试管插入盛有80℃的烧杯里(甲、乙试管均套有气球密封).过一会后,发现甲试管中的白磷燃烧,乙试管中的红磷没有燃烧.请根据小海同学的实验现象,对比得出可燃物燃烧所需的条件之一:可燃物温度达到着火点.
(3)归纳演绎法:
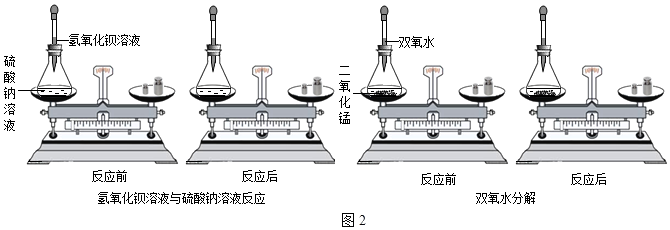
小海同学通过对大量化学反应如氢氧化钡溶液与硫酸钠溶液,双氧水分解(如图2)反应前后各物质的质量总和的测定,得出参加化学反应的各物质的质量总和等于(填“大于”、“小于”或“等于”)反应后生成的各种物质的质量总和.
根据小海得出的结论,可推出7.9g高锰酸钾加热一会后,剩余固体质量为7.5g,则反应生成氧气的质量为0.4g.
0 151040 151048 151054 151058 151064 151066 151070 151076 151078 151084 151090 151094 151096 151100 151106 151108 151114 151118 151120 151124 151126 151130 151132 151134 151135 151136 151138 151139 151140 151142 151144 151148 151150 151154 151156 151160 151166 151168 151174 151178 151180 151184 151190 151196 151198 151204 151208 151210 151216 151220 151226 151234 211419
(1)分类法:利用下列4组物质
A.ZnO、MgO、CO2、Na2O B.Cu、N2、O2、Cl2
C.KNO3、NaHCO3、KClO3、Fe(OH)3 D.H2SO4、H2O、HCl、HNO3
请按要求填写下表空白(填写物质的化学式或分类标准)
| A | B | C | D | |
| 分类标准 | 金属氧化物 | ② | 盐 | ④ |
| 不属于该类别的物质 | ① | Cu | ③ | H2O |

A.通过对CO2+H2O═H2CO3;6CO2+6H2O$\frac{\underline{\;光照\;}}{\;}$ C6H12O6+6O2两个化学反应的对比,你能得出的结论是相同的反应物在不同的反应条件下生成的产物可能不同.
B.如图1所示:小海同学将盛有干燥白磷的甲试管和干燥红磷的乙试管插入盛有80℃的烧杯里(甲、乙试管均套有气球密封).过一会后,发现甲试管中的白磷燃烧,乙试管中的红磷没有燃烧.请根据小海同学的实验现象,对比得出可燃物燃烧所需的条件之一:可燃物温度达到着火点.
(3)归纳演绎法:
小海同学通过对大量化学反应如氢氧化钡溶液与硫酸钠溶液,双氧水分解(如图2)反应前后各物质的质量总和的测定,得出参加化学反应的各物质的质量总和等于(填“大于”、“小于”或“等于”)反应后生成的各种物质的质量总和.
根据小海得出的结论,可推出7.9g高锰酸钾加热一会后,剩余固体质量为7.5g,则反应生成氧气的质量为0.4g.

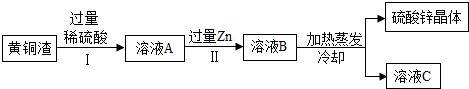
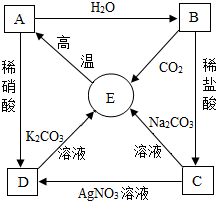 A~E均为初中化学常见物质,A、B、C、D、E均含有同一种元素,B常用于改良酸性土壤.它们之间的相互转化关系如图所示:(图中“→”表示物质间存在转化关系,部分生成物已略去).请回答下列问题:
A~E均为初中化学常见物质,A、B、C、D、E均含有同一种元素,B常用于改良酸性土壤.它们之间的相互转化关系如图所示:(图中“→”表示物质间存在转化关系,部分生成物已略去).请回答下列问题: