6.某实验小组的同学用碳酸钠粉末、粒状大理石、稀盐酸、浓盐酸、稀硫酸这几种药品,探究哪两种药品的反应适合在实验室制取CO2.请你参与下列的探究并回答问题.
【提出问题】上述哪两种物质的反应最适合在实验室制取CO2?
【查阅资料】1.常温下,纯净的浓盐酸是无色、有酸味和刺激性气味;它具有很强的挥发性(挥发出氯化氢气体).
2稀硫酸与碳酸钙反应,生成微溶于水的硫酸钙.
【方案设计】大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO2,你认为原因浓盐酸易挥发,使制出的CO2不纯.
讨论后大家设计了如下三个实验进行对比分析.

【实验与结论】(1)请你填写实验报告中①、②处的内容.
(2)根据探究结论,实验室制取二氧化碳的反应原理为盐酸+碳酸钙─→氯化钙+水+二氧化碳 ( 用文字表达式表示).
【拓展与迁移】由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等.请你再写出一种需要考虑的因素:制出的气体要纯净.
【提出问题】上述哪两种物质的反应最适合在实验室制取CO2?
【查阅资料】1.常温下,纯净的浓盐酸是无色、有酸味和刺激性气味;它具有很强的挥发性(挥发出氯化氢气体).
2稀硫酸与碳酸钙反应,生成微溶于水的硫酸钙.
【方案设计】大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO2,你认为原因浓盐酸易挥发,使制出的CO2不纯.
讨论后大家设计了如下三个实验进行对比分析.

【实验与结论】(1)请你填写实验报告中①、②处的内容.
| 实验 | 实验现象 | 实验内容 |
| A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
| B | 产生气泡,速率迅速减慢,反应几乎停止. | 无法持续产生CO2,不能用于实验室制取CO2 |
| C | ①持续均匀产生气泡 | ②反应速率适中,便于收集,适合实验室制取二氧化碳 |
【拓展与迁移】由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等.请你再写出一种需要考虑的因素:制出的气体要纯净.
3.化学实验是学习化学的基础,请根据下列装置图回答问题.

(1)写出仪器a、b的名称长颈漏斗;b锥形瓶.
(2)写出A图中产生气体的反应文字表达式碳酸钙+盐酸→氯化钙+水+二氧化碳.
(3)B图中,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛先熄灭,说明二氧化碳具有不可燃、不支持燃烧和密度比空气大性质.这一性质在实际生活中的应用是灭火.
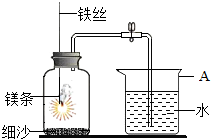
(4)小明按C图实验时,集气瓶炸裂了,其可能的原因是燃着的铁丝碰到集气瓶壁.
(5)小明对铁丝在氧气中燃烧为什么会火星四射进行探究.下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录.请你分析回答:①含碳0.6%的铁丝在氧气中燃烧的实验现象剧烈燃烧,火星四射;②产生不同现象的原因是铁丝中含有的碳引起的.

(1)写出仪器a、b的名称长颈漏斗;b锥形瓶.
(2)写出A图中产生气体的反应文字表达式碳酸钙+盐酸→氯化钙+水+二氧化碳.
(3)B图中,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛先熄灭,说明二氧化碳具有不可燃、不支持燃烧和密度比空气大性质.这一性质在实际生活中的应用是灭火.
(4)小明按C图实验时,集气瓶炸裂了,其可能的原因是燃着的铁丝碰到集气瓶壁.
(5)小明对铁丝在氧气中燃烧为什么会火星四射进行探究.下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录.请你分析回答:①含碳0.6%的铁丝在氧气中燃烧的实验现象剧烈燃烧,火星四射;②产生不同现象的原因是铁丝中含有的碳引起的.
| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | (未填) |
2. (1)向容积为250mL的细颈玻璃仪器A中加水至虚线处,再滴几滴红墨水,一段时间后,A中的现象是整瓶水变红,说明分子在不断的运动.
(1)向容积为250mL的细颈玻璃仪器A中加水至虚线处,再滴几滴红墨水,一段时间后,A中的现象是整瓶水变红,说明分子在不断的运动.
(2)继续向A中加酒精至凹液面最低处正好与刻度线相切.塞紧玻璃塞,将A中液体倒转摇匀,重复2次.静置一段时间后,A中的现象为液面要低于刻度线且距离较远,说明分子间存在间隔.仪器A细颈部的作用是便于观察液面的变化.
(3)请你选择以上其中一点性质,重新设计一个实验进行研究.请完成下表
 (1)向容积为250mL的细颈玻璃仪器A中加水至虚线处,再滴几滴红墨水,一段时间后,A中的现象是整瓶水变红,说明分子在不断的运动.
(1)向容积为250mL的细颈玻璃仪器A中加水至虚线处,再滴几滴红墨水,一段时间后,A中的现象是整瓶水变红,说明分子在不断的运动.(2)继续向A中加酒精至凹液面最低处正好与刻度线相切.塞紧玻璃塞,将A中液体倒转摇匀,重复2次.静置一段时间后,A中的现象为液面要低于刻度线且距离较远,说明分子间存在间隔.仪器A细颈部的作用是便于观察液面的变化.
(3)请你选择以上其中一点性质,重新设计一个实验进行研究.请完成下表
| 实验步骤 | 实验现象 | 实验结论 |
| 将少量香水喷洒在室内 | 过一会儿,整个室内都闻到香水气味 | 分子是不断运动的 |
20.下列说法中正确的是( )
0 150644 150652 150658 150662 150668 150670 150674 150680 150682 150688 150694 150698 150700 150704 150710 150712 150718 150722 150724 150728 150730 150734 150736 150738 150739 150740 150742 150743 150744 150746 150748 150752 150754 150758 150760 150764 150770 150772 150778 150782 150784 150788 150794 150800 150802 150808 150812 150814 150820 150824 150830 150838 211419
| A. | 相对原子质量是一个比值,单位为克 | |
| B. | 原子是化学变化中的最小微粒 | |
| C. | 所有原子都是由质子、中子和核外电子构成的 | |
| D. | 一切物质都是由分子构成的 |
 .
. 某校研究性学习小组探究空气中氧气的体积分数,他们想选用以下药品进行实验:①木炭;②红磷;③铁丝;④镁条.
某校研究性学习小组探究空气中氧气的体积分数,他们想选用以下药品进行实验:①木炭;②红磷;③铁丝;④镁条.