13.小明在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.
[探究目的]探究所得溶液的酸碱性.
[提出猜想]所得溶液可能呈酸性,也可能呈中性,还可能呈酸性.
[实验验证]
[分析与思考]
(1)用pH试纸可以粗略地测出溶液的酸碱度.
(2)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小明对所得溶液进行了如下处理:向溶液中逐滴加入硫酸铜溶液,并发生了反应,直到不产生沉淀为止.然后过滤,把滤液倒入蒸发皿进行加热蒸发溶剂,得到NaCl晶体.上述产生沉淀的化学方程式CuSO4+2NaOH═Cu(OH)2↓+Na2SO4.
(3)若无色酚酞试液变不色,为了进一步确定溶液的酸碱性,小明提出了以下方案:
方案一:取样,加入Na2CO3溶液,若观察到有气泡产生,则所取的溶液呈酸性;若无明显现象,则溶液呈中性.
方案二:取样,加入铁屑,若有大量气泡产生,则所取的溶液呈酸性;该反应的化学方程式为Fe+2HCl═FeCl2+H2↑;若无明显现象,则溶液呈中性.
方案三:…
0 150634 150642 150648 150652 150658 150660 150664 150670 150672 150678 150684 150688 150690 150694 150700 150702 150708 150712 150714 150718 150720 150724 150726 150728 150729 150730 150732 150733 150734 150736 150738 150742 150744 150748 150750 150754 150760 150762 150768 150772 150774 150778 150784 150790 150792 150798 150802 150804 150810 150814 150820 150828 211419
[探究目的]探究所得溶液的酸碱性.
[提出猜想]所得溶液可能呈酸性,也可能呈中性,还可能呈酸性.
[实验验证]
| 实验操作 | 实验现象 | 结 论 |
| 用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 | 若无色酚酞试液变红色. | 溶液呈碱性; |
| 若无色酚酞试液变不色. | 溶液呈中性或酸性; |
(1)用pH试纸可以粗略地测出溶液的酸碱度.
(2)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小明对所得溶液进行了如下处理:向溶液中逐滴加入硫酸铜溶液,并发生了反应,直到不产生沉淀为止.然后过滤,把滤液倒入蒸发皿进行加热蒸发溶剂,得到NaCl晶体.上述产生沉淀的化学方程式CuSO4+2NaOH═Cu(OH)2↓+Na2SO4.
(3)若无色酚酞试液变不色,为了进一步确定溶液的酸碱性,小明提出了以下方案:
方案一:取样,加入Na2CO3溶液,若观察到有气泡产生,则所取的溶液呈酸性;若无明显现象,则溶液呈中性.
方案二:取样,加入铁屑,若有大量气泡产生,则所取的溶液呈酸性;该反应的化学方程式为Fe+2HCl═FeCl2+H2↑;若无明显现象,则溶液呈中性.
方案三:…
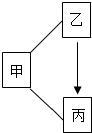 甲、乙、丙是初中化学中常见的物质,其转化关系如图所示(反应条件已省 略).若乙是相对分子质量最小的氧化物,甲、乙均由两种相同的元素组成,请写出实验室由甲制取丙的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
甲、乙、丙是初中化学中常见的物质,其转化关系如图所示(反应条件已省 略).若乙是相对分子质量最小的氧化物,甲、乙均由两种相同的元素组成,请写出实验室由甲制取丙的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.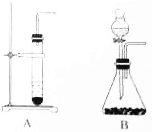
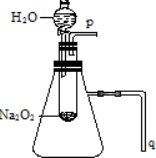 用脱脂棉包住约0.2g过氧化钠粉末.置于石棉网上.往脱酯棉上滴水.可观察到脱脂棉剧烈燃烧起来
用脱脂棉包住约0.2g过氧化钠粉末.置于石棉网上.往脱酯棉上滴水.可观察到脱脂棉剧烈燃烧起来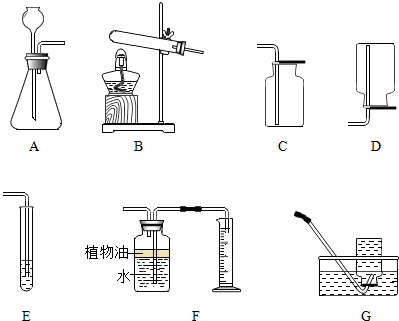
 如图是某品牌矿物质水的标签,则:
如图是某品牌矿物质水的标签,则: