14. 暖贴的发热材料主要由铁粉、活性炭、食盐、水等物质构成.
暖贴的发热材料主要由铁粉、活性炭、食盐、水等物质构成.
【提出问题】
发热材料中各主要物质起到了什么作用?
【猜想与假设】
Ⅰ.铁粉生锈,发生氧化反应,放出热量.
Ⅱ.活性炭能加快铁粉氧化的速率.
Ⅲ.食盐能加快铁粉氧化的速率.
【进行实验】
【解释与结论】
(1)铁生锈的条件是与水和氧气并存.
(2)已知铁粉在一定条件下生锈,发生氧化反应的产物可能是Fe(OH)3,该反应的化学方程式为4Fe+6H2O+3O2=4Fe(OH)3.
(3)分析2(填实验编号)数据,可证明猜想与假设Ⅱ正确.
(4)分析实验组4与对照组数据,可证明猜想与假设Ⅲ正确.请填写表中空缺数据.
【反思与评价】
(5)某同学认为没有必要进行实验组1,你是否同意他的观点并说明理由不同意,实验1的目的是想证明没有铁,活性炭和食盐与水混合不会放热.
(6)某同学质疑此实验中忽略了发热材料中的水.你认为分析3(填实验编号)的数据,可证明水的作用.
 暖贴的发热材料主要由铁粉、活性炭、食盐、水等物质构成.
暖贴的发热材料主要由铁粉、活性炭、食盐、水等物质构成.【提出问题】
发热材料中各主要物质起到了什么作用?
【猜想与假设】
Ⅰ.铁粉生锈,发生氧化反应,放出热量.
Ⅱ.活性炭能加快铁粉氧化的速率.
Ⅲ.食盐能加快铁粉氧化的速率.
【进行实验】
| 实验编号 | 实验药品及用量 | 反应时间 /min | 温度上升值/°C | ||||
| 铁粉/g | 活性炭/g | 食盐/g | 水/g | ||||
| 对照组 | 1 | 0.2 | 0.1 | 5 | 10 | 58 | |
| 实 验 组 | 1 | 0 | 0.2 | 0.1 | 5 | 10 | 0 |
| 2 | 1 | 0 | 0.1 | 5 | 10 | 2.7 | |
| 3 | 1 | 0.2 | 0.1 | 0 | 10 | 4.5 | |
| 4 | 10 | 20 | |||||
(1)铁生锈的条件是与水和氧气并存.
(2)已知铁粉在一定条件下生锈,发生氧化反应的产物可能是Fe(OH)3,该反应的化学方程式为4Fe+6H2O+3O2=4Fe(OH)3.
(3)分析2(填实验编号)数据,可证明猜想与假设Ⅱ正确.
(4)分析实验组4与对照组数据,可证明猜想与假设Ⅲ正确.请填写表中空缺数据.
【反思与评价】
(5)某同学认为没有必要进行实验组1,你是否同意他的观点并说明理由不同意,实验1的目的是想证明没有铁,活性炭和食盐与水混合不会放热.
(6)某同学质疑此实验中忽略了发热材料中的水.你认为分析3(填实验编号)的数据,可证明水的作用.
12.小明同学对一种“汽泡爽”的冲调饮料进行了实验探究.
【饮料说明】
①主要原料:柠檬酸(C6H8O7)和小苏打(NaHCO3);
②使用说明:将一包“汽泡爽”粉末倒入玻璃杯中,加入200mL冷水,看到有大量气泡快速生成,待粉末完全溶解,就得到一杯果味饮料.
小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响.
【实验一】探究“汽泡爽”产生气体的成分.
(1)小明阅读资料发现:“汽泡爽”原料中的柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3X↑,则X的化学式是CO2,为了检验该气体,小明应选择的试剂是澄清石灰水.
(2)如果实验室以柠檬酸和小苏打粉末混合后加水反应制取X气体,可以选择的发生装置是B(选填图1装置编号,下同),收集装置是C.
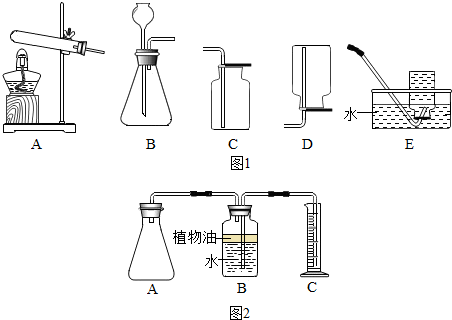
【实验二】探究加水温度对产生气体量的影响.
(1)小明先用冷水和热水各冲了一杯饮料,品尝时发现冷水冲的饮料中气泡较多,热水冲的饮料中气泡较少.他查阅资料发现:随着温度升高,气体在一定量的水中溶解的量会迅速降低.于是小明设计了如下对比实验方案,请填写表中空白.
(2)在老师的帮助下,小明采用相同的两套实验装置(如图2),编号为1、2,分别完成上述实验,在A中先加入水,再分别加入相同规格的一袋“汽泡爽”,迅速塞紧胶塞.量筒C用于收集A中产生的气体所排出的液体.B中油层的作用是防止二氧化碳溶解在B装置的水中.
(3)通过实验,小明测得:a=64mL,b=132mL,由此获得结论:“汽泡爽”产生气体的量与加水温度有关系.但是老师看到小明的实验报告后却指出,一包“汽泡爽”产生气体的量与反应物(柠檬酸和小苏打)的量有关,实验中小明所用的反应物量相等,产生气体的总量应该近似相等.请分析小明测得该组数据a、b相差较大的可能原因温度高气体在水中的溶解度小,收集到的气体多.
(4)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是将装置1反应后的液体温度升高到50℃,继续收集气体并测量体积.
【饮料说明】
①主要原料:柠檬酸(C6H8O7)和小苏打(NaHCO3);
②使用说明:将一包“汽泡爽”粉末倒入玻璃杯中,加入200mL冷水,看到有大量气泡快速生成,待粉末完全溶解,就得到一杯果味饮料.
小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响.
【实验一】探究“汽泡爽”产生气体的成分.
(1)小明阅读资料发现:“汽泡爽”原料中的柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3X↑,则X的化学式是CO2,为了检验该气体,小明应选择的试剂是澄清石灰水.
(2)如果实验室以柠檬酸和小苏打粉末混合后加水反应制取X气体,可以选择的发生装置是B(选填图1装置编号,下同),收集装置是C.

【实验二】探究加水温度对产生气体量的影响.
(1)小明先用冷水和热水各冲了一杯饮料,品尝时发现冷水冲的饮料中气泡较多,热水冲的饮料中气泡较少.他查阅资料发现:随着温度升高,气体在一定量的水中溶解的量会迅速降低.于是小明设计了如下对比实验方案,请填写表中空白.
| 装置编号 | 加入水的体积 | 加入水的温度 | 收集到的气体的体积 |
| 1 | 200mL | 15℃ | a(待记录) |
| 2 | 200mL | 50℃ | b(待记录) |
(3)通过实验,小明测得:a=64mL,b=132mL,由此获得结论:“汽泡爽”产生气体的量与加水温度有关系.但是老师看到小明的实验报告后却指出,一包“汽泡爽”产生气体的量与反应物(柠檬酸和小苏打)的量有关,实验中小明所用的反应物量相等,产生气体的总量应该近似相等.请分析小明测得该组数据a、b相差较大的可能原因温度高气体在水中的溶解度小,收集到的气体多.
(4)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是将装置1反应后的液体温度升高到50℃,继续收集气体并测量体积.
10.厨房内有一瓶无标签的无色溶液,经①闻气味、②尝味道,初步确定其为白醋.白醋中含有的醋酸是一种酸,具有酸的通性.为了进一步了解醋酸的性质,请你与小文同学一起探究:
[提出问题]醋酸能与哪些不同类别的物质反应呢?
[猜想]
①活泼金属;
②碳酸盐;
③碱.(填物质类别不要填具体物质)
[设计实验]请你选用家中能找到的物质验证你的一种猜想.
[应用]黄蜂毒刺呈碱性,若人被黄蜂蜇了,可用白醋涂在皮肤上.其利用了醋酸能与碱性物质反应的性质.
[继续探究]根据生活经验,有关白醋(酸的通性除外)你还想探究什么问题?做鱼时为什么要放白醋?.
[提出问题]醋酸能与哪些不同类别的物质反应呢?
[猜想]
①活泼金属;
②碳酸盐;
③碱.(填物质类别不要填具体物质)
[设计实验]请你选用家中能找到的物质验证你的一种猜想.
| 实验步骤 | 实验现象 | 结论 |
[继续探究]根据生活经验,有关白醋(酸的通性除外)你还想探究什么问题?做鱼时为什么要放白醋?.
8.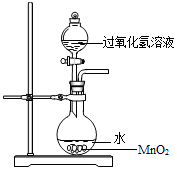 用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:
用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:
猜想1:加水可以起到稀释的作用,使反应速度变缓. 猜想2:…
并根据猜想进行了实验:每次取15毫升15%的过氧化氢溶液,稀释成不同溶质质量分数,在其他条件相同的情况下进行实验.记录数据如下:
(1)实验室用过氧化氢制氧气的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)过氧化氢溶液的溶质质量分数对反应速度有怎样的影响?一定范围内,过氧化氢溶质质量分数越大反应速度越快.
(3)根据表中数据可知,该同学的猜想2是:加水可以给溶液降温.
 用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:
用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:猜想1:加水可以起到稀释的作用,使反应速度变缓. 猜想2:…
并根据猜想进行了实验:每次取15毫升15%的过氧化氢溶液,稀释成不同溶质质量分数,在其他条件相同的情况下进行实验.记录数据如下:
| 实验 | 1 | 2 | 3 | 4 | 5 |
| 过氧化氢溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% |
| MnO2粉末用量/克 | 0.5 | 0.5 | 0.5 | 0.5 | 0.5 |
| 收集到500mL气体时所用时间/秒 | 560 | 186 | 103 | 35 | 12 |
| 反应后液体温度/℃ | 26 | 38 | 43 | 59 | 71 |
(2)过氧化氢溶液的溶质质量分数对反应速度有怎样的影响?一定范围内,过氧化氢溶质质量分数越大反应速度越快.
(3)根据表中数据可知,该同学的猜想2是:加水可以给溶液降温.
7.化学实验是学习化学的基础,请根据下列装置图回答问题.
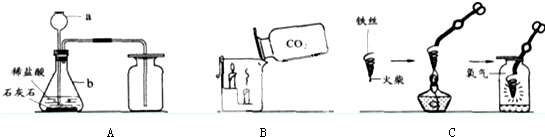
(1)写出仪器a、b的名称长颈漏斗;b锥形瓶.
(2)写出A图中产生气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)B图中,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层先灭,说明二氧化碳具有不能燃烧、不支持燃烧和密度比空气大性质.这一性质在实际生活中的应用为灭火.
(4)C图中螺旋状铁丝的末端系一根火柴的作用是引燃铁丝.
(5)小明按C图实验时,集气瓶炸裂了,其可能的原因是燃着的铁丝碰到集气瓶壁.
(6)小明对铁丝在氧气中燃烧为什么会火星四射进行探究.下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录.请你分析回答:
铁丝在氧气中燃烧产生火星四射的原因是碳与氧气或熔融状态的铁的氧化物反应生成二氧化碳气体,二氧化碳气体体积迅速膨胀,推动周围的呈熔融状态的铁及其氧化物向四周飞溅.

(1)写出仪器a、b的名称长颈漏斗;b锥形瓶.
(2)写出A图中产生气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)B图中,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层先灭,说明二氧化碳具有不能燃烧、不支持燃烧和密度比空气大性质.这一性质在实际生活中的应用为灭火.
(4)C图中螺旋状铁丝的末端系一根火柴的作用是引燃铁丝.
(5)小明按C图实验时,集气瓶炸裂了,其可能的原因是燃着的铁丝碰到集气瓶壁.
(6)小明对铁丝在氧气中燃烧为什么会火星四射进行探究.下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录.请你分析回答:
| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 剧烈燃烧,大量火星 |
6.南京市国民经济和社会发展第“十二五”规划纲要指出,要做强做优电子信息等工业支柱产业.硅(Si)是信息技术的关键材料,常用以下方法制得纯硅,如图所示:

(1)图中①、③发生了置换反应,②发生了化合反应.写出②和③的化学反应方程式:
②Si+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4;③SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl.
(2)完成一种表示置换反应的通式:单质(I)+化合物(I)=单质(Ⅱ)+化合物(Ⅱ).
根据已学知识填表:
0 150579 150587 150593 150597 150603 150605 150609 150615 150617 150623 150629 150633 150635 150639 150645 150647 150653 150657 150659 150663 150665 150669 150671 150673 150674 150675 150677 150678 150679 150681 150683 150687 150689 150693 150695 150699 150705 150707 150713 150717 150719 150723 150729 150735 150737 150743 150747 150749 150755 150759 150765 150773 211419

(1)图中①、③发生了置换反应,②发生了化合反应.写出②和③的化学反应方程式:
②Si+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4;③SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl.
(2)完成一种表示置换反应的通式:单质(I)+化合物(I)=单质(Ⅱ)+化合物(Ⅱ).
根据已学知识填表:
| 单质(I) | 单质(Ⅱ) | 相应的置换反应的化学方程式(各举一例) | |
| A | 金属 | 非金属 | |
| B | 金属(I) | 金属(Ⅱ) | |
| C | 非金属 | 金属 | |
| D | SiO2+2C$\frac{\underline{\;高温、电炉\;}}{\;}$Si+2CO↑ |
 物质之间发生化学反应时常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.
物质之间发生化学反应时常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验. “化学反应条件的控制是实验的灵魂”,某校科学兴趣小组在老师指导下,进行了“影响比较金属活动性因素”的实验,请你帮助回答下列问题:
“化学反应条件的控制是实验的灵魂”,某校科学兴趣小组在老师指导下,进行了“影响比较金属活动性因素”的实验,请你帮助回答下列问题: