17.小红、小军、小明三人化学学习小组在实验中,用到了三个分别盛有KCl溶液、KOH溶液、K2SO4溶液的滴瓶.
小军发现小红将三个滴瓶中的三只滴管混用,认为小红实验操作不规范,滴瓶中的试剂会因此受污染而无法再次使用,学习小组就盛有KCl溶液的滴瓶是否被另外两种试剂污染进行了如下探究.
提出问题:该滴瓶中溶质的成分是什么?
提出猜想:通过分析,提出如下猜想:
猜想Ⅰ溶质成分只有:KCl;
猜想Ⅱ溶质成分为:KCl和KOH;
猜想Ⅲ溶质成分为:KCl、K2SO4;
猜想Ⅳ溶质成分为:KCl、KOH和K2SO4.
实验探究:为证明猜想,小军设计了如下实验方案,请你一起完成下列实验报告;
实验反思:小明认为该实验方案并未证明猜想Ⅱ、Ⅲ是否成立,应补充相应实验予以证明,你是否赞同?否(选填“是”或“否”).
小军发现小红将三个滴瓶中的三只滴管混用,认为小红实验操作不规范,滴瓶中的试剂会因此受污染而无法再次使用,学习小组就盛有KCl溶液的滴瓶是否被另外两种试剂污染进行了如下探究.
提出问题:该滴瓶中溶质的成分是什么?
提出猜想:通过分析,提出如下猜想:
猜想Ⅰ溶质成分只有:KCl;
猜想Ⅱ溶质成分为:KCl和KOH;
猜想Ⅲ溶质成分为:KCl、K2SO4;
猜想Ⅳ溶质成分为:KCl、KOH和K2SO4.
实验探究:为证明猜想,小军设计了如下实验方案,请你一起完成下列实验报告;
| 实验操作 | 实验现象 | 结论或解释 |
| (1)取该滴瓶内溶液烧了于试管中,向试管中加入适量BaCl2溶液 | 产生白色沉淀 | 该反应的化学方程式为BaCl2+K2SO4═BaSO4↓+2KCl |
| (2)将上述反应后的混合液过滤,取滤液于另一支试管中,向该试管中加入酚酞试液 | 酚酞试液变红色 | 证明猜想Ⅳ成立 |
15.有一类化合物其化学式可表示为CnH2n+2(n≥l,n为正整数),这类化合物统称为烷烃,下列有关烷烃的说法中,正确的是( )
| A. | 甲烷(CH4)是最简单的烷烃 | |
| B. | 烷烃在空气中燃烧时,一定只生成二氧化碳和水 | |
| C. | 烷烃都属于有机高分子化合物 | |
| D. | 烷烃中碳元素的质量分数随n的增大而变小 |
11.钢铁工业是国家工业的基础.
(1)图1是教材中炼铁高炉及炉内化学变化过程示意图,根据图示回答问题.若图1中采用的铁矿石的主要成分为氧化铁,请写出A区和B区所发生主要反应的化学方程式:A区Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;B区(焦炭的作用)C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2、CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(2)某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究.
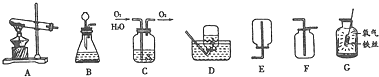
[设计实验]用一氧化碳还原纯净的氧化铁 粉末,实验装置如图2.

[进行实验]该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g) ②反
应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量).
[分析与讨论]本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
[查阅资料]
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁.
③四氧化三铁、铁粉都能被磁铁吸引,而氧化亚铁、氧化铁均不能被磁铁吸引.
[实验与猜想]
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁.
②进行猜想:黑色固体粉末可能
a.全部为铁 b.全部是四氧化三铁 c.铁与四氧化三铁的混合物.
[得出结论]
通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称)四氧化三铁.
计算过程:
[反思与评价]
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图中采用虚线框内的装置,其作用有A、B.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
(1)图1是教材中炼铁高炉及炉内化学变化过程示意图,根据图示回答问题.若图1中采用的铁矿石的主要成分为氧化铁,请写出A区和B区所发生主要反应的化学方程式:A区Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;B区(焦炭的作用)C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2、CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(2)某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究.
[设计实验]用一氧化碳还原纯净的氧化铁 粉末,实验装置如图2.

[进行实验]该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g) ②反
应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量).
[分析与讨论]本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
[查阅资料]
| 物质 性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁.
③四氧化三铁、铁粉都能被磁铁吸引,而氧化亚铁、氧化铁均不能被磁铁吸引.
[实验与猜想]
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁.
②进行猜想:黑色固体粉末可能
a.全部为铁 b.全部是四氧化三铁 c.铁与四氧化三铁的混合物.
[得出结论]
通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称)四氧化三铁.
计算过程:
[反思与评价]
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图中采用虚线框内的装置,其作用有A、B.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
9.在一定条件下,向一密闭容器内加入ABCD四种物质各20克,充分反应后测定其质量,得到数据如下,回答下列有关问题:
(1)这一反应类型是化合反应,未知值为16.
(2)由表中数据分析可知,A可能没有参加化学反应,也可能是该反应的催化剂.
(3)写出一例与上述反应类型的反应化学方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
0 150558 150566 150572 150576 150582 150584 150588 150594 150596 150602 150608 150612 150614 150618 150624 150626 150632 150636 150638 150642 150644 150648 150650 150652 150653 150654 150656 150657 150658 150660 150662 150666 150668 150672 150674 150678 150684 150686 150692 150696 150698 150702 150708 150714 150716 150722 150726 150728 150734 150738 150744 150752 211419
| 物质 | A | B | C | D |
| 反应前质量(克) | 20 | 20 | 20 | 20 |
| 反应后质量(克) | 20 | 30 | 未知 | 14 |
(2)由表中数据分析可知,A可能没有参加化学反应,也可能是该反应的催化剂.
(3)写出一例与上述反应类型的反应化学方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.


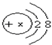 ,若X等于11,则该微粒表示阳(填“阳”或“阴”)离子.在N、N2、2N2三种符号中,只表示微观意义,而不表示宏观意义的是2N2.
,若X等于11,则该微粒表示阳(填“阳”或“阴”)离子.在N、N2、2N2三种符号中,只表示微观意义,而不表示宏观意义的是2N2.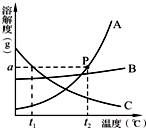 A、B、C三种物质的溶解度曲线如图所示.
A、B、C三种物质的溶解度曲线如图所示.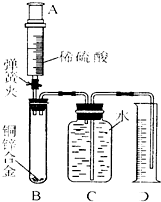 某化学小组利用图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去).探究过程如下:
某化学小组利用图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去).探究过程如下: