8.下列叙述中,正确的是( )
| A. | 溶液是由一种溶质和溶剂组成的混合物 | |
| B. | 液态空气不是混合物 | |
| C. | 凡是均一透明的液体就是溶液 | |
| D. | 将少量高锰酸钾放入水中,得到的深紫色液体是溶液 |
6.小黎同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:
(1)如图1所示,在白色点滴板上进行实验,请将实验现象填入下表:
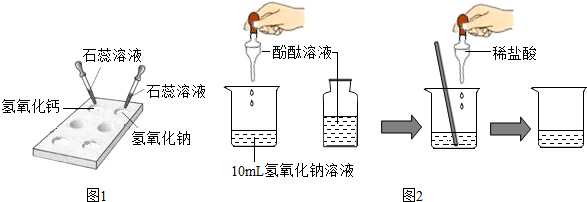
(2)回忆检验二氧化碳气体的反应,写出该反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
(3)二氧化硫(SO2)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式SO2+2NaOH═Na2SO3+H2O.
(4)如图2所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显红色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止,说明溶液呈中性.写出该反应的化学方程式NaOH+HCl═NaCl+H2O反应类型复分解反应;由此可知:中和反应的实质是H+和OH-反应生成H2O.
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质.(任写两点)
①都能使酸碱指示剂变色;
②碱能与酸性氧化物反应生成盐和水.
(1)如图1所示,在白色点滴板上进行实验,请将实验现象填入下表:
| 氢氧化钠溶液 | 氢氧化钙溶液 | |
| 加紫色石蕊溶液 | 蓝色 | 蓝色 |

(2)回忆检验二氧化碳气体的反应,写出该反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
(3)二氧化硫(SO2)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式SO2+2NaOH═Na2SO3+H2O.
(4)如图2所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显红色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止,说明溶液呈中性.写出该反应的化学方程式NaOH+HCl═NaCl+H2O反应类型复分解反应;由此可知:中和反应的实质是H+和OH-反应生成H2O.
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质.(任写两点)
①都能使酸碱指示剂变色;
②碱能与酸性氧化物反应生成盐和水.
5.下列有关溶液的说法正确的是( )
| A. | 某温度下两种不同物质的溶液,溶质质量分数相同,则这两种物质的溶解度一定相同 | |
| B. | 在一定温度下,同一种溶质其饱和溶液的溶质质量分数比不饱和溶液的大 | |
| C. | 均一、稳定的液体不都是溶液.碘酒是纯净物,所以不是溶液 | |
| D. | 溶液中溶质可以是一种或多种.溶液长期放置后,会出现分层现象 |
20.CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:
【查阅资料】
资料:已知碳酸钙与盐酸的复分解反应可自发进行.在常温下,测得浓度均为a%的下列六种溶液的pH大小情况:
表中pH大小情况揭示出复分解反应的一条规律,即较强酸发生类似反应可以生成较弱酸.下列反应均能发生,其中不符合该规律的是D(填字母).
A、H2SO4+2NaHCO3=Na2SO4+2H2O+2CO2↑ B、2HCl+CaS=CaCl2+H2S↑
C、CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D、H2S+CuSO4=H2SO4+CuS↓
【实验探究】小茜同学用这种大理石和盐酸反应来制取二氧化碳,为了得到纯净的二氧化碳,设计了如下装置,请你分析:
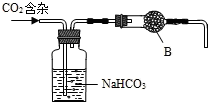
(1)制备的CO2气体中,可能含有的杂质是HCl、H2S、和水蒸气;
(2)上述装置中,NaHCO3溶液可以吸收HCl、H2S等酸性气体;
(3)B装置的干燥剂不能用生石灰的原因是氧化钙能与二氧化碳反应.
0 150514 150522 150528 150532 150538 150540 150544 150550 150552 150558 150564 150568 150570 150574 150580 150582 150588 150592 150594 150598 150600 150604 150606 150608 150609 150610 150612 150613 150614 150616 150618 150622 150624 150628 150630 150634 150640 150642 150648 150652 150654 150658 150664 150670 150672 150678 150682 150684 150690 150694 150700 150708 211419
【查阅资料】
资料:已知碳酸钙与盐酸的复分解反应可自发进行.在常温下,测得浓度均为a%的下列六种溶液的pH大小情况:
| 溶质 | H2SO4 | HCl | H2S | H2CO3 | HClO |
| pH | 小→大 | ||||
A、H2SO4+2NaHCO3=Na2SO4+2H2O+2CO2↑ B、2HCl+CaS=CaCl2+H2S↑
C、CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D、H2S+CuSO4=H2SO4+CuS↓
【实验探究】小茜同学用这种大理石和盐酸反应来制取二氧化碳,为了得到纯净的二氧化碳,设计了如下装置,请你分析:

(1)制备的CO2气体中,可能含有的杂质是HCl、H2S、和水蒸气;
(2)上述装置中,NaHCO3溶液可以吸收HCl、H2S等酸性气体;
(3)B装置的干燥剂不能用生石灰的原因是氧化钙能与二氧化碳反应.
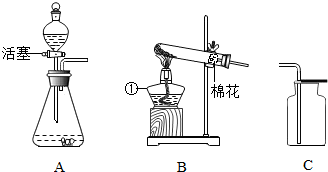

 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.