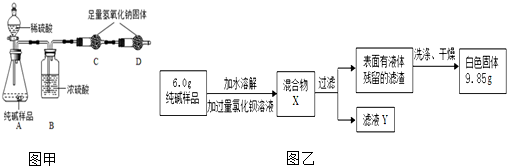
14. 某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图所示,装置气密性良好).一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.
某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图所示,装置气密性良好).一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.
[观察现象]①装置中右侧导管中的液面升高.
②铁钉生锈,试管底部有黑色固体物质.
[提出问题]导管中液面为何升高?黑色固体物质又是什么?
[理论分析]小组同学根据已学习过的知识分析得知,液面上升的原因是铁钉生锈消耗了试管内的氧气,使试管内压强低于大气压.
[猜想与假设]小组中的小明同学猜测该黑色固体可能含有:①Fe、②Fe3O4、③FeCl3、④C四种物质.
[分析与验证]小组同学根据小明的四种猜测做了以下分析:
(1)小强同学认为一定含有碳,该结论也得到小组同学的认可,理由是铁钉是铁合金,含有碳.
(2)小组同学不能确定是否含有铁,请你帮他们设计方案进行确认:
[知识链接]相信你一定在家中做过铁钉分别在水以及食盐水中生锈的实验,你的结论之一是铁钉在食盐水(填“水”或“食盐水”)中生锈快.
 某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图所示,装置气密性良好).一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.
某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图所示,装置气密性良好).一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.[观察现象]①装置中右侧导管中的液面升高.
②铁钉生锈,试管底部有黑色固体物质.
[提出问题]导管中液面为何升高?黑色固体物质又是什么?
[理论分析]小组同学根据已学习过的知识分析得知,液面上升的原因是铁钉生锈消耗了试管内的氧气,使试管内压强低于大气压.
[猜想与假设]小组中的小明同学猜测该黑色固体可能含有:①Fe、②Fe3O4、③FeCl3、④C四种物质.
[分析与验证]小组同学根据小明的四种猜测做了以下分析:
(1)小强同学认为一定含有碳,该结论也得到小组同学的认可,理由是铁钉是铁合金,含有碳.
(2)小组同学不能确定是否含有铁,请你帮他们设计方案进行确认:
| 实验步骤 | 实验现象 | 实验结论 |
| 你选用的试剂是: |
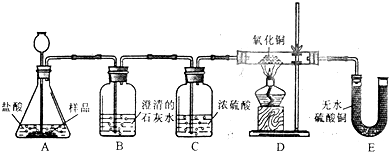
12.某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品,反应的化学方程式为:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.某研究性学习兴趣小组对该厂生产的烧碱样品进行如下探究.
【提出问题】烧碱样品中含有哪些杂质?
【猜想】(1)可能含有NaCl,作出此猜想的依据是电解的过程中氯化钠没有完全反应.
(2)可能含有碳酸钠,做出此猜想的理由是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示).
【实验设计】
【反思】小明认为上述实验不能说明样品中含有氯化钠,理由是在步骤②中加入盐酸时引入了氯离子.
【提出问题】烧碱样品中含有哪些杂质?
【猜想】(1)可能含有NaCl,作出此猜想的依据是电解的过程中氯化钠没有完全反应.
(2)可能含有碳酸钠,做出此猜想的理由是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示).
【实验设计】
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量的烧碱样品置于试管中加水溶解,用手触摸试管外壁. | 试管外壁发热 | 原因是氢氧化钠溶于水时放出热量 |
| ②向①所得的溶液中加入盐酸至过量. | 开始时无明显现象,过一段时间后有气泡产生. | 说明样品中含有杂质Na2CO3 |
| ③向②所得的溶液中加入硝酸银溶液. | 有白色沉淀产生. | AgNO3+NaCl═AgCl↓+NaNO3 说明样品中含有杂质氯化钠 |
10. 梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上表明锡纸的材质为“铝箔”.
梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上表明锡纸的材质为“铝箔”.
【提出问题】锡纸的材质到底是锡还是铝呢?小吴认为可以把锡纸放入盐酸中观察是否有气体放出来区别是锡还是铝,小周同学认为这样不能区别,理由是锡和铝都能与盐酸反应生成氢气.小施查阅资料发现锡的熔点为232℃,而铝的熔点为660℃,他用加热的方法区别出锡纸的材质是铝不是锡,接着同学们对铝这种金属进行探究.
【探究活动一】铝的含量分析
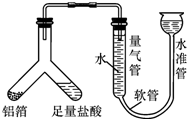
(1)小施用如图装置测定铝箔中金属铝的含量,检查该装置气密性的操作是从水准管一端注入水,待水准管和量气管出现较大高度差为止,静止几分钟,两侧高度差不缩小,证明装置气密性好.
(2)若测定进入量气管的气体体积为100mL(氢气的密度为0.09g/L),铝箔中金属铝的质量为0.081g(铝箔中只有铝能与盐酸反应生成气体).
【探究活动二】铝箔燃烧
同学们做铝箔燃烧的实验.小吴用坩埚钳夹持一小块铝箔放在酒精灯火焰上,轻轻晃动,观察到铝箔熔化,失去了光泽,但铝箔并不燃烧;小周另取一块铝箔,用砂纸仔细打磨,再用坩埚钳夹持放在酒精灯的火焰上,观察到铝箔仍不能燃烧.
(1)小施同学认为铝箔不能在空气中燃烧是因为铝与氧气反应生成一层致密的氧化铝薄膜附在铝的表面,阻止反应的进行,这也是铝箔抗腐蚀性强的原因.
(2)小施同学改进了实验,让铝箔燃烧并发出耀眼的白光,小施同学的实验方案是将铝箔卷曲,尖端夹一根火柴,将火柴引燃后,把火柴和铝箔一起伸入到盛有氧气的集气瓶中即可观察到铝箔燃烧并发出耀眼的白光.
【探究活动三】小吴将打磨后的铝片与铜盐溶液反应,现象如下:
(1)铝与氯化铜溶液反应的化学方程式为2Al+3CuCl2═2AlCl3+3Cu.
(2)对比两个实验,小周推测对铝与铜盐溶液的反应可能有促进作用的离子是Cl-(填离子符号),为了验证此推测,小施向实验一的CuSO4溶液中加入1gNaCl(填化学式)固体,立即观察到铝片上出现大量红色的铜.
 梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上表明锡纸的材质为“铝箔”.
梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上表明锡纸的材质为“铝箔”.【提出问题】锡纸的材质到底是锡还是铝呢?小吴认为可以把锡纸放入盐酸中观察是否有气体放出来区别是锡还是铝,小周同学认为这样不能区别,理由是锡和铝都能与盐酸反应生成氢气.小施查阅资料发现锡的熔点为232℃,而铝的熔点为660℃,他用加热的方法区别出锡纸的材质是铝不是锡,接着同学们对铝这种金属进行探究.
【探究活动一】铝的含量分析
(1)小施用如图装置测定铝箔中金属铝的含量,检查该装置气密性的操作是从水准管一端注入水,待水准管和量气管出现较大高度差为止,静止几分钟,两侧高度差不缩小,证明装置气密性好.
(2)若测定进入量气管的气体体积为100mL(氢气的密度为0.09g/L),铝箔中金属铝的质量为0.081g(铝箔中只有铝能与盐酸反应生成气体).
【探究活动二】铝箔燃烧
同学们做铝箔燃烧的实验.小吴用坩埚钳夹持一小块铝箔放在酒精灯火焰上,轻轻晃动,观察到铝箔熔化,失去了光泽,但铝箔并不燃烧;小周另取一块铝箔,用砂纸仔细打磨,再用坩埚钳夹持放在酒精灯的火焰上,观察到铝箔仍不能燃烧.
(1)小施同学认为铝箔不能在空气中燃烧是因为铝与氧气反应生成一层致密的氧化铝薄膜附在铝的表面,阻止反应的进行,这也是铝箔抗腐蚀性强的原因.
(2)小施同学改进了实验,让铝箔燃烧并发出耀眼的白光,小施同学的实验方案是将铝箔卷曲,尖端夹一根火柴,将火柴引燃后,把火柴和铝箔一起伸入到盛有氧气的集气瓶中即可观察到铝箔燃烧并发出耀眼的白光.
【探究活动三】小吴将打磨后的铝片与铜盐溶液反应,现象如下:
| 实验一:4mL8%CuSO4溶液 | 实验二:4mL8%CuCl2溶液 | |
| 实验 现象 | 短时间内无变化,一段时间后铝片上才出现少量红色的铜 | 铝片上迅速有红色的铜出现 |
(2)对比两个实验,小周推测对铝与铜盐溶液的反应可能有促进作用的离子是Cl-(填离子符号),为了验证此推测,小施向实验一的CuSO4溶液中加入1gNaCl(填化学式)固体,立即观察到铝片上出现大量红色的铜.
9. 有一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.如表是实验中可能出现的现象与对应结论,请你填写表中空白处的相关内容:
有一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.如表是实验中可能出现的现象与对应结论,请你填写表中空白处的相关内容:
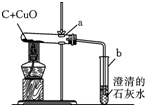
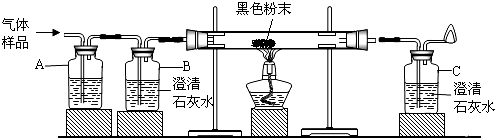
通过实验及分析,确定该粉末为氧化铜和碳粉混合物,为了进一步探究它们的性质,探究小组又利用这种混合物补充做了如图所示实验:
①试管a中的化学方程式为C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
②氧化铜和碳反应属于置换反应(填基本反应类型).
③最能说明a试管中氧化铜和碳已完全反应的实验现象是b中的导管口不再产生气泡.
0 150501 150509 150515 150519 150525 150527 150531 150537 150539 150545 150551 150555 150557 150561 150567 150569 150575 150579 150581 150585 150587 150591 150593 150595 150596 150597 150599 150600 150601 150603 150605 150609 150611 150615 150617 150621 150627 150629 150635 150639 150641 150645 150651 150657 150659 150665 150669 150671 150677 150681 150687 150695 211419
 有一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.如表是实验中可能出现的现象与对应结论,请你填写表中空白处的相关内容:
有一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.如表是实验中可能出现的现象与对应结论,请你填写表中空白处的相关内容:| 现象 | 结论 |
| 溶液呈蓝色,有黑色不溶物 | 含CuO、C |
| 溶液颜色无明显变化,有黑色不溶物 | 只含C |
①试管a中的化学方程式为C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
②氧化铜和碳反应属于置换反应(填基本反应类型).
③最能说明a试管中氧化铜和碳已完全反应的实验现象是b中的导管口不再产生气泡.
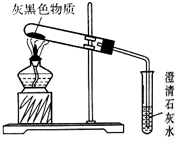 镁是一种银白色的金属,但实验室看到的镁条常常有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?甲同学认为是MgO;乙同学认为是Mg2(OH)2CO3;丙同学认为是Mg(OH)2.
镁是一种银白色的金属,但实验室看到的镁条常常有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?甲同学认为是MgO;乙同学认为是Mg2(OH)2CO3;丙同学认为是Mg(OH)2.
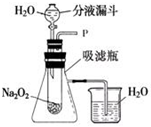 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.