17.已知FeO、Fe2O3、Fe3O4组成的混合物中,铁与氧的质量比为21:8,则混合物中FeO、Fe2O3、Fe3O4三种物质的质量比可能是( )
| A. | 9:15:5 | B. | 9:20:13 | C. | 5:7:13 | D. | 5:9:15 |
16.生产自来水的时,向水中通入一定量的氯气.这是因为氯气跟水反应,生成盐酸和次氯酸,其中次氯酸具有强氧化性,可以起到消毒灭菌的作用.某学生用这种自来水来配制下列物质的溶液.通常不会使药品明显变质的是( )
| A. | 石蕊试液 | B. | 硝酸银溶液 | C. | 碳酸钠溶液 | D. | 硝酸钾溶液 |
15.某化学实验小组的同学对实验室2瓶氢氧化钠固体产生了兴趣,为探究其成分进行了有关实验.请你参与他们进行的探究活动:
【提出问题】久置氢氧化钠固体的成分是什么?
【猜想与假设】猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:NaOH和Na2CO3
【实验与探究】
(1)实验如下:
(2)为了进一步的验证猜想结果,小明同学提出如下实验方案:继续实验二,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则此瓶中猜想Ⅲ成立;若酚酞不变红,则猜想Ⅱ成立.
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈碱性(填“酸”或“碱”),能使酚酞变红,因此他认为该方案的操作步骤中应该改进的是滴加过量的氯化钡溶液
【反思与交流】久置的固体氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH═Na2CO3+H2O.
【提出问题】久置氢氧化钠固体的成分是什么?
【猜想与假设】猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:NaOH和Na2CO3
【实验与探究】
(1)实验如下:
| 实验操作步骤 | 实验现象 | 结论及解释 |
| 实验一:取其中一瓶的少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的稀盐酸. | 实验过程中始终没有气泡产生. | 则证明此瓶中猜想Ⅰ成立. |
| 实验二:取另一瓶中的少量固体样品于试管中,加蒸馏水完全溶解,然后滴加少量氯化钡溶液. | 实验过程中产生 白色沉淀 | 则证明猜想Ⅱ或Ⅲ成立. 此过程中发生反应的化学方程式为BaCl2+Na2CO3═BaCO3↓+2NaCl |
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈碱性(填“酸”或“碱”),能使酚酞变红,因此他认为该方案的操作步骤中应该改进的是滴加过量的氯化钡溶液
【反思与交流】久置的固体氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH═Na2CO3+H2O.
13.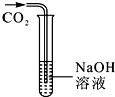 化学反应也有“悄悄”进行的.小明和他的同学对二氧化碳与氢氧化钠溶液的反应进行了如下探究.
化学反应也有“悄悄”进行的.小明和他的同学对二氧化碳与氢氧化钠溶液的反应进行了如下探究.
探究一:二氧化碳是否与氢氧化钠发生了化学反应?
将二氧化碳通入盛有氢氧化钠溶液的大试管(如图).取少量大试管中的液体于另一支试管中,滴加足量的稀盐酸,观察到有气泡产生,证明二氧化碳与氢氧化钠发生了反应;
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】小明认为溶质是Na2CO3;小刚认为溶质是Na2CO3和NaOH;
【查阅资料】CaCl2溶液呈中性;
【实验验证】
小刚为了验证自己的猜想,进行了如下实验,请你补充完整.
【实验反思】写出二氧化碳与氢氧化钠反应的化学方程式CO2+2NaOH=Na2CO3+H2O;
【实验拓展】同学们联想到氢氧化钠与稀硫酸发生中和反应也观察不到明显现象,为了确定其反应是否发生,由同学设计了如下的实验方案:先用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀硫酸,边滴加边测定混合溶液的pH.请你分析上述方案中,为什么要“当测定pH小于或等于7时”才可证明发生反应了,其原因是pH小于或等于7时,表明OH-被消耗,说明酸碱发生了反应;
(注意:若答对以下小题将奖励4分,但全卷总分不超过60分)
【总结提高】试设计两种不同方案证明氢氧化钠和稀硫酸确实发生了反应,从实验操作、实验现象和实验结论等方面加以说明.
 化学反应也有“悄悄”进行的.小明和他的同学对二氧化碳与氢氧化钠溶液的反应进行了如下探究.
化学反应也有“悄悄”进行的.小明和他的同学对二氧化碳与氢氧化钠溶液的反应进行了如下探究.探究一:二氧化碳是否与氢氧化钠发生了化学反应?
将二氧化碳通入盛有氢氧化钠溶液的大试管(如图).取少量大试管中的液体于另一支试管中,滴加足量的稀盐酸,观察到有气泡产生,证明二氧化碳与氢氧化钠发生了反应;
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】小明认为溶质是Na2CO3;小刚认为溶质是Na2CO3和NaOH;
【查阅资料】CaCl2溶液呈中性;
【实验验证】
小刚为了验证自己的猜想,进行了如下实验,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量试管中的溶液于试管中,加入足量CaCl2溶液,过滤;②向滤液中滴加适量酚酞试液 | 酚酞试液变红 | 小刚猜想成立 |
【实验拓展】同学们联想到氢氧化钠与稀硫酸发生中和反应也观察不到明显现象,为了确定其反应是否发生,由同学设计了如下的实验方案:先用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀硫酸,边滴加边测定混合溶液的pH.请你分析上述方案中,为什么要“当测定pH小于或等于7时”才可证明发生反应了,其原因是pH小于或等于7时,表明OH-被消耗,说明酸碱发生了反应;
(注意:若答对以下小题将奖励4分,但全卷总分不超过60分)
【总结提高】试设计两种不同方案证明氢氧化钠和稀硫酸确实发生了反应,从实验操作、实验现象和实验结论等方面加以说明.
| 实验操作 | 实验现象 | 实验结论 | |
| 方案一 | 氢氧化钠和稀硫酸发生了反应 | ||
| 方案二 |
12.生活在密闭狭小的特殊环境(如潜艇、太空舱)里,O2会越来越少,CO2会越来越多,因此将CO2转化为O2,不仅有科学意义也有重要的实用价值.据科学文献报道,NiFe2O4在一定条件下既能促进CO2分解又可重复使用.NiFe2O4在此反应中是( )
| A. | 粘合剂 | B. | 制冷剂 | C. | 防腐剂 | D. | 催化剂 |
11.氢化钙固体是登山运动员常用的能源提供剂.某探究小组的同学通过查阅资料得知,氢化钙(CaH2)遇水反应生成氢氧化钙和氢气.探究小组的同学把一定量的CaH2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液.经检验滤渣的成分是碳酸钙.
[提出问题]滤液中溶质的成分是什么?
[猜想与假设]
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经讨论,大家认为猜想四不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
[实验验证]
[反思与拓展]
(1)若向NH4Cl的溶液中加一定量CaH2,充分反应,产生的气体是氢气、氨气.
(2)登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是携带安全.
0 150497 150505 150511 150515 150521 150523 150527 150533 150535 150541 150547 150551 150553 150557 150563 150565 150571 150575 150577 150581 150583 150587 150589 150591 150592 150593 150595 150596 150597 150599 150601 150605 150607 150611 150613 150617 150623 150625 150631 150635 150637 150641 150647 150653 150655 150661 150665 150667 150673 150677 150683 150691 211419
[提出问题]滤液中溶质的成分是什么?
[猜想与假设]
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经讨论,大家认为猜想四不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
[实验验证]
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想二不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | 先无变化后产生气泡 | 猜想三成立 |
(1)若向NH4Cl的溶液中加一定量CaH2,充分反应,产生的气体是氢气、氨气.
(2)登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是携带安全.


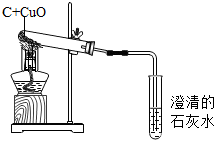 如图所示是木炭还原氧化铜的实验,写出该反应的化学方程式:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2 ↑.实验完毕后,发现试管内仍有黑色固体物质存在,其中网罩的作用是提高温度.澄清石灰水的作用是验证反应是否产生二氧化碳.
如图所示是木炭还原氧化铜的实验,写出该反应的化学方程式:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2 ↑.实验完毕后,发现试管内仍有黑色固体物质存在,其中网罩的作用是提高温度.澄清石灰水的作用是验证反应是否产生二氧化碳.