11.一种名为“污渍爆炸盐”的洗涤产品能高效去除衣物上的顽固污渍,某校化学研究性学习小组的同学在老师的指导下对该产品开展了以下探究活动.
【查阅资料】“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4相对分子质量为122),它是一种白色固体粉末,易溶于水且能与水反应生成一种碳酸盐和一种强氧化性的物质,是当前使用最为广泛的洗涤助剂之一.
【实验探究一】过碳酸钠的性质
为探究过碳酸钠的性质,同学们设计了以下实验,请按要求完成表格内容:
【实验探究二】:过碳酸钠含量测定
老师给同学们一份含碳酸钠杂质的过碳酸钠样品(不含其它杂质)要求设计方案测定该样品中过碳酸钠的含量,同学们经讨论设计了如图所示的实验装置.图中装置B盛装氢氧化钠溶液、C盛装澄清石灰水、D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气.

操作步骤:(1)首先关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气排出锥形瓶中的空气,此时装置B的作用是吸收反应前锥形瓶中的二氧化碳;
(2)依次关闭活塞K1、K3、K4,打开活塞K2、K,此时E中装入碱石灰的作用是吸收生成的二氧化碳,反应完全后关闭活塞K,再次打开活塞K1通入氮气的作用是将装置中的气体排出,被E装置完全吸收.
(3)同学们在实验前称取了44克含碳酸钠杂质的过碳酸钠样品(不含其他杂质)进行实验.根据实验后E装置增重17.6克,求该样品中过碳酸钠的含量.(写出计算过程,结果保留一位小数)
(4)装置F的作用是防止空气中的二氧化碳和水蒸气进入E装置,影响测定结果的准确性,如不连接装置F,测定的过碳酸钠含量会偏低(填“偏高”或“偏低”).
0 150485 150493 150499 150503 150509 150511 150515 150521 150523 150529 150535 150539 150541 150545 150551 150553 150559 150563 150565 150569 150571 150575 150577 150579 150580 150581 150583 150584 150585 150587 150589 150593 150595 150599 150601 150605 150611 150613 150619 150623 150625 150629 150635 150641 150643 150649 150653 150655 150661 150665 150671 150679 211419
【查阅资料】“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4相对分子质量为122),它是一种白色固体粉末,易溶于水且能与水反应生成一种碳酸盐和一种强氧化性的物质,是当前使用最为广泛的洗涤助剂之一.
【实验探究一】过碳酸钠的性质
为探究过碳酸钠的性质,同学们设计了以下实验,请按要求完成表格内容:
| 序号 | 实验步骤 | 实验现象 | 实验结论(或解释) |
| ① | 向盛有过碳酸钠固体的试管中加入适量水 | 固体溶解 | 过碳酸钠易溶于水,能与水发生反应. |
| ② | 向序号①的所得溶液中加入适量的二氧化锰 | 有大量气泡产生 | / |
| ③ | 将带火星的木条置于试管口 | 木条复燃 | 序号②试管中产生的气体是氧气;过碳酸钠溶于水能生成过氧化氢. |
| ④ | 取序号 ③试管中的上层清液加入氯化钙溶液 | 产生白色沉淀 | 反应的化学方程式Na2CO3+CaCl2═CaCO3↓+2NaCl. |
| 小结 | 过碳酸钠与水反应的化学方程式是Na2CO4+H2O═Na2CO3+H2O2. | ||
老师给同学们一份含碳酸钠杂质的过碳酸钠样品(不含其它杂质)要求设计方案测定该样品中过碳酸钠的含量,同学们经讨论设计了如图所示的实验装置.图中装置B盛装氢氧化钠溶液、C盛装澄清石灰水、D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气.

操作步骤:(1)首先关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气排出锥形瓶中的空气,此时装置B的作用是吸收反应前锥形瓶中的二氧化碳;
(2)依次关闭活塞K1、K3、K4,打开活塞K2、K,此时E中装入碱石灰的作用是吸收生成的二氧化碳,反应完全后关闭活塞K,再次打开活塞K1通入氮气的作用是将装置中的气体排出,被E装置完全吸收.
(3)同学们在实验前称取了44克含碳酸钠杂质的过碳酸钠样品(不含其他杂质)进行实验.根据实验后E装置增重17.6克,求该样品中过碳酸钠的含量.(写出计算过程,结果保留一位小数)
(4)装置F的作用是防止空气中的二氧化碳和水蒸气进入E装置,影响测定结果的准确性,如不连接装置F,测定的过碳酸钠含量会偏低(填“偏高”或“偏低”).
 原子得到或失去电子后形成离子.某离子的结构示意图如图
原子得到或失去电子后形成离子.某离子的结构示意图如图 海洋是丰富的化学资源宝库.通过晾晒海水,可得到含少量泥沙的粗盐.为得到比较纯净的NaCl(不考虑可溶性杂质),设计了如图所示的实验操作:
海洋是丰富的化学资源宝库.通过晾晒海水,可得到含少量泥沙的粗盐.为得到比较纯净的NaCl(不考虑可溶性杂质),设计了如图所示的实验操作: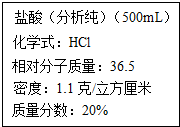 某学校实验室从化学试剂商店买回的一瓶未开封的盐酸试剂(氯化氢水溶液),试剂瓶的标签上的部分内容如图,请仔细阅读后计算
某学校实验室从化学试剂商店买回的一瓶未开封的盐酸试剂(氯化氢水溶液),试剂瓶的标签上的部分内容如图,请仔细阅读后计算